2021-2022學(xué)年江蘇省常熟市高三(下)開學(xué)化學(xué)試卷
發(fā)布:2024/11/17 2:0:2
一、單項選擇題:共14題,每題3分,共42分。每題只有一個選項最符合題意。
-
1.已知反應(yīng):2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O,下列關(guān)于該反應(yīng)說法錯誤的是( )
A.Cl2是非電解質(zhì) B.氧化性:NaClO3>Cl2 C.氧化產(chǎn)物和還原產(chǎn)物的物質(zhì)的量之比為1:2 D.產(chǎn)物ClO2和Cl2都可以用于自來水消毒殺菌 組卷:54引用:1難度:0.7 -
2.實驗室制備Na2S2O3的反應(yīng)原理:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2。下列有關(guān)說法正確的是( )
A.SO2為非極性分子,反應(yīng)中作氧化劑 B.Na2S的電子式為 
C.CO32-中C形成3個δ鍵,為三角錐形 D.基態(tài)O原子的軌道表示式:  組卷:33引用:1難度:0.7
組卷:33引用:1難度:0.7 -
3.水合肼(N2H4?H2O)為無色透明的油狀發(fā)煙液體,是一種重要的精細(xì)化工原料,其制備的反應(yīng)原理為NaClO+2NH3═N2H4?H2O+NaCl.下列關(guān)于實驗室制備水合肼的操作不正確的是( )
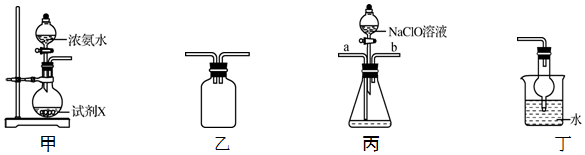
A.裝置甲中試劑X可以選擇生石灰 B.裝置乙作為反應(yīng)過程的安全瓶 C.裝置丙制備水合肼時氨氣從b口進(jìn)入 D.裝置丁可用于吸收多余的尾氣 組卷:84引用:6難度:0.6 -
4.化學(xué)與生產(chǎn)、生活關(guān)系密切。下列物質(zhì)的性質(zhì)和用途都正確且有對應(yīng)關(guān)系的是( )
A.“84”消毒液和潔廁靈可發(fā)生反應(yīng),可更好地消殺新冠變異毒株奧密克戎 B.油脂能水解,可以用于生成氨基酸片 C.葡萄糖具有氧化性,可用于制銀鏡工藝 D.KMnO4溶液可氧化水果釋放的催熟劑,用浸泡過KMnO4溶液的硅藻土可用于水果保鮮 組卷:2引用:1難度:0.8 -
 5.X、Y、Z、W為前四周期原子序數(shù)依次增大的四種元素,X、Y、Z的原子半徑和最外層電子數(shù)如圖所示。W的基態(tài)原子最外層只有1個電子且內(nèi)層電子全部充滿。下列說法正確的是( )
5.X、Y、Z、W為前四周期原子序數(shù)依次增大的四種元素,X、Y、Z的原子半徑和最外層電子數(shù)如圖所示。W的基態(tài)原子最外層只有1個電子且內(nèi)層電子全部充滿。下列說法正確的是( )A.第一電離能:X<Y B.W的基態(tài)原子的電子排布式:1s22s22p63s23p64s1 C.Z元素沒有正化合價 D.X的簡單氫化物分子間能形成氫鍵 組卷:11引用:2難度:0.6
二、非選擇題:共4題,共58分。
-
17.某興趣小組用電鍍污泥[含Cr(OH)3,Ni(OH)2、Cu(OH)2、FeO及Fe(OH)3]制備K2Cr2O7晶體,流程如圖:

已知:①在堿性條件下,三價鉻可被H2O2氧化為六價鉻;在酸性條件下,六價鉻可被H2O2還原為三價鉻。
②Cr(OH)3具有兩性。
③六價鉻在溶液中物種分布分?jǐn)?shù)與pH關(guān)系如圖1所示。
請回答:
(1)“氨浸”時,鎳及銅分別以[Ni(NH3)6]2+及[Cu(NH3)4]2+形式被浸出,畫出[Cu(NH3)4]2+的結(jié)構(gòu)簡式。
(2)實驗室在“氧化”時可以用了圖2裝置,生成CrO42-的離子方程式為,具體操作時應(yīng)該先滴入溶液。
(3)步驟“調(diào)pH”值時,加入適量硫酸而不能過量的原因是。
(4)為了測定K2Cr2O7產(chǎn)品的純度,可采用滴定法:(K2Cr2O7:294g/mol)稱取重鉻酸鉀試樣wg配成250mL溶液,取出25.00mL于錐形瓶中,加10mL2mol/LH2SO4和足量碘化鉀,使Cr2O72-完全轉(zhuǎn)化為Cr3+,再用amol/L的EDTA(用H4Y表示)標(biāo)準(zhǔn)溶液進(jìn)行滴定,(Cr3++Y4+═CrY-)實驗消枆EDTA標(biāo)準(zhǔn)溶液bmL,則該樣品的純度為(寫出計算過程)。
(5)PbCrO4是一種黃色顏料,請設(shè)計由K2Cr2O7溶液制備PbCrO4的實驗方案:。[實驗中須使用的試劑有:6mol?L-1的KOH溶液,0.5mol?L-1Pb(NO3)2溶液]。
已知:①Pb(OH)2開始沉淀時pH為7.2,完全沉淀時pH為8.7,PbCrO4的Ksp為2.8×10-13。
②PbCrO4可由沸騰的鉻酸鹽溶液與鉛鹽溶液作用制得,當(dāng)制得PbCrO4晶種后更易生成PbCrO4沉淀。組卷:10引用:1難度:0.5 -
18.含氨廢氣的利用利處理意義重大。
(1)NH3與O2作用
4NH3(g)+3O2(g)→2N2(g)+6H2O(1)ΔH=-akJ?mol-1
4NH3(g)+5O2(g)→4NO(g)+6H2O(1)ΔH=-bkJ?mol-1
4NH3(g)+4O2(g)→2N2O(g)+6H2O(1)ΔH=-ckJ?mol-1
則4NH3(g)+6NO(g)→5N2(g)+6H2O(1)ΔH=kJ?mol-1。
工業(yè)尾氣中NH3可通過催化氧化為N2除去。將一定比例NH3、O2和N2的混合氣體以一定流速通過裝有催化劑的反應(yīng)管,NH3的轉(zhuǎn)化率、N2的選擇性[×100%]與溫度的關(guān)系如圖1所示。2n生成(N2)n總轉(zhuǎn)化(NH3)
(2)催化氧化除去尾氣中的NH3應(yīng)選擇反應(yīng)溫度不高于250℃的原因。
(3)氮氧化物(SCR)技術(shù)脫除煙氣中氨與氮氧化物。反應(yīng)原理如圖2所示。設(shè)參加反應(yīng)的NO和NO2的物質(zhì)的量相等,寫出圖中發(fā)生的SCR技術(shù)無害化處理的化學(xué)方程式:。
(4)在V-Ti-O-Mo催化劑作用下,利用氨氧化合成重要原料2-氰基吡啶( ):2
):2 (s)+2NH3(g)+3O2(g)2催化劑
(s)+2NH3(g)+3O2(g)2催化劑 (s)+6H2O(g)ΔH<0。為探究催化劑V-Ti-O-Mo在不同溫度下對反應(yīng)的影響,在10L容器中加入2-甲基吡啶、氨、氧氣的物質(zhì)的量分別為10mol、60mol和40mol,在360~400℃下用時1h分別進(jìn)行了多組實驗,實驗結(jié)果如表所示。已知:收率=轉(zhuǎn)化率×選擇性。
(s)+6H2O(g)ΔH<0。為探究催化劑V-Ti-O-Mo在不同溫度下對反應(yīng)的影響,在10L容器中加入2-甲基吡啶、氨、氧氣的物質(zhì)的量分別為10mol、60mol和40mol,在360~400℃下用時1h分別進(jìn)行了多組實驗,實驗結(jié)果如表所示。已知:收率=轉(zhuǎn)化率×選擇性。
催化劑V-Ti-O-Mo的最佳催化溫度范圍是:反應(yīng)溫度/℃ 2-甲基吡啶轉(zhuǎn)化率/% 選擇性/% 收率/% 360 80.7 94.9 76.6 370 86.5 95.5 82.6 380 91.1 93.5 85.2 390 95.4 80.1 76.4 400 97.7 58.1 56.8 。有人認(rèn)為360℃時,2-甲基吡啶轉(zhuǎn)化率80.7%不是該反應(yīng)的平衡轉(zhuǎn)化率,其理由是。
(S)用CuO-CeO2作催化劑參與NH3-sco反應(yīng)。路徑如圖3所示。高分散的活性CuO將是NH3轉(zhuǎn)移至CeO2表面,隨后通過Ce4+與Ce3+之間的快速轉(zhuǎn)化,NH3形成NHx。當(dāng)沒有氣態(tài)氧存在時,NHx與晶格氧反應(yīng)生成N2和N2O,同時出現(xiàn)氧空位。隨后通入氣態(tài)氧的作用。 組卷:18引用:1難度:0.6
組卷:18引用:1難度:0.6


