2022年天津市十二區縣重點學校聯考高考化學模擬試卷(二)
發布:2024/4/20 14:35:0
一、選擇題(本大題共12小題,共36分)
-
1.大氣中氮氧化物和碳氫化合物受紫外線作用可產生二次污染物光化學煙霧,其中某些反應過程如圖所示。下列說法不正確的是( )
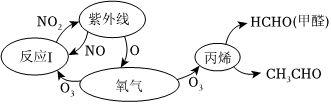
A.NO2 不是酸性氧化物 B.O2和O3 是氧的兩種同素異形體 C.反應I屬于氧化還原反應 D.煙霧是一種固溶膠,其分散劑是空氣 組卷:122引用:8難度:0.9 -
2.下面有關晶體的敘述中,不正確的是( )
A.氯化銫晶體中,每個Cs+周圍緊鄰8個Cl- B.金剛石為空間網狀結構,由共價鍵形成的碳原子環中,最小的環上有6個碳原子 C.干冰晶體中,每個CO2分子周圍緊鄰12個CO2分子 D.金屬銅屬于六方最密堆積結構,金屬鎂屬于面心立方最密堆積結構 組卷:66引用:3難度:0.6 -
3.“嫦娥五號”帶回了富含氦-3的月壤,氦-3可作為未來可控核聚變(3He+3He→4He+21H)的清潔能源。下列說法正確的是( )
A.氦-3聚變屬于化學變化 B.3He和4He具有相同的性質 C.He位于第1周期第ⅡA族 D.2H和3He具有相同的中子數 組卷:35引用:2難度:0.8 -
4.化學與生產、生活及環境密切相關,下列有關說法正確的是( )
A.工業上海水提鎂涉及的一系列反應都是氧化還原反應 B.汽車尾氣污染物中含有的氮氧化物,是汽油或柴油不完全燃燒造成的 C.江河入海口形成的三角洲與膠體聚沉有關 D.用于光纜通信的光導纖維和制作航天服的聚酯纖維都是新型無機非金屬材料 組卷:79引用:4難度:0.9 -
5.化學是現代生產、生活與科技的中心學科之一,下列與化學有關的說法,錯誤的是( )
A.PM2.5是指空氣中直徑小于或等于2.5 μm的顆粒物,PM2.5的值越大,則代表空氣污染越嚴重 B.2018年22歲的中國科學家曹原發現將兩層石墨烯以1.1°的“魔角”旋轉疊加在一起時可得到一種超導體。石墨烯是碳元素的一種同素異形體 C.顧名思義,蘇打水就是蘇打的水溶液,也叫弱堿性水,是帶有弱堿性的飲料 D.工業上定期去除鍋爐中的水垢,往往可以先加入Na2CO3溶液浸泡處理后,再加入鹽酸去除沉淀物 組卷:135引用:5難度:0.5
二、綜合題(本大題共4小題,共64分)
-
15.我國科學家在某雜志上發表研究報告稱,利用鉻同位素的系統分析發現,“古代大氣氧含量高于現代水平的1%”。鉻的同位素有
Cr、5024Cr、5224Cr、5324Cr.鉻及其化合物在生活、生產中有廣泛應用。回答下列問題:5424
(1)基態Cr的價層電子排布圖為5324。
(2)交警用“酒精儀”查酒駕,其化學反應原理如下:
2K2Cr2O7+3CH3CH2OH+8H2SO4→3CH3COOH+2Cr2(SO4)3+2K2SO4+11H2O
①CH3CH2OH、CH3COOH的沸點高于對應的CH3OCH3(二甲醚)、HCOOCH3(甲酸甲酯),其主要原因是。
②CH3COOH分子中碳原子的雜化類型是;CH3COOH分子中σ鍵和π鍵數目之比為。
③K2SO4晶體中陰離子的空間構型是。上述反應中,只含極性鍵的極性分子有(填分子式)。
(3)晶體鉻的晶胞結構如圖1所示,其堆積模型為;鉻原子的配位數為。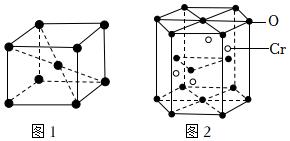
(4)鉻的一種氧化物晶胞結構如圖2所示。六棱柱邊長為a nm,高為b nm,NA代表阿伏加德羅常數的值。該晶體的化學式為;該晶體的密度ρ=g?cm-3。組卷:75引用:3難度:0.5 -
16.CO和NO是汽車尾氣中的主要污染物,易引起酸雨、溫室效應和光化學煙霧等環境污染問題。隨著我國機動車保有量的飛速發展,汽車尾氣的有效處理變得迫在眉睫。其中的一種方法為2CO(g)+2NO(g)=N2(g)+2CO2(g),請回答下列問題:
(1)已知該反應為自發反應,則該反應的反應熱△H0(填“>”或“<”或“=”)
(2)已知:N2(g)+O2(g)═2NO(g)△H=akJ?mol-1
C(s)+O2(g)═CO2(g)△H=bkJ?mol-1
2C(s)+O2(g)═2CO(g)△H=ckJ?mol-1
則2CO(g)+2NO(g)═N2(g)+2CO2(g)△H=kJ?mol-1(用含a、b、c的表達式表示)。
(3)一定溫度下,將2molCO、4molNO充入一恒容密閉容器。已知起始壓強為1MPa,到達平衡時,測得N2的物質的量為0.5mol,則:
①該溫度此反應用平衡分壓代替平衡濃度的平衡常數Kp=。(寫出計算表示式)
②該條件下,可判斷此反應到達平衡的標志是。
A.單位時間內,斷裂2molC=O同時形成1molN≡N。
B.混合氣體的平均相對分子質量不再改變。
C.混合氣體的密度不再改變。
D.CO與NO的轉化率比值不再改變。
(4)某研究小組探究催化劑對CO、NO轉化的影響。將CO和NO以一定的流速通過兩種不同的催化劑進行反應,相同時間內測量逸出氣體中N2的含量,從而確定尾氣脫氮率(即NO的轉化率),結果如圖1所示:
①由圖可知:要達到最大脫氮率,該反應應采取的最佳實驗條件為。
②若低于200℃,圖中曲線I脫氮率隨溫度升高變化不大的主要原因為。
(5)電解NO制備NH4NO3,其工作原理如圖2所示,為使電解產物全部轉化為NH4NO3,需要補充物質A,A是,理由是。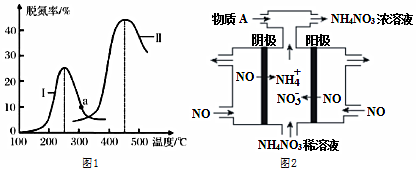 組卷:56引用:2難度:0.5
組卷:56引用:2難度:0.5


