2023年江蘇省無錫市錫山區天一實驗學校中考化學一模試卷
發布:2024/4/20 14:35:0
一、選擇題(本題包括20題,每小題只有1個選項符合題意。1~10每小題1分,11~20每小題1分,共30分)
-
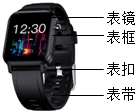 1.智能手表的部分信息如圖,下列描述中相關性質屬于化學性質的是( )
1.智能手表的部分信息如圖,下列描述中相關性質屬于化學性質的是( )A.玻璃透光性好作表鏡 B.鈦合金耐腐蝕作表框 C.不銹鋼硬度大作表扣 D.橡膠彈性良好作表帶 組卷:765引用:30難度:0.7 -
2.pH試紙能測定溶液的酸堿度,試紙自身顏色為( )
A.黃色 B.白色 C.紫色 D.藍色 組卷:45引用:3難度:0.7 -
3.下列物質俗稱、化學式相符合的一組是( )
A.火堿 Na2CO3 B.熟石灰 CaO C.生石灰 CaCO3 D.燒堿 NaOH 組卷:69引用:10難度:0.6 -
4.下列操作正確的是( )
A. 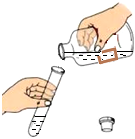
傾倒液體B. 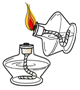
點燃酒精燈C. 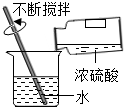
稀釋濃硫酸D. 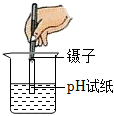
測定溶液酸堿度組卷:26引用:7難度:0.7 -
5.下列有關實驗現象的描述正確的是( )
A.打開盛濃鹽酸的瓶塞有白煙生成 B.小木條蘸取濃硫酸后,小木條變黑 C.硫在空氣中燃燒發出藍紫色火焰 D.稀硫酸能使紫色石蕊溶液變藍 組卷:43引用:6難度:0.6 -
6.下列物質放入水中,能形成溶液的是( )
A.泥沙 B.面粉 C.蔗糖 D.汽油 組卷:407引用:27難度:0.9 -
7.建立模型是學習化學的重要方法。下列有關模型正確的是( )
A. 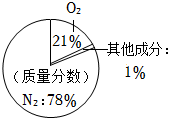
空氣組成模型B. 
原子結構模型C. 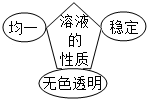
溶液性質模型D. 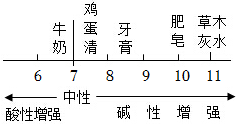
物質酸堿度模型組卷:279引用:10難度:0.5 -
8.下列化學家與酸堿指示劑的發現有關的是( )
A.門捷列夫 B.阿伏加德羅 C.波義耳 D.拉瓦錫 組卷:41引用:2難度:0.8 -
9.部分水果及飲料的pH如下:
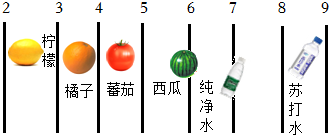
下列說法正確的是( )A.西瓜汁顯堿性 B.橘子汁中滴入酚酞,溶液變紅 C.蘇打水顯酸性 D.胃酸過多的人應該少飲檸檬水 組卷:446引用:19難度:0.7
二、解答題(共8小題,滿分50分)
-
27.鐵及其化合物在生產生活中應用廣泛。
Ⅰ.鐵的性質和防護
(1)某麥片中含微量鐵粉,食用后鐵粉與胃酸(含HCl)反應轉化為人體可吸收的微量元素,此反應的化學方程式為,基本反應類型為。
(2)鋼鐵的銹蝕主要是鐵與空氣中的等物質發生化學反應的結果。
(3)為防止鐵生銹,可對鐵制品進行“發藍”處理,使其表面生成致密氧化物(其中Fe、O元素質量比為21:8)保護膜,該氧化物的化學式為。
Ⅱ.廢鐵的再利用
硫酸鐵在農業可用作肥料,是花木、果樹制造葉綠素的催化劑。用廢鐵屑(主要成分為Fe,含少量Fe2O3和FeCO3)制備硫酸鐵的主要流程如下:
已知:FeCO3+H2SO4═FeSO4+H2O+CO2↑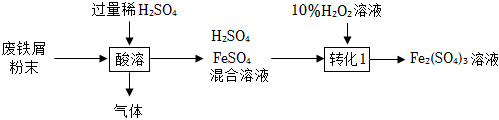
(4)酸溶時生成的氣體成分為。
(5)“轉化1”溫度不宜過高的原因是。
Ⅲ.鐵的冶煉
我國勞動人民在春秋戰國時期就會冶鐵煉鋼,實驗室模擬煉鐵實驗裝置如圖所示。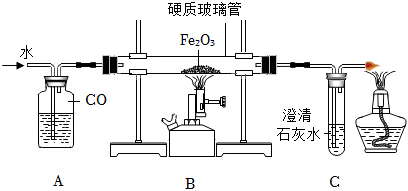
(6)實驗時,應先注水片刻后再加熱的目的是。
(7)實驗過程中,硬質玻璃管中的現象為,發生反應的化學方程式為。組卷:184引用:4難度:0.5 -
28.酸堿中和反應是初中階段重要的一類反應,請你參與一起探究。
【實驗1】從能量變化角度探究酸和堿的反應
某小組同學測量鹽酸與氫氧化鈉溶液反應過程中溫度的變化,觀察到溶液溫度升高,因此,得出兩者能反應的結論。有同學認為此結論不夠嚴謹,在密閉隔熱容器中設計了以下實驗:
①10mL一定濃度的鹽酸與10mL蒸餾水混合,測量溶液溫度的變化。
②10mL一定濃度的氫氧化鈉溶液與10mL蒸餾水混合,測量溶液溫度的變化。
③10mL一定濃度的鹽酸與10mL一定濃度的氫氧化鈉溶液混合,測量溶液溫度的變化。
用數字化實驗技術測得3個實驗中溶液溫度隨時間變化的關系如圖1所示。
(1)由圖1可知,鹽酸、氫氧化鈉溶液稀釋時均(填“放熱”或“吸熱”),但它們稀釋時溫度的變化量遠(填“大于”或“小于”)兩溶液混合時溫度的變化量,由此說明氫氧化鈉和鹽酸發生了反應。
(2)從微觀角度分析,此中和反應的溫度變化主要是由于(填離子符號)兩種離子反應放出熱量的緣故,由此說明氫氧化鈉和鹽酸發生了中和反應。
(3)在10mL溶質質量分數為10%的NaOH溶液(密度為1.1g/mL)中加入溶質質量分數為5%的鹽酸(密度為1.0g/mL)溶液的體積為mL,就能使反應后溶液的pH等于7。(寫出計算過程,結果保留整數)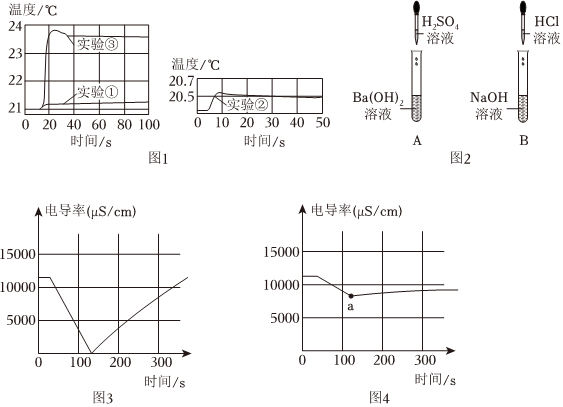
【實驗2】從溶液電導率變化角度探究酸和堿的反應
小組同學根據圖2進行相應實驗操作,利用電導率傳感器分別測定A試管和B試管反應過程中溶液的電導率變化,電導率的大小能反映離子濃度的大小。
(4)根據圖3所示電導率變化,請寫出對應試管中發生反應的化學方程式為。
(5)圖4中電導率的變化(填“能”或“不能”)說明酸和堿發生了反應,a點所示溶液中含有的微粒有(填微粒符號)。組卷:334引用:5難度:0.5


