2021-2022學年廣東省東莞市東華高級中學高一(下)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共16小題,共48分。每小題3分。在每個小題給出的四個選項中,只有一個是符合題目要求的。
-
1.下列說法不正確的是( )
A.凡是放出熱量的化學反應均可用來造福人類 B.目前,全球仍處于化石能源時代 C.人體生命活動所需要的能量,是由氧化還原反應提供的 D.當今社會人們所需的能量絕大部分是由化學反應產生的 組卷:12引用:1難度:0.8 -
2.下列說法錯誤的是( )
A.化學反應放熱還是吸熱,取決于生成物具有的總能量和反應物具有的總能量的相對大小 B.化學鍵的斷裂和形成是化學反應中能量變化的主要原因 C.需要加熱才能發生的化學反應一定是吸熱反應 D.反應物的總能量高于生成物的總能量時,發生放熱反應 組卷:9引用:1難度:0.7 -
3.下列有關化學用語表示不正確的是( )
A.氯離子的結構示意圖: 
B.質子數為6、中子數為8的核素: C146C.CH4的分子結構模型: 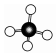
D.CO2的電子式: 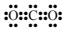 組卷:14引用:2難度:0.7
組卷:14引用:2難度:0.7 -
4.下列變化中屬于原電池反應的是( )
A.鐵銹可用稀鹽酸洗去 B.在空氣中金屬鋁表面迅速被氧化形成保護膜 C.在Fe與稀H2SO4反應時,加幾滴CuSO4溶液,可加快反應速率 D.紅熱的鐵絲與水接觸表面形成藍黑色保護層 組卷:11引用:2難度:0.9 -
5.在一定溫度下的恒容密閉容器中,加入少量A發生反應:A(s)?B(g)+2C(g)。當下列物理量不再發生變化,可以判斷該反應達到化學平衡狀態的是( )
①B的體積分數
②混合氣體的壓強
③混合氣體的總質量
④混合氣體的平均相對分子質量A.①②③ B.②③ C.①④ D.①②③④ 組卷:72引用:5難度:0.7 -
6.頁巖氣是指賦存于富有機質泥頁巖及其夾層中,以吸附和游離狀態為主要存在方式的非常規天然氣,成分以甲烷為主,是一種清潔、高效的能源資源和化工原料。世界能源研究所的最新研究表明,中國頁巖氣儲量高達30萬億立方米以上,居世界第一,幾乎是美國的兩倍。下列關于頁巖氣主要成分甲烷的描述不正確的是( )
A.甲烷完全燃燒只生成CO2和H2O,可推測出甲烷僅由碳、氫兩種元素組成 B.甲烷分子中,碳元素的質量分數為75% C.甲烷分子和氨氣分子所含的電子總數相等 D.鑒別H2、CO和CH4三種無色氣體的方法是比較三種氣體燃燒后的產物 組卷:74引用:1難度:0.8 -
7.金屬鎂和鋁設計成如圖所示的原電池。下列說法正確的是( )
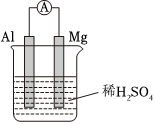
A.鋁作該原電池的負極 B.溶液中 向Al極移動SO2-4C.Mg電極的電極反應式為2H+-2e-═H2↑ D.電流方向為Al→A→Mg 組卷:29引用:3難度:0.4
二、非選擇題:本題共5小題,共52分。
-
20.將氣體A、B置于固定容積為2L的密閉容器中,發生如下反應:3A(g)+B(g)?2C(g)+2D(g),反應進行到10s末,達到平衡,測得A的物質的量為1.8mol,B的物質的量為0.6mol,C的物質的量為0.8mol。
(1)用C表示10s內反應的平均反應速率為。
(2)反應前A的物質的量濃度是。
(3)10s末,生成物D的濃度為。
(4)A與B的平衡轉化率之比為。
(5)平衡后,若改變下列條件,生成D的速率如何變化(填“增大”、“減小”或“不變”):降低溫度;增大A的濃度;恒容下充入氖氣。組卷:26引用:3難度:0.7 -
21.根據要求,回答下列問題:
Ⅰ.把化學能轉化為電能的裝置叫做原電池。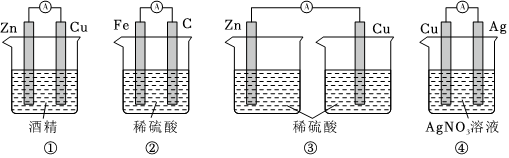
(1)裝置①、②、③中,能組成原電池的是裝置。
(2)裝置④中,正極材料是;負極的電極反應式為;電池工作時,總反應的離子方程式為;燒杯中向NO-3電極移動(填“Cu”或“Ag”);導線中電子的流動方向為(填“Cu到Ag”或“Ag到Cu”)。
Ⅱ.某同學利用鐵與鹽酸的反應,探究影響反應速率的因素(實驗所用鐵的質量相等且鐵塊的形狀相同,鹽酸均過量),實驗設計如下:
(1)若四組實驗均以收集到448mL(標準狀況)氫氣為標準,則上述實驗中還需要測定的數據是實驗編號 鹽酸濃度/(mol?L-1) 鐵的狀態 溫度/K 1 2.00 塊狀 293 2 4.00 塊狀 293 3 4.00 粉末 293 4 4.00 塊狀 313 。
(2)實驗1和2是探究對該反應速率的影響。實驗和是探究溫度對該反應速率的影響。
(3)不同時間t產生的氫氣體積V如圖甲所示,曲線c對應的實驗編號是。每一組實驗中產生氫氣的速率v隨時間t變化的曲線如圖乙所示,其中t1~t2速率變化的主要原因是。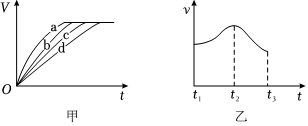
(4)若上述實驗所用鹽酸的體積均為250mL,實驗3反應進行到2min時收集到448mL(標準狀況)氫氣,反應后溶液體積不變,則該條件下,該時間段內,以鹽酸的濃度變化表示的平均反應速率v(HCl)=。組卷:28引用:2難度:0.6


