2022-2023學年新疆烏魯木齊101中高一(上)月考化學試卷(12月份)
發布:2024/10/12 2:0:2
一、選擇題題(20題每題2分共40分)
-
1.潮濕的氯氣、新制的氯水、次氯酸鈉及漂粉精的水溶液均能使有色布條褪色,因為它們均含有微粒( )
A.Cl2 B.HClO C.HCl D.H2O 組卷:131引用:4難度:0.9 -
2.下列實驗操作中,正確的是( )
A.鈉要保存在煤油中,實驗時剩余的鈉要放到廢液缸中 B.鎂等活潑金屬燃燒時,可用含CO2的干粉滅火器滅火 C.H2還原CuO實驗,結束時要先停止加熱,后停止通H2 D.酒精燈使用完畢,可直接吹滅 組卷:10引用:3難度:0.5 -
3.下列有關Fe3+、Fe2+的性質及應用的說法正確的是( )
①向盛有FeCl3溶液的試管中加過量鐵粉,充分振蕩后加1滴KSCN溶液,黃色逐漸消失,加KSCN后溶液顏色不變
②將廢鐵屑加入FeCl2溶液中,可用于除去工業廢氣中的Cl2
③向FeCl2溶液中滴加NH4SCN溶液,溶液顯紅色
④將NaOH濃溶液滴加到飽和FeCl3溶液中制備Fe(OH)3膠體
⑤向Fe2(SO4)3溶液中加入過量鐵粉的離子方程式:Fe3++Fe=2Fe2+
⑥Fe2+與H2O2在酸性溶液中的反應:2Fe2++H2O2+2H+=2Fe3++2H2OA.①②⑥ B.①②③ C.①④⑤ D.②④⑥ 組卷:551引用:8難度:0.7 -
4.有關化學鍵和晶體的說法正確的是( )
A.干冰是共價分子,其升華破壞了共價鍵 B.氯化銨屬于離子化合物,其加熱僅破壞了共價鍵 C.汞是金屬晶體,其氣化破壞了共價鍵 D.二氧化硅屬于共價化合物,其熔化破壞了共價鍵 組卷:60引用:3難度:0.8 -
5.下列有關鐵及其化合物的敘述中,不正確的是( )
A.高溫下,鐵和水蒸氣反應可以生成氫氣 B.將飽和氯化鐵溶液滴入沸水中,煮沸至紅褐色,可以制得氫氧化鐵膠體 C.Fe3O4常用作紅色油漆和涂料 D.用KSCN溶液鑒別FeCl2溶液和Fe2(SO4)3溶液 組卷:536引用:7難度:0.5 -
6.設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.1mol單質Fe與足量的高溫水蒸氣反應,失去3NA個電子 B.標準狀況下,2.24L NO與1.12L O2混合后氣體分子總數為0.1NA C.0.1mol/L的CH3COONa溶液中所含碳原子總數為0.2NA D.標準狀況下,H2和CO混合氣體4.48L在足量O2中充分燃燒消耗O2分子數為0.1NA 組卷:30引用:3難度:0.6 -
7.NA為阿伏加德羅常數的值,下列說法正確的是( )
A.0.1mol的11B中,含有0.6NA個中子 B.100mL0.1mol?L-1的NaOH水溶液中含有氧原子數為0.01NA C.18gD2O中含有的質子數為10NA D.23gNa與足量H2O反應生成的H2分子數為NA 組卷:40引用:4難度:0.5 -
8.超重水(3H2O)是生化實驗的重要原料,下列說法不正確的是( )
A.1H2與2H2互為同位素 B.1H、2H、3H是不同的核素 C.氚(3H)原子核外有1個電子 D.1H218O與2H216O的相對分子質量相同 組卷:21引用:4難度:0.7
三、實驗題(共22分)
-
23.某小組同學探究不同條件下氯氣與二價錳化合物的反應
資料:i.Mn2+在一定條件下被Cl2或ClO-氧化成MnO2(棕黑色)、(綠色)、MnO2-4(紫色)。MnO-4
ii.濃堿條件下,可被OH-還原為MnO-4。MnO2-4
iii.Cl2的氧化性與溶液的酸堿性無關,NaClO的氧化性隨堿性增強而減弱。
實驗裝置如圖(夾持裝置略)
(1)B中試劑是序號 物質a C中實驗現象 通入Cl2前 通入Cl2后 Ⅰ 水 得到無色溶液 產生棕黑色沉淀,且放置后不發生變化 Ⅱ 5%NaOH溶液 產生白色沉淀,在空氣中緩慢變成棕黑色沉淀 棕黑色沉淀增多,放置后溶液變為紫色,仍有沉淀 Ⅲ 40%NaOH 溶液 產生白色沉淀,在空氣中緩慢變成棕黑色沉淀 棕黑色沉淀增多,放置后溶液變為紫色,仍有沉淀 。
(2)通入Cl2前,Ⅱ、Ⅲ中沉淀由白色變為黑色的化學方程式為。
(3)對比實驗Ⅰ、Ⅱ通入Cl2后的實驗現象,對于二價錳化合物還原性的認識是。
(4)根據資料ii,Ⅲ中應得到綠色溶液,實驗中得到紫色溶液,分析現象與資料不符的原因:
原因一:可能是通入Cl2導致溶液的堿性減弱。
原因二:可能是氧化劑過量,氧化劑將氧化為MnO2-4。MnO-4
①化學方程式表示可能導致溶液堿性減弱的原因,但通過實驗測定溶液的堿性變化很小。
②取Ⅲ中放置后的1mL懸濁液,加入4mL40%NaOH溶液,溶液紫色迅速變為綠色,且綠色緩慢加深。溶液紫色變為綠色的離子方程式為,溶液綠色緩慢加深,原因是MnO2被(填“化學式”)氧化,可證明Ⅲ的懸濁液中氧化劑過量;
③取Ⅱ中放置后的1mL懸濁液,加入4mL水,溶液紫色緩慢加深,發生的反應是。
④從反應速率的角度,分析實驗Ⅲ未得到綠色溶液的可能原因。組卷:31引用:3難度:0.7
四、元素或物質推斷題(共24分)
-
24.X、Y、Z、W、Q是元素周期表中原子序數依次增大的五種短周期主族元素,信息如下表。
(1)元素Y在元素周期表中的位置是元素編號 元素性質與原子結構 X 最外層電子數是內層電子數的2倍 Y 其單質與氫氣在暗處能劇烈化合并發生爆炸 Z 短周期元素中原子半徑最大 W 其氧化物是兩性氧化物 Q 同周期元素中,最高價氧化物對應水化物的酸性最強 。
(2)Z在氧氣中完全燃燒所得產物的電子式為。
(3)Y、W、Q的簡單離子半徑由大到小的順序是(用離子符號表示)。
(4)某同學為了比較X元素和硅元素非金屬性的相對強弱,用如圖所示裝置進行實驗。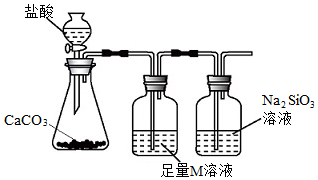
已知:H2SiO3是一種難溶于水的白色物質。
①M為(填化學式),其作用是。
②能說明X元素的非金屬性比硅元素強的實驗現象是。
(5)元素Z與W相比,金屬性較弱的是(填元素名稱),請寫出能證明這一結論的實驗事實(列舉一條)。組卷:28引用:3難度:0.7


