2014-2015學年四川省成都市實驗外國語學校(西區(qū))高三(上)周考化學試卷(1)
發(fā)布:2024/4/20 14:35:0
一、選擇題(本題包括7小題,共42分,每小題6分,每小題只有一個正確選項)
-
1.氮氧化鋁(AlON)是一種透明高硬度防彈材料,可以由反應Al2O3+C+N2
2AlON+CO合成,下列有關說法正確的是( )高溫A.氮氧化鋁中氮的化合價是-3 B.反應中氮氣作氧化劑 C.反應中每生成5.7g AlON 同時生成1.12 L CO D.反應中氧化產(chǎn)物和還原產(chǎn)物的物質(zhì)的量之比是2:1 組卷:15引用:7難度:0.9 -
2.設NA代表阿伏加德羅常數(shù),下列敘述正確的是( )
A.標準狀況下,11.2L的O2和NO的混合物含有的分子數(shù)約為0.5×6.02×1023 B.1mol的羥基與1 mol的氫氧根離子所含電子數(shù)均為9 NA C.常溫常壓下42g 乙烯和丁烯混合氣體中,極性鍵數(shù)為6NA D.6.4g SO2與足量氧氣反應生成SO3,轉(zhuǎn)移電子數(shù)為0.2NA 組卷:57引用:5難度:0.5 -
3.僅用下表提供的玻璃儀器(非玻璃儀器和藥品任選),能實現(xiàn)相應實驗目的是( )
選項 實驗目的 玻璃儀器 A 驗證Na2CO3和NaHCO3的熱穩(wěn)定性 酒精燈、試管、導氣管 B 實驗室用濃氨水和生石灰制備氨氣 普通漏斗、燒杯、玻璃棒 C 測定NaOH溶液濃度 滴定管、錐形瓶、燒杯 D 分離乙醇和乙酸乙酯的混合物 分液漏斗、燒杯 A.A B.B C.C D.D 組卷:158引用:20難度:0.9
二、非選擇題(本題包括4小題,共58分)
-
10.硫化堿法是工業(yè)上制備Na2S2O3的方法之一,反應原理為:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2(該反應ΔH>0)
某研究小組在實驗室用硫化堿法制備Na2S2O3?5H2O流程如下.
(1)吸硫裝置如圖所示.
①裝置B的作用是檢驗裝置A中SO2的吸收效率,B中試劑是,表明SO2吸收效率低的實驗現(xiàn)象是B中.
②為了使SO2盡可能吸收完全,在不改變A中溶液濃度、體積的條件下,除了及時攪拌反應物外,還可采取的合理措施是、.(寫出兩條)
(2)假設本實驗所用的Na2CO3含少量NaCl、NaOH,設計實驗方案進行檢驗.(室溫時CaCO3飽和溶液的pH=10.2)
限選試劑及儀器:稀硝酸、AgNO3溶液、CaCl2溶液、Ca(NO3)2溶液、酚酞溶液、蒸餾水、pH計、燒杯、試管、滴管
(3)Na2S2O3溶液是定量實驗中的常用試劑,測定其濃度的過程如下:準確稱取a g KIO3(化學式量:214)固體配成溶液,加入過量KI固體和H2SO4溶液,滴加指示劑,用Na2S2O3溶液滴定至終點,消耗Na2S2O3溶液的體積為V mL.則c(Na2S2O3)=序號 實驗操作 預期現(xiàn)象 結論 ① 取少量樣品于試管中,加入適量蒸餾水,充分振蕩溶解, .樣品含NaCl ② 另取少量樣品于燒杯中,加入適量蒸餾水,充分攪拌溶解, .樣品含NaOH mol?L-1.(只列出算式,不作運算)
已知:Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O 2S2O32-+I2═S4O62-+2I-.組卷:142引用:7難度:0.5 -
11.聚合硫酸鐵又稱聚鐵,化學式為[Fe2(OH)n(SO4)3-0.5n]m,廣泛用于污水處理。實驗室利用硫酸廠燒渣(主要成分為鐵的氧化物及少量FeS、SiO2等)制備聚鐵和綠礬(FeSO4?7H2O),過程如圖1:
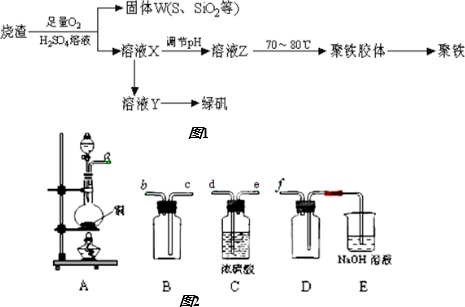
(1)驗證固體W焙燒后產(chǎn)生的氣體含有SO2的方法是:。
(2)實驗室制備、收集干燥的SO2,所需儀器如圖2.裝置A產(chǎn)生SO2,按氣流方向連接各儀器接口,順序為a→→→→→f.裝置A中發(fā)生反應的化學方程式為。
(3)制備綠礬時,向溶液X中加入過量,充分反應后,經(jīng)過濾操作得到溶液Y,再經(jīng)濃縮、結晶等步驟得到綠礬。過濾所需的玻璃儀器有。
(4)欲測定溶液Y中Fe2+的濃度,需要用容量瓶配制KMnO4標準溶液,用KMnO4標準溶液滴定時應選用滴定管(填“酸式”或“堿式”)。
(5)溶液Z的pH影響聚鐵中鐵的質(zhì)量分數(shù)。若溶液Z的pH偏小,將導致聚鐵中鐵的質(zhì)量分數(shù)(填“偏大”、“偏小”或“無影響”)。組卷:307引用:11難度:0.5


