當前位置:
章節挑題
請展開查看知識點列表
>
更多>>
 已完結
已完結
|
期末復習
典型試卷
考前必刷
瀏覽次數:1661
更新:2025年06月03日
|
 已完結
已完結
|
熱點預測
高考復習
難題搶練
瀏覽次數:1431
更新:2025年05月26日
|
271.金屬冶煉一般有下列四種方法:①焦炭法 ②水煤氣(或H2、CO)法 ③活潑金屬置換法④電解法.這四種方法在工業上均有應用.古代有:(Ⅰ)火燒孔雀石煉銅;(Ⅱ)濕法煉銅.現代有:(Ⅲ)鋁熱法煉鉻;(Ⅳ)從光鹵石中煉鎂.對它們的冶煉方法的分析,不正確的是( )
A.(Ⅰ),① B.(Ⅱ),② C.(Ⅲ),③ D.(Ⅳ),④ 發布:2024/5/23 20:38:36組卷:67引用:13難度:0.9272.某化學興趣探究小組將一批廢棄的線路板簡單處理后,得到含Cu(70%)、Al(25%)、Fe(4%)及少量Au等金屬的混合物,并設計出如下制備硫酸銅和硫酸鋁晶體的流程:
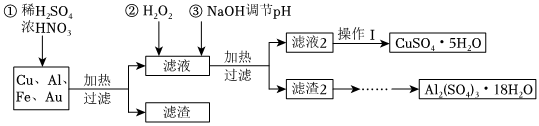
已知:Fe3+、Al3+、Cu2+開始沉淀至沉淀完全的pH范圍分別為:2.2~3.2、4.1~5.0、5.3~6.6.
(1)得到濾渣1的主要成分為.
(2)操作Ⅰ包含的實驗步驟有:、冷卻結晶、過濾、洗滌、干燥;過濾操作所用到的玻璃儀器有燒杯、玻璃棒和.
(3)操作Ⅰ中常用無水乙醇對晶體進行洗滌,選用無水乙醇的原因是.
(4)第②步加H2O2后發生反應的離子方程式為.
(5)取上述硫酸鋁晶體進行熱重分析,其熱分解主要分為三個階段:323K~523K,553K~687K,當溫度在1 043K以上不再失重,下表列出了不同溫度下的失重率:
[硫酸鋁晶體化學式為Al2(SO4)3?18H2O,相對分子質量為666]
已知:失重%=×100%.加熱減少的質量原晶體樣品的總質量
通過計算確定(寫出計算過程):溫度(K) 失重(%) 第一階段 323~523 40.54 第二階段 553~687 48.65 第三階段 1 043以上 84.68
①失重第一階段分解產物的化學式;
②失重第二階段反應的反應化學方程式.發布:2024/5/23 20:38:36組卷:38引用:3難度:0.5273.從海水中提取溴的工業流程如圖
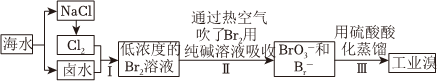
(1)以上步驟Ⅰ中已獲得游離態的溴,步驟Ⅱ又將之轉變成化合態的溴,其目的是。
(2)實驗室保存液溴時,通常在盛液溴的試劑瓶中加少量的水,這與液溴的(填字母)有關。
A.氧化性
B.還原性
C.揮發性
D.腐蝕性
E.密度比水大
(3)流程Ⅱ中將吹出的溴蒸氣用純堿溶液吸收時還有CO2生成,寫出吸收時發生反應的離子方程式:。
(4)實驗室分離溴水中的溴還可以用溶劑萃取法,下列可以用作溴的萃取劑的是。(填字母)
A.四氯化碳
B.乙醇
C.燒堿溶液
D.苯發布:2024/5/23 20:38:36組卷:38引用:3難度:0.5274.鑒別CH4、CO、H2三種無色氣體的方法是( )
A.點燃→通入澄清石灰水→加入溴的四氯化碳溶液 B.點燃→罩上小燒杯→加入澄清石灰水 C.點燃→通入澄清石灰水 D.點燃→通入酸性KMnO4溶液 發布:2024/5/23 20:38:36組卷:18引用:3難度:0.9275.一定條件下,物質A、B、C、D的轉化關系如圖所示:A
BDCD
(1)若A極易溶于水,且水溶液顯堿性,寫出A的兩種用途、;寫出A在催化劑作用下轉化為化合物B的化學方程式。
(2)若A為淡黃色固體單質,將C溶于水配制成18mol?L-1的濃溶液。取100mL該溶液加入過量的銅片,加熱使之充分反應,當參加反應的銅片質量為38.4g時,轉移電子的物質的量為mol,生成的氣體在標準狀況下的體積為L。發布:2024/5/23 20:38:36組卷:10引用:2難度:0.4276.“綠水青山就是金山銀山”。近年來,綠色發展、生態保護成為中國展示給世界的一張新“名片”。
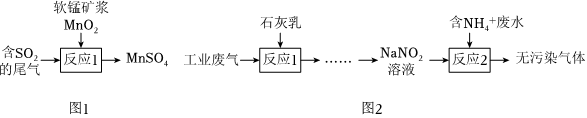
(1)硫酸工業排出的尾氣(主要含SO2)有多種處理方式。
①寫出用過量氨水吸收尾氣的離子方程式:。
②尾氣也可用軟錳礦漿(MnO2)吸收,寫出圖1所示“反應1”的化學方程式:。
(2)治理汽車尾氣中NO和CO的方法之一是在汽車的排氣管上裝一個催化轉化裝置,使NO和CO在催化劑作用下轉化為無毒物質。寫出該反應的化學方程式:。
(3)某工廠擬綜合處理含廢水和工業廢氣(主要含N2、Cl2、NO),設計了如圖2流程:NH+4
①“反應1”用于吸收Cl2,“反應1”的化學方程式為。
②“反應2”的離子方程式為。發布:2024/5/23 20:38:36組卷:125引用:7難度:0.6277.生活處處有化學,下列說法正確的是( )
A.食品中的淀粉和纖維素的組成都可用(C6H10O5)n表示,它們互為同分異構體 B.棉、麻、絲、毛的燃燒產物都只有CO2和H2O C.在紫外線、飽和CuSO4溶液、福爾馬林等作用下,蛋白質均會發生變性 D.煎炸食物的花生油和牛油都是可皂化的飽和酯類 發布:2024/5/23 20:38:36組卷:132引用:3難度:0.5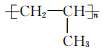 278.某高分子化合物的結構簡式如圖。下列敘述錯誤的是( )
278.某高分子化合物的結構簡式如圖。下列敘述錯誤的是( )A.聚合度為n B.單體為CH2=CHCH3 C.鏈節為-CH2-CH-CH3- D.該高分子化合物是混合物 發布:2024/5/23 20:38:36組卷:52引用:4難度:0.8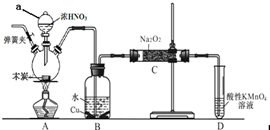 279.亞硝酸鈉在漂白、電鍍等方面應用廣泛.現以木炭、濃硝酸、水和銅為原料生成的一氧化氮與過氧化鈉反應制備亞硝酸鈉的裝置如下圖所示(部分夾持裝置略).
279.亞硝酸鈉在漂白、電鍍等方面應用廣泛.現以木炭、濃硝酸、水和銅為原料生成的一氧化氮與過氧化鈉反應制備亞硝酸鈉的裝置如下圖所示(部分夾持裝置略).
已知:
①3NaNO2+3HCl═3NaCl+HNO3+2NO↑+H2O
②酸性條件下,NO或NO2-都能與MnO4-反應生成NO3-和Mn2+;
完成下列填空:
(1)寫出a儀器的名稱.
(2)為避免B中逸出的氣體中混有的雜質氣體與Na2O2反應,應在B、C裝置間增加一個裝置,則該裝置中盛放的藥品名稱為.
(3)寫出NO與Na2O2在常溫下生成NaNO2的化學反應方程式;當該反應中轉移0.1mole-時,理論上吸收標準狀況下NO的體積為L.
(4)D裝置中發生反應的離子方程式為.
(5)將11.7g過氧化鈉完全轉化成為亞硝酸鈉,理論上至少需要木炭g.發布:2024/5/23 20:38:36組卷:33引用:2難度:0.9280.現有6瓶失去標簽的液體,已知它們可能是乙醇、乙酸、苯、乙酸乙酯、油脂、葡萄糖中的一種.現通過如下實驗來確定各試劑瓶中所裝液體的名稱:
(1)寫出這6種物質的名稱.實驗步驟和方法 實驗現象 ①把6瓶液體分別依次標號A、B、C、D、E、F,然后聞氣味 只有F沒有氣味 ②各取少量于試管中,加水稀釋 只有C、D、E不溶解而浮在水面上 ③分別取少量6種液體于試管中,加新制Cu(OH)2并加熱 只有B使沉淀溶解,F中產生磚紅色沉淀 ④各取C、D、E少量于試管中,加稀NaOH溶液并加熱 只有C仍有分層現象,且在D的試管中聞到特殊香味
A,B,C,D,
E,F.
(2)在D中加入NaOH溶液并加熱的化學方程式為.
(3)已知乙醛發生銀鏡反,試寫出葡萄糖發生銀鏡反應的化學方程式.發布:2024/5/23 20:38:36組卷:14引用:3難度:0.1



