2020年浙江省嘉興市嘉善縣中考化學模擬試卷(5月份)
發布:2025/6/29 7:0:8
一、選擇題(共5小題,每小題3分,滿分15分)
-
1.下列四個圖形屬于符號的是( )
A. 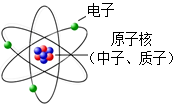
原子結構B. 
節水標志C. 
甲烷分子結構D. 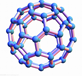
足球烯結構組卷:46引用:4難度:0.9 -
2.下列除雜質所選用試劑正確的是( )
A.用稀鹽酸除去銅粉中的鐵粉 B.用濃硫酸吸收O2中的CO2氣體 C.用適量稀硫酸除去NaCl溶液中的Na2CO3 D.用稀鹽酸除去Fe2O3中的CaCO3 組卷:387引用:6難度:0.5 -
3.下列有關實驗現象的說法不正確的是( )
A.加熱銅綠時,綠色固體會變成黑色固體 B.鎂條燃燒時,產生耀眼的白光,同時生成一種白色的粉末狀物質 C.加熱碳酸氫銨時,產生有刺激性氣味的氣體 D.鐵絲生銹后產生一種物質是氧化鐵 組卷:4引用:1難度:0.6 -
4.下列圖像與其對應描述相符的是( )
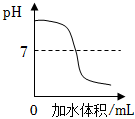
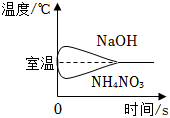
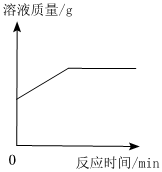
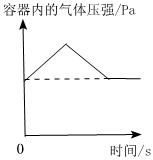
A.氫氧化鈉溶液加水稀釋 B.把NaOH和NH4NO3固體分別溶于水 C.向一定量的硝酸銀溶液中插入銅 D.紅磷在盛有一定量空氣的密閉容器中燃燒至熄滅 A.A B.B C.C D.D 組卷:128引用:2難度:0.7 -
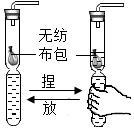 5.小明同學用軟塑料瓶自制氣體了一套發生裝置(如圖所示),下列關于該裝置的說法不正確的是( )
5.小明同學用軟塑料瓶自制氣體了一套發生裝置(如圖所示),下列關于該裝置的說法不正確的是( )A.通過捏放瓶身可隨時控制反應的發生和停止 B.若無紡布包內藥品為大理石,利用該裝置可制二氧化碳 C.利用該裝置制氧氣,液體試劑為雙氧水 D.利用該裝置制氧氣,無紡布包內二氧化錳越多,生成氧氣就越多 組卷:478引用:6難度:0.7
二、解答題(共6小題,滿分0分)
-
 6.嫦娥四號探測器用表面鍍金的鉬絲做金屬網。
6.嫦娥四號探測器用表面鍍金的鉬絲做金屬網。
(1)鉬能制成細絲,是利用了鉬的性。
(2)鉬絲表面鍍金,原因之一是利用了金的化學性質。
(3)我國的鉬礦儲量非常豐富,用輝礦(MoS2)制備鉬的過程如下:
MoS2MoO3Ⅰ高溫MoⅡ氫氣、高溫
①過程1中反應的化學方程式:2MoS2+7O22MoO3+4高溫。
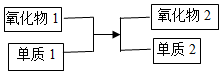
②過程Ⅱ分兩個階段:第一階段反應為:MoO3+H2H2O+MoO2.第二階段過程如圖。寫出第二階段反應化學方程式:高溫。組卷:40引用:2難度:0.7 -
7.閱讀材料,回答問題。
出現新冠病毒以來,過氧乙酸作為高效消毒劑而被廣泛使用。過氧乙酸(化學式為CH3COOOH)在常溫下是一種無色有刺激性氣味的液體,易揮發。它對呼吸道黏膜有刺激性,高含量的過氧乙酸溶液對皮膚有腐蝕性。商品過氧乙酸是40%的醋酸溶液,使用前通常先用蒸餾水等將其稀釋,消毒時可用噴霧法消毒,也可將其配制成0.2%的水溶液洗手消毒。過氧乙酸不穩定,易分解生成無毒物質,若用噴霧法消毒,過氧乙酸在半小時內就可完全分解。
(1)過氧乙酸是(填“無機化合物”或“有機物”)。
(2)在過氧乙酸溶液中,溶劑是(寫化學式)。
(3)分別指出過氧乙酸的物理性質和化學性質(各寫一點即可)。
物理性質:,化學性質:。
(4)100g溶質質量分數為0.2%的過氧乙酸洗手液中,含過氧乙酸g。
(5)在稀釋40%的醋酸溶液時應注意的是。組卷:10引用:2難度:0.6 -
 8.感悟衣食住行中的化學魅力“慈母手中線,游子身上衣”現在的衣服不僅僅有保暖作用,還有裝飾美體的功能。
8.感悟衣食住行中的化學魅力“慈母手中線,游子身上衣”現在的衣服不僅僅有保暖作用,還有裝飾美體的功能。
(1)這件大衣中的粘纖屬于人造纖維,屬于合成纖維的是(選填“羊毛”或“聚酯纖維”)。羊毛的主要成分是。
(2)如果衣服染上油漬,干洗店用干洗劑四氯乙烯除去油污的原理是。(選填“乳化”或溶解”)組卷:24引用:1難度:0.7 -
9.已知碘元素符號為I,它的原子結構示意圖如圖2所示:
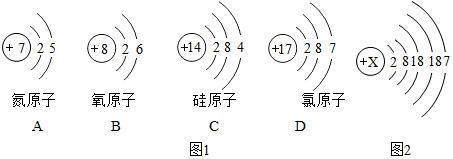
(1)x值=。
(2)碘元素的化學性質與下列哪元素的化學性質最相似?如圖1答:
已知F、Cl、I元素等都落在元素周期表中的同一個族中,由“我國人民分成56個民族”這句話得到啟示,我們能推斷它們歸為同族的依據是。
(3)在食鹽中適量加入一種含碘的化合物(其化學式為KIO3),可以有效地防治碘缺乏病。請模仿用來制取氧氣的KClO3的命名方法,說出KIO3的名稱。答:。組卷:10引用:1難度:0.1 -
10.氧氣是人類活動所必需的自然資源。實驗室常用物質分解的方法制取氧氣。
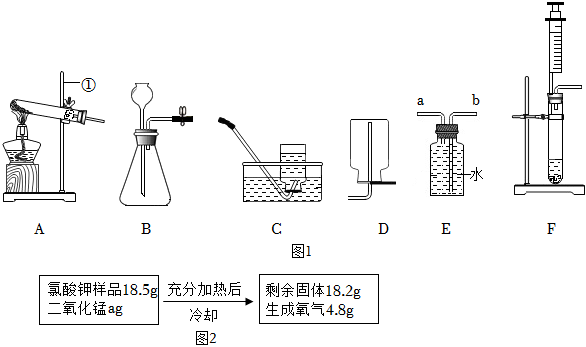
(1)圖1中儀器①的名稱是。
(2)實驗室用高錳酸鉀制取并收集氧氣,可選擇(填字母)裝置,此法制取氧氣的化學方程式為。
(3)檢查B裝置氣密性的方法是(可借助水和圖中的其他裝置)。
(4)如果用E裝置收集氧氣,氣體應從管(填“a”或“b”)進入。
(5)某同學認為可用F裝置可以代替B裝置,與B相比,F裝置的優點是。
(6)實驗室有一瓶含雜質的氯酸鉀(雜質不參加反應)。某同學加熱該氯酸鉀來制氧氣,實驗數據記錄如圖2,請回答下列問題:
①a=。
②計算受熱分解的氯酸鉀的質量。組卷:1引用:2難度:0.6 -
11.計算通電分解36g水可得到多少g氫氣?
(1)上面是四位同學的解題過程,其中有兩位同學的解法是正確的,他們是甲同學
解:設可得氫氣質量為X.
2H2O2H2↑+O2↑通電
20 4
36g x=204x=7.2g36gx
答:可得到7.2g氫氣.乙同學
解:設可得氫氣質量為X
H2OH2↑+O2↑通電
18 2
36g x=182x=4g36x
答:可得到4g氫氣.丙同學
解:水中氫元素的質量分數
=×100%氫的相對原子質量×2水的相對原子質量
=×100%1×21×2+16×1
≈11.1%
氫氣的質量為36×11.1%=4.0g
答:可得到4.0g氧氣.丁同學
解:設可得氫氣質量為X
2H2O2H2↑+O2↑通電
36 4
36g x=364x=4g36gx
答:可得到4g氫氣;另外兩位的錯誤,請擇其一說明錯誤原因是.
(2)請根據化學方程式計算加熱31.6g高錳酸鉀完全分解所產生的氧氣質量是多少?(寫出計算過程)組卷:20引用:1難度:0.3


