2020年河南省信陽市淮濱一中中考化學模擬試卷(3)
發布:2025/6/30 4:0:8
一、單選題(14分)
-
1.元素周期表的發現使化學研究變得有規律可循,研制出第一張元素周期表的科學家是( )
A.門捷列夫 B.道爾頓 C.拉瓦錫 D.阿伏加德羅 組卷:52引用:3難度:0.8 -
2.下列實驗操作能達到相應實驗目的的是( )
實驗目的 實驗操作 A 除去CO2中的少量CO 點燃 B 鑒別CuO粉末和木炭粉 觀察顏色 C 鑒別H2和CH4 分別點燃,在火焰上方罩一干冷燒杯 D 鑒別雙氧水和蒸餾水 取樣,分別加入二氧化錳 A.A B.B C.C D.D 組卷:68引用:4難度:0.5 -
3.工業上將過氧化氫轉化為固態的過碳酸鈉晶體(2Na2CO3?3H2O2),該晶體具有碳酸鈉和過氧化氫的雙重性質。接觸下列物質不會使過碳酸鈉失效的是( )
A.氯化鈉 B.氯化鋇 C.二氧化錳 D.鹽酸 組卷:99引用:3難度:0.5 -
4.令X、Y、Z和R分別代表四種元素.若aXm+、bYn+、cZn-、dRm-四種離子的電子層結構相同(令a、b、c、d分別為四種元素的核電荷數),則下列關系正確的是( )
A.a-c=m-n B.a-b=n-m C.c-d=m+n D.b-d=n+m 組卷:191引用:7難度:0.7 -
5.物質是由微粒構成的,下列物質由原子構成的是( )
A.硅 B.氯化鈉 C.氨氣 D.干冰 組卷:6引用:2難度:0.6 -
6.規范的實驗操作是確保實驗成功的前提。下列實驗操作中正確的是( )
A.稀釋濃硫酸時,將水沿玻璃棒慢慢注入濃硫酸中,并不斷攪拌 B.排水法收集氣體時,當導管口開始有氣泡冒出時,立即收集 C.在實驗室里制取氧氣等氣體時,要檢查裝置的氣密性 D.測定某溶液的pH時,先用水將pH試紙潤濕 組卷:9引用:1難度:0.6 -
7.下列物質中屬于純凈物的是( )
A.澄清石灰水 B.潔凈的空氣 C.液氧 D.醫用酒精 組卷:19引用:1難度:0.5 -
8.分類是學習化學的方法之一,下列各組物質按單質、氧化物、混合物的順序排列的是( )
A.蒸餾水、二氧化碳、空氣 B.氮氣、氯酸鉀、空氣 C.氧氣、氯化鈉溶液、石油 D.氧氣、氧化鈣、海水 組卷:25引用:3難度:0.8 -
9.我國古代的化學工業比較發達,如制造青銅器最早出現的朝代就是( )
A.春秋 B.商代 C.戰國 D.西漢 組卷:5引用:2難度:0.9 -
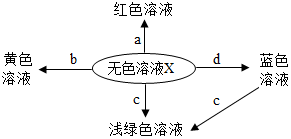 10.如圖表示化學反應中溶液的顏色變化。下列敘述不正確的是( )
10.如圖表示化學反應中溶液的顏色變化。下列敘述不正確的是( )A.若X是稀鹽酸,a可能是紫色石蕊試液 B.若X是稀鹽酸,b可能是氧化物 C.若X是稀硫酸,c不可能是單質 D.若X是稀硫酸,d不一定是堿類物質 組卷:524引用:4難度:0.7 -
11.小明整理的“氧氣”思維導圖中錯誤的是( )
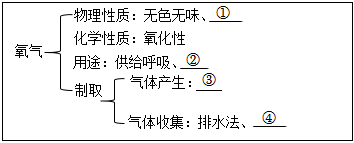
A.①處:“物理性質”中可添加“密度大于空氣” B.②處:“用途”中可添加“燃料” C.③處:“氣體產生”中可添加“氯酸鉀 氯化鉀+氧氣”加熱二氧化錳D.④處:“氣體收集”中可添加“向上排空氣法” 組卷:25引用:2難度:0.6 -
12.下列說法正確的是( )
A.所有的物質都是由分子構成的 B.石墨和金剛石的物理性質不同,是因為碳原子的排列方式不同 C.質子數相同的微粒一定是同一種元素 D.用水銀溫度計測量體溫,說明汞分子間的間隔隨溫度的升高而變大 組卷:19引用:3難度:0.6 -
13.小明想除去白襯衫上的鐵銹痕跡,在用清水洗滌前,他從家中選擇的最合適的物質是( )
A.汽油 B.白醋 C.食鹽水 D.洗衣粉 組卷:35引用:2難度:0.9 -
14.某農場需要購置NH4NO3和CO(NH2)2兩種化肥總重量為100kg,經測得其中含氫元素的質量分數為6%,則其中含氮元素的質量為( )
A.36kg B.40kg C.42kg D.50kg 組卷:626引用:9難度:0.9
二、填空題(16分)
-
15.用化學符號或化學符號中數字的意義填空。
(1)地殼中含量最多的金屬元素與非金屬元素組成的化合物。
(2)Fe2+中“2”的意義是。組卷:8引用:2難度:0.5 -
16.為驗證二氧化碳溶于水是否存在化學變化,小輝取四朵用紫色石蕊溶液染成干燥的紫色紙花,分別按如圖進行實驗.
請根據圖示進行思考并回答下表中的問題:(Ⅰ) (Ⅱ) (Ⅲ) (Ⅳ) 現象 紫色紙花變紅 紫色紙花不變色 紫色紙花不變色 分析 ①實驗(Ⅲ)驗證了 :
實驗(Ⅳ)驗證了;
②通過實驗(Ⅰ)、(Ⅳ),可驗證酸能使;
③通過實驗(Ⅳ)結束后,將紙花用酒精燈小心加熱烘烤后紙花又變紫,說明碳酸.
寫出該反應的化學方程式. 組卷:221引用:4難度:0.5
組卷:221引用:4難度:0.5 -
17.下表是元素周期表的部分內容,請認真分析并回答后面的問題:
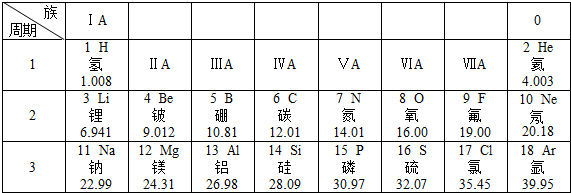
(1)請從上表中查出地殼中含量最多的金屬元素的相對原子質量為.
(2)表中不同種元素最本質的區別是(填序號):
A.相對原子質量不同 B.質子數不同 C.中子數不同
(3)元素周期表中每一個橫行叫做一個周期,通過分析,同一周期元素之間的排列有一定的規律,如:(填字母序號)、…
A從左到右各元素原子的電子層數相同
B從左到右,各元素原子的原子序數依次增加
C從左到右,各元素原子的最外層電子數相同
(4)元素周期表中,原子序數為12的鎂元素的原子結構示意圖如圖 ,該原子在化學反應中易(“得到”“失去”)電子.說明元素的化學性質與原子的關系密切.
,該原子在化學反應中易(“得到”“失去”)電子.說明元素的化學性質與原子的關系密切.
(5)僅含碳和氫兩種元素的有機物稱為烴,如烷烴、烯烴、炔烴等.烷烴中最簡單的是甲烷(CH4),其余隨碳原子數的增加,依次為乙烷(C2H6)、丙烷(C3H8)、丁烷(C4H10)等.如果烷烴中的碳原子數為n,則烷烴的化學式可以用通式表示.它們在氧氣中完全燃燒的產物都是二氧化碳和水,試寫出甲烷在空氣中充分燃燒的化學方程式:.組卷:13引用:1難度:0.3 -
18.“遠在高空是地球衛士,近在身邊是健康殺手。”臭氧(O3)對環境的作用需辯證地認識。臭氧具有極強的氧化性和殺菌性能,臭氧反應后的產物是氧氣。臭氧主要存在于15000-30000米的高空,能減弱高能量紫外線對地球表面的輻射。
(1)臭氧是無污染的氧化劑的理由是。臭氧屬于(填字母)。
A.純凈物
B.混合物
C.氧氣
D.稀有氣體
(2)有人提出:你吸入的空氣中的某個氧原子可能來自于若干年前恐龍的身體。該說法表達的觀點是。(填字母)
A.分子聚集形成物質,分子在不停地運動
B.在化學變化中原子既不會產生,也不會消失
C.原子內部結構復雜,原子不是構成物質的最小微粒
(3)高空中臭氧層能吸收紫外線,有學者認為,致冷劑氟利昂進入高空大氣后會產生氯原子(Cl?),引發以下反應:Cl?+O3═ClO?+O2Ⅰ,2ClO?═2Cl?+O2Ⅱ,Cl?加快了上述轉化過程總反應的速率,但自身的質量和化學性質在總反應前后沒有發生變化,其作用是,該轉化過程總反應的化學方程式。
(4)磷在臭氧中燃燒與在氧氣中燃燒相似,請寫出磷在臭氧中燃燒的化學方程式:。組卷:5引用:1難度:0.6 -
19.1909年,化學家哈伯用氮氣和氫氣在高溫高壓條件下首次合成了氨氣,反應原理為N2+3H2
2NH3.氨氣具有可燃性,燃燒時發熱量高.近年,科學家發現用催化劑在常溫下就能合成氨氣,使其有望成為替代氫能的新一代能源高溫高壓
(1)若用下面三幅模型圖表示合成氨氣的過程. !
!
①則從反應開始到完成的排列順序為(用字母表示).
②分析圖中微觀過程,你能總結出的一條結論是.
(2)氨氣燃燒時可能生成氧化物而污染環境,但在一定條件下,氨氣燃燒卻沒有任何污染,該反應原理是4NH3+3O22N2+6X,其中X的化學式是點燃,請寫出X物質具有的一條物理性質.
(3)如果氨氣不慎泄漏,在關閉閥門和防止明火的前提下,噴灑大量水霧即可.由此可知氨氣可能具有的一條性質是.組卷:12引用:1難度:0.7 -
20.碳中和,中國在行動。由于人類過度開采使用地下碳(主要是煤、石油、天然氣),導致碳排放量急劇增加,打破了大氣中二氧化碳的平衡。為緩解溫室效應,中國將在2060年前實現碳中和。如圖所示是在密閉容器中物質變化過程的微觀示意圖:

(1)A、B、C中表示混合物的是,理由是。
(2)上述變化1、2和3中,屬于化學變化的是(填序號),請寫出其化學反應的文字表達式,該變化前后不變的粒子是(填粒子名稱),由此圖分析可知,化學變化的實質是。
(3)變化2和3分別是二氧化碳的液化和汽化,其中,變化2中微粒之間發生的變化是。
(4)下列有關于二氧化碳的說法,正確的有(填序號)。
A.二氧化碳是由碳和氧氣組成的
B.二氧化碳是由碳原子和氧分子構成的
C.二氧化碳分子是由碳原子和氧分子構成的
D.一個二氧化碳分子是由一個碳原子和兩個氧原子構成的組卷:17引用:1難度:0.5
三、簡答題(10分)
-
 21.在2008年3月24日的北京奧運會圣火采集現場,最高女祭司手中取火用的火炬中,用來充當引火之物的引子是折疊好的電影膠片。而在早期取火儀式中,火炬中填充的是干草。如今之所以偏愛膠片,是因為膠片是以硝酸纖維素為主要成分,比干草更易燃。最高女祭司采集圣火成功之后,首先用手中的火炬引燃了一旁的火種罐,火種罐中盛放的是希臘當地的特產橄欖油。
21.在2008年3月24日的北京奧運會圣火采集現場,最高女祭司手中取火用的火炬中,用來充當引火之物的引子是折疊好的電影膠片。而在早期取火儀式中,火炬中填充的是干草。如今之所以偏愛膠片,是因為膠片是以硝酸纖維素為主要成分,比干草更易燃。最高女祭司采集圣火成功之后,首先用手中的火炬引燃了一旁的火種罐,火種罐中盛放的是希臘當地的特產橄欖油。
試回答下列問題:
(1)根據燃燒的條件,膠片是,用凹面鏡的作用是。
(2)膠片、干草、橄欖油的著火點由高到低的順序是。
(3)硝酸纖維素的化學式為C6H7O2(ONO2)3,它是由種元素組成,每個分子含有個原子。
(4)橄欖油中含有:油酸(單不飽和脂肪酸)70~80%,亞油酸(多不飽和脂肪酸):6~9%,棕櫚酸(飽和脂肪酸):7~15%,另外還含有維生素A和E.油酸的化學式為C18H34O2。
①橄欖油是(選填“純凈物”、“混合物”)。
②油酸完全燃燒的化學方程式是。組卷:7引用:1難度:0.5 -
22.在加熱條件下用鎂消耗從空氣中得到的氮氣(生成物中鎂元素為+2價,氮元素為-3價),最終得到一種少量的密度較大的氣體--氬.
(1)鎂和氮氣反應的化學方程式是.
(2)上述反應中各反應物與生成物之間的質量比是.
(3)已知參加反應的鎂的質量為3.6g,消耗的氮氣體積是L.(在標準狀況下,氮氣的密度為1.25g?L-1)組卷:2引用:3難度:0.3 -
23.生活中處處有化學,請你用所學的化學知識解釋.
(1)新裝修房屋內的空氣中通常含有較多的甲醛(CH2O)、苯(C6H6)等有毒物質.這兩種物質都屬于(填“無機物”或“有機物”).在搬入新裝修房屋之前,可利用“光觸媒”技術--用TiO2在光催化作用下將上述有害物質轉化為二氧化碳和水,降低室內空氣污染.
(2)目前市面上有一種底部有兩層(一層存放水,另一層存放鎂和鐵的混合物)的新型“即熱飯盒”.使用時打開隔離層,即生以下反應:Mg+2H2O═X+H2↑,X的化學式是.
(3)有些食品保鮮劑的主要成分為活性鐵粉,保鮮的原因是,欲檢測一份這樣的保鮮劑是否已經完全失效,所用的試劑是,此反應的方程式為.組卷:5引用:1難度:0.5 -
24.根據電解水實驗裝置圖回答下列問題:

(1)指出電源的正負極:AB;
(2)C試管中為氣,D試管中產生的是氣;C、D兩試管中氣體的體積比為。
(3)寫出該反應的文字表達式,其反應類型為。
(4)該實驗得出的結論是:水是由和組成的。組卷:9引用:2難度:0.5
四、綜合題(10分)
-
 25.電池在我們的生活中應用極為廣泛,2019年諾貝爾化學獎頒發給了在鋰電池研究方面做出貢獻的科學家。
25.電池在我們的生活中應用極為廣泛,2019年諾貝爾化學獎頒發給了在鋰電池研究方面做出貢獻的科學家。
(1)一種鋰電池放電時的反應為8Li+3SOCl2═Li2SO3+6LiCl+2S,此反應中鋰的化合價由變為。
(2)鐵碳電池放電時鐵被腐蝕,其反應為2Fe+O2+2H2O═2Fe(OH)2,4Fe(OH)2+O2+2X═4Fe(OH)3,2Fe(OH)3═Fe2O3+3H2O,則X的化學式為,鐵被腐蝕的條件是。
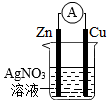
(3)如圖所示將一根鋅棒和一根銅棒放入一定量的硝酸銀溶液中,發生反應,電流表指針發生偏轉。
①反應的化學方程式為。
②溶液質量(填“增加”或“減少”)。
③此裝置將化學反應產生的能量轉化為。
(4)電池的制造離不開金屬,而金屬大都是用礦石冶煉得到的,“火法煉銅”中用輝銅礦(主要成分Cu2S)煉銅的原理是Cu2S與氧氣在高溫條件下反應生成銅和一種會導致酸雨的氣體(其相對分子質量為64)。利用上述方法制得3.2t銅,產生導致酸雨的氣體多少噸?組卷:41引用:2難度:0.5


