2023-2024學年山東省泰安市東平縣九年級(上)期末化學試卷
發布:2025/7/1 2:0:9
一、選擇題(本題包括20小題。每小題2分,共40分。每小題只有一個選項符合題意。)
-
1.光亮的鐵釘在下列情況下最容易生銹的是( )
A. 
B. 
C. 
D.  組卷:10引用:2難度:0.6
組卷:10引用:2難度:0.6 -
2.下列反應能進行的是( )
A.用稀鹽酸除鐵銹生成黃色的溶液 B.氯化銅溶解在硫酸中生成藍色的硫酸銅溶液 C.銅溶解在稀硫酸中生成藍色的硫酸銅 D.鐵溶解在稀鹽酸中生成黃色的氯化鐵 組卷:41引用:4難度:0.7 -
3.鈦(Ti)合金在國防、醫用材料等領域有重要應用。某鈦鐵礦的主要成分為鈦和鐵的含氧化合物,可用于制備金屬鈦。則該鈦鐵礦的主要成分可能為( )
A.FeTiO3 B.TiO2 C.CaTiO3 D.Fe2O3 組卷:41引用:1難度:0.7 -
4.化學與生活息息相關,下列說法不正確的是( )
A.生活中常用煮沸的方法降低水的硬度 B.服用含有氫氧化鋁的藥物,治療胃酸過多癥 C.菠菜中的鐵可以預防貧血 D.霉變大米高溫蒸煮后即可食用 組卷:35引用:2難度:0.8 -
5.炎熱的夏季,將下列物質露置在空氣中一段時間,其中能發生化學變化且質量減少的是( )
A.碳酸氫銨 B.濃鹽酸 C.生石灰 D.氫氧化鈉 組卷:4引用:2難度:0.5 -
6.新農村建設中,許多村莊道路兩側安裝了太陽能路燈。下列關于太陽能路燈所用材料的說法,正確的是( )
A.鋁合金燈柱屬于復合材料 B.電池板中的硅元素是地殼中含量最高的元素 C.鋁合金耐腐蝕性強,燈柱下部分刷漆只是為了美觀 D.透明的塑料燈罩屬于有機合成高分子材料 組卷:39引用:3難度:0.7 -
7.資源、能源利用和環境保護是人類共同關注的問題。下列說法錯誤的是( )
A.使用新型可降解的塑料可減少“白色污染” B.地球上淡水約占全球水儲量的96.5%,所以可利用的淡水資源取之不盡用之不竭 C.廢舊電池回收利用能減少對土壤的污染 D.煤、石油、天然氣是不可再生的化石能源 組卷:8引用:3難度:0.7 -
8.打開汽水瓶蓋,氣體從瓶中逸出的主要原因是( )
A.汽水變成蒸汽揮發出來 B.壓強減小后,使汽水中氣體的溶解度減小而逸出 C.汽水中的水蒸氣揮發出來 D.溫度升高使汽水中的碳酸分解 組卷:57引用:4難度:0.9 -
9.下列混合物,能按“溶解——過濾——蒸發”的步驟加以分離的是( )
A.酒精和水 B.食鹽和沙子 C.鐵和銅 D.廚房中的白糖和食鹽 組卷:15引用:1難度:0.6 -
10.以下不會使蛋白質失去原有生理功能的物質是( )
A.甲醛溶液 B.乙酸鉛溶液 C.飽和硫酸銨溶液 D.濃硝酸 組卷:97引用:5難度:0.7 -
11.2008年北京奧與會“祥云”火炬所使用的燃料由先前的丁烷改為丙烷(化學式為C3H8),下列有關敘述不正確的是( )
A.丙烷屬于有機化合物 B.丙烷燃燒的火焰比丁烷燃燒的火焰更為醒目 C.丙烷完全燃燒的產物為二氧化碳和水 D.丙烷中碳氫元素的質量比為3:8 組卷:4引用:1難度:0.9 -
12.某物質的pH=3,則該溶液( )
A.呈酸性 B.呈堿性 C.呈中性 D.酸堿性無法判斷 組卷:37引用:6難度:0.9 -
13.在給定條件下,下列物質間的轉化能實現的是( )
A.H2O O2點燃B.CuO CuSO4稀硫酸C.Fe FeCl3稀鹽酸D.S SO3O2組卷:15引用:3難度:0.5 -
14.pH試紙能測定溶液的酸堿度,試紙自身顏色為( )
A.黃色 B.白色 C.紫色 D.藍色 組卷:45引用:3難度:0.7 -
15.下列溶液中的離子能大量存在的是( )
A.呈藍色溶液中:Ba2+、OH-、Cl- B.pH=12的溶液中:Mg2+、K+、SO42- C.pH=2的溶液中:K+、CO32-、SO42- D.無色透明的溶液中:Al3+、Cl-、NO3- 組卷:421引用:9難度:0.5 -
16.如圖是元素周期表中鋁元素的某些信息。由該圖不能獲得的信息是( )

A.鋁元素符號是Al B.原子序數是13 C.相對原子質量是26.98 D.地殼中含量最高的金屬元素是鋁 組卷:37引用:2難度:0.6 -
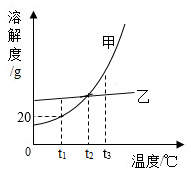 17.如圖是甲、乙兩種固體物質的溶解度曲線,下列說法中正確的是( )
17.如圖是甲、乙兩種固體物質的溶解度曲線,下列說法中正確的是( )A.甲中混有少量乙,可以用蒸發溶劑的方法得到甲 B.把100g溶質質量分數為5%的甲溶液從t2℃降溫到t1℃,其溶質質量分數仍為5% C.甲的溶解能力比乙強 D.t2℃時,將甲、乙溶液恒溫蒸發等質量的水,析出晶體的質量相同 組卷:67引用:2難度:0.5 -
18.某科技團隊設想利用物質溶解時的降溫效果,打造無電力冷卻系統,他們選擇的這種物質可能是( )
A.NH4NO3 B.NaOH C.NaCl D.MnO2 組卷:214引用:6難度:0.7 -
19.下列圖像不能正確反映對應變化關系的是( )
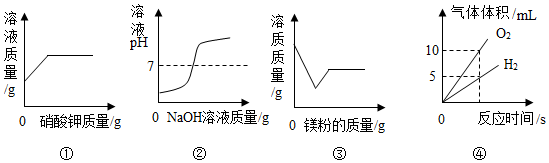
A.①室溫下,向一定量硝酸鉀的不飽和溶液中不斷加入硝酸鉀固體 B.②向一定量的稀鹽酸中不斷加入過量的NaOH溶液 C.③向一定量氯化亞鐵和氯化鋁的混合溶液中不斷加入鎂粉至過量 D.④將一定量的水通電分解一段時間 組卷:199引用:7難度:0.5 -
20.下列有關實驗現象的描述正確的是( )
A.硫在空氣中燃燒產生明亮的藍紫色火焰,放熱,生成有刺激性氣味的氣體 B.汞在空氣中持續加熱會生成紅色粉末 C.氫氧化鈉溶液中滴加硫酸銅溶液出現藍色絮狀沉淀氫氧化銅 D.將火柴梗平放入蠟燭的火焰中,約1秒后取出,火柴梗與內焰接觸部分最先變黑 組卷:4引用:1難度:0.6
二、(本題包括3小題,共26分)
-
21.人類生存和社會發展離不開化學,請用所學的化學知識回答下列問題:
(1)與農家肥相比,化肥有效成分高,見效快,合理使用化肥可在一定程度上促進糧食等農產品增產.硝酸鉀是一種復合肥料,該物質所含酸根離子的符號是.尿素是一種常用的氮肥,化學式是CO(NH2)2,它由種元素組成,其中N元素的質量分數是(精確到0.1%),一個CO(NH2)2分子中含有(四個氫原子)(括號里的字用化學符號表示).
(2)京滬高鐵在軌道系統上創造了多項世界及中國第一.在施工建設中,焊接鐵軌中的縫隙常用點燃鋁和氧化鐵(Fe2O3)混合物的方法,此反應生成氧化鋁和熔融狀態下的鐵,同時放出大量的熱,寫出該反應的化學方程式,反應過程中能轉化為熱能,反應類型為.
(3)服用碘片(有效成分為KI)可以治療I-131造成的輻射,但服用碘酒(有效成分為I2)卻會引起中毒.KI和I2性質不同的原因是.組卷:77引用:2難度:0.5 -
22.我國化學家侯德榜先生創立的聯合制堿法,將堿廠與氨廠聯合,既提高效益又減少污染,促進了世界制堿工業的發展。聯合制堿法的模擬流程如圖一所示。三種鹽的溶解度隨溫度變化的曲線如圖二所示。吸氨碳化塔中溫度控制在30℃-35℃,其中發生的主要反應是:HN3+CO2+H2O+NaCl=NaHCO3+NH4Cl。請回答問題
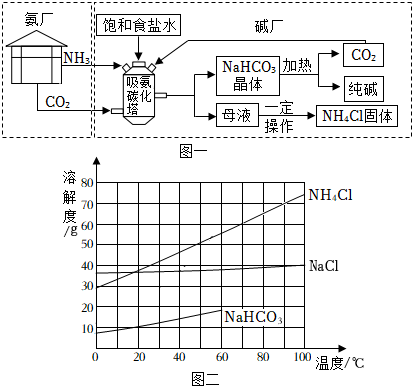
(1)通常狀況下,NH3的溶解度遠大于CO2的溶解度。生產時吸氨碳化塔中應該先通入的是(填“NH3”或“CO2”),這樣操作的目的是。
(2)加熱NaHCO3制得純堿的化學方程式是。
(3)結合圖二分析,吸氨碳化塔中析出NaHCO3固體的主要原因是(填序號)。
①溶劑質量減少;
②NaHCO3難溶于水;
③30℃-35℃時,NaCl、NaHCO3、NH4Cl的溶解度相比較,NaHCO3的溶解度最小,易達到飽和而析出。
(4)圖一“母液”中NaHCO3是否達到飽和。(填“是”“否”)
(5)圖一中循環使用的物質(填化學式),堿廠與氨廠聯合后,得到NH4Cl代替氨水做化肥,其優點是(答一條即可)。組卷:49引用:2難度:0.6 -
23.請根據如圖回答相關問題。
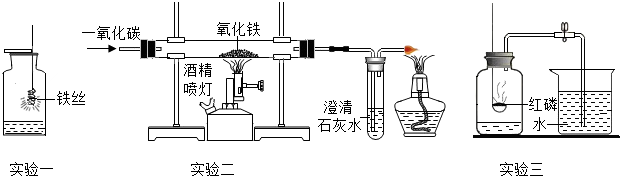
(1)實驗一中,集氣瓶中少量水的作用。
(2)實驗二是實驗室用一氧化碳還原氧化鐵,硬質玻璃管中的現象是,試管中發生反應的化學方程式為。
(3)實驗三是測定空氣中氧氣體積分數的實驗裝置,燃燒停止后紅磷仍有剩余,燃燒停止的原因是。組卷:17引用:2難度:0.6
三、(本題包括2小題,共24分)
-
24.某化學興趣小組為探究氫氧化鈉的性質,進行了如下系列實驗。
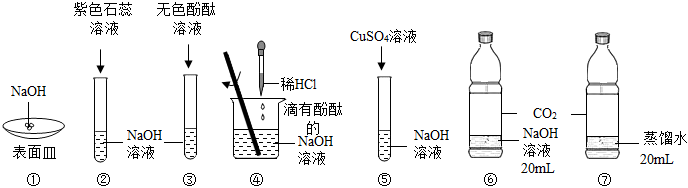
(1)實驗②:向試管中滴入紫色石蕊溶液后,試管內溶液變成色。
(2)實驗④:當滴加稀鹽酸至溶液顯無色時,此時溶液中的溶質:一定含有的氯化鈉,還可能含的溶質有(填化學式)。為檢驗可能含有的溶質,選用下列哪些試劑可達到檢驗目的(填字母代號)。
A.AgNO3溶液
B.CuO
C.Fe
(3)實驗⑤:寫出觀察到藍色沉淀的化學反應方程式。
(4)實驗⑥⑦為用軟礦泉水瓶所做的對比實驗,裝氫氧化鈉溶液的軟礦泉水瓶變癟更明顯,原因是(用化學方程式表示)。
(5)判斷一個反應能否進行,可以檢驗反應物的消失,也可以檢驗生成物的存在,請你設計實驗方案證明⑥試管中有新物質的生成:(寫出操作及其現象)。組卷:38引用:2難度:0.4 -
 25.某小組同學在協助老師整理化學試劑時,發現一瓶標簽殘缺,其質量分數為5%的無色液體(如圖)。他們對此瓶無色液體產生了興趣,于是經過教師同意后進行了如下探究。
25.某小組同學在協助老師整理化學試劑時,發現一瓶標簽殘缺,其質量分數為5%的無色液體(如圖)。他們對此瓶無色液體產生了興趣,于是經過教師同意后進行了如下探究。
【提出問題】無色液體的成分是什么?
【大膽猜想】
猜想一:只是水
猜想二:稀硫酸
猜想三:過氧化氫溶液
小組同學對標簽進行了仔細的觀察、分析,他們一致認為猜想一不合理。理由是。
【設計方案】
同學們結合所學知識設計出如下探究方案。
(1)向盛有少量無色液體的試管加入幾顆鋅粒。
(2)向盛有少量二氧化錳的試管中加入適量的該液體,并將帶火星的木條放在試管口。
【實驗與事實】
實驗(1)無明顯現象。
實驗(2)有產生,帶火星的木條復燃,證明生成的氣體是。在反應中二氧化錳起作用。
【結論與解釋】
(1)以上事實證明猜想是正確的。
(2)產生氣體的反應的符號表達式為。
【反思與評價】
(1)在實驗中,某同學提出應該先將氣體收集,然后用帶火星的木條檢驗,你認為(填“有”或“沒有”)必要。
(2)為避免在今后的實驗中出現標簽殘缺的情況,在傾倒液體時應注意。
【拓展與遷移】
根據探究結果,重新貼好標簽。標簽上化學式H2O2中氧元素的化合價為價。組卷:5引用:1難度:0.5
四、(本題包括2小題,共10分)
-
26.食醋中一般含有3%-5%的醋酸,醋酸又叫乙酸(CH3COOH),是無色有刺激性氣味的液體,能溶于水。現在有含醋酸4%的食醋200g,小明同學用含醋酸4%的食醋配制2%的醋酸溶液,需要加水的質量時多少?最后配制出的2%的醋酸溶液是多少克?
組卷:12引用:2難度:0.6 -
27.我國科學家實現電催化高效分解硫化氫技術,根據化學方程式計算生產2噸氫氣,理論上需要硫化氫多少噸?(將以下計算過程補充完整)
解:設理論上需要硫化氫的質量為x。
H2SS↓+H2一定條件組卷:22引用:1難度:0.6


