2021年江西南昌紅谷灘區上海外國語學校中考化學復習卷(10)
發布:2025/7/2 12:0:10
一.選擇題(共9小題)
-
1.下列金屬各30克,分別與足量稀鹽酸反應,生成氫氣最多的是( )
A.Al B.Mg C.Fe D.Zn 組卷:39引用:3難度:0.7 -
 2.中華民族在世界冶金史上曾譜寫過輝煌的篇章,如圖即為我國東漢晚期所鑄的青銅奔馬(馬踏飛燕)。早在2000多年前的西漢時期就有“曾青得鐵則化為銅”的記載,從現代化學的觀點理解,這句話的涵義是( )
2.中華民族在世界冶金史上曾譜寫過輝煌的篇章,如圖即為我國東漢晚期所鑄的青銅奔馬(馬踏飛燕)。早在2000多年前的西漢時期就有“曾青得鐵則化為銅”的記載,從現代化學的觀點理解,這句話的涵義是( )A.木炭還原氧化銅生成單質銅 B.氧化銅在單質鐵的催化作用下,分解成銅 C.氫氧化銅和鐵的化合物反應生成銅 D.單質鐵從銅鹽溶液中置換出銅 組卷:10引用:8難度:0.7 -
3.如圖為某同學設計的工業煉鐵的模擬裝置。下列說法正確的是( )
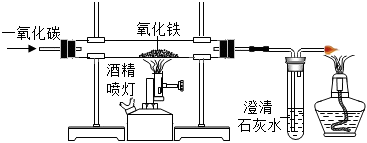
A.實驗過程中澄清石灰水變渾濁 B.實驗中硬質玻璃管內的現象是紅色氧化鐵變成黑色的鐵粉 C.實驗中應該先點燃酒精噴燈,再點燃酒精燈 D.實驗結束后,先停止通入CO,再熄滅酒精噴燈 組卷:444引用:4難度:0.6 -
4.向硝酸銀溶液中加入一定質量的鋁粉和銅粉的混合物,充分反應后過濾,得到濾渣和濾液。以下推斷正確的是( )
A.濾液中一定含有硝酸鋁和硝酸銅 B.若向濾渣中加入鹽酸,若無氣泡產生,則濾液中一定沒有硝酸銅 C.濾渣中一定含有銅和銀 D.反應后所得濾渣的質量一定比加入的混合物質量大 組卷:101引用:3難度:0.8 -
5.學習化學的目的并不在于要成為化學家,重要的是善于用化學知識去分析、解決生產生活中的問題.從化學的角度看,下列說法中正確的是( )
A.常用鋼絲球擦洗鋁壺可以使其光亮潔凈且耐用 B.食品添加劑對人體有害,應禁止生產和使用任何食品添加劑 C.夜晚發現液化氣泄漏立即開燈檢查 D.日本大地震中和核泄漏事件引起人們的反思,要安全可靠地使用核能 組卷:9引用:4難度:0.7 -
6.小麥、玉米、高粱都是釀造白酒的原料,富含的營養素是( )
A.蛋白質 B.油脂 C.糖類 D.水 組卷:37引用:4難度:0.8 -
7.下列有關實驗現象正確的是( )
A.把打磨過的鋁絲插入硫酸銅溶液中,鋁絲表面有紅色固體生成,溶液由藍色變為無色 B.打開盛有濃鹽酸的試劑瓶瓶蓋,瓶口上方出現白煙 C.將少量高錳酸鉀放入裝有汽油的試管中振蕩,得到紫紅色溶液 D.氫氧化鉀溶液與氯化鐵溶液混合,有白色沉淀生成 組卷:22引用:2難度:0.6 -
8.鋅、鐵與相同濃度的稀硫酸反應生成相同質量的氫氣,下列說法中不正確的是( )
A.參與反應酸的量可能不足 B.消耗鋅的質量比消耗鐵的質量少 C.消耗稀硫酸中溶質的質量相等 D.相同條件下,鋅與稀硫酸反應比鐵與稀硫酸反應快 組卷:71引用:4難度:0.7 -
9.向等質量的鎂粉與鐵粉中分別加入足量稀硫酸,反應生成的氫氣質量與反應時間的關系圖中,正確的是( )
A. 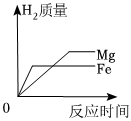
B. 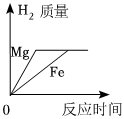
C. 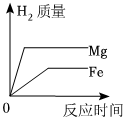
D. 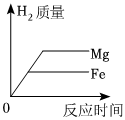 組卷:1引用:0難度:0.9
組卷:1引用:0難度:0.9
二.實驗探究題(共11小題)
-
10.實驗室將一定量的鋅粉加入含硝酸銀的廢液中,用于回收其中的銀。
(1)回收時發生反應的化學方程式為。
(2)反應完全后,為判斷銀是否全部被鋅置換,同學們將反應后的混合物進行過濾,取少量濾渣,滴入稀鹽酸,產生氣泡,由此說明銀(填“全部”或“部分”)被置換。
(3)還可用鐵代替鋅回收廢液中的銀。為驗證鋅、鐵銀三種金屬的活動性順序,小明設計了如圖所示的四個實驗: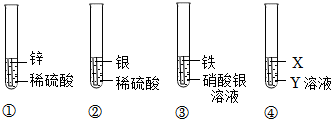
下列說法不正確的是(填字母)。
A.通過實驗①②③能驗證鋅的金屬活動性比鐵的強
B.實驗③中溶液的質量變小
C.X可能為鋅,Y可能為硫酸亞鐵組卷:49引用:3難度:0.5 -
11.學習制取幾種常見氣體丙探究其性質是初中化學學習的重要內容。

(1)甲是實驗室制取氧氣的實驗。試管口放一團棉花的作用是。
(2)乙是制取氣體的裝置。用該裝置收集的氣體具有的性質是。
(3)丙是鐵絲在氧氣中燃燒的實驗。實驗中在瓶底放少量水的作用是。
(4)丁是金屬性質的實驗。步驟①體現了銅具有性,B試管中反應的化學方程式為,由該實驗可得出Ag、Fe、Cu三種金屬的活動性由強到弱的是。組卷:25引用:1難度:0.6 -
12.金屬材料在生產生活中有著廣泛的應用。請回答下列問題:
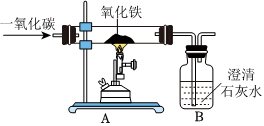
(1)鐵制成鐵鍋利用了鐵的延展性和性。廢舊鐵鍋不要隨意丟棄,應回收利用,這樣做的意義是(寫出一點即可)。
(2)如圖為實驗室用一氧化碳還原氧化鐵實驗裝置圖,該裝置中存在的主要問題是。
(3)某工廠欲從溶質是AgNO3和Cu(NO3)2的生產廢液中回收Ag和Cu。實驗員取樣,向其中加入一定質量的鋅,充分反應后過濾,得到濾渣和濾液。
①若所得濾液為無色,則濾渣中一定含有的金屬是(填化學式,下同)。
②若向所得濾渣中加入一定量稀硫酸,無氣泡冒出,寫出濾液中含有溶質的所有可能組成。組卷:24引用:2難度:0.6 -
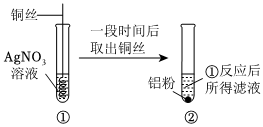 13.為探究金屬的化學性質某同學設計了如圖實驗。
13.為探究金屬的化學性質某同學設計了如圖實驗。
(1)①中發生反應的化學方程式是。
(2)若充分反應后的②中固體有3種,則①反應后的濾液中的溶質是(答名稱)。
(3)若②反應后溶液的顏色為無色,則溶液中的金屬離子符號是。組卷:33引用:3難度:0.5 -
14.某項目小組開展了如圖“鐵的性質”探究實驗。回答下列問題:
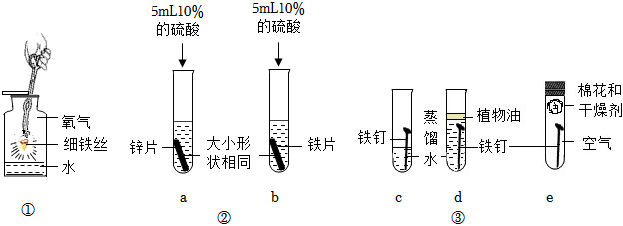
(1)①的實驗現象是。
(2)實驗②中產生氣泡速度更快的是(填字母標號),由此可知金屬活動性:鋅鐵(填“強于”或“弱于”)。試管b中發生反應的化學方程式為,基本反應類型是。
(3)實驗③進行一段時間后,鐵釘明顯銹蝕的是(填字母標號),對比三支試管的現象可知,鐵生銹需要的條件是。組卷:17引用:1難度:0.6 -
 15.近年來,我國已掌握載人航天領域的重大技術,載人航天重大工程建設順利推進。請根據所學知識回答下列問題:
15.近年來,我國已掌握載人航天領域的重大技術,載人航天重大工程建設順利推進。請根據所學知識回答下列問題:
Ⅰ.航天器使用的動力
(1)我國的載人飛船均由長征二號F運載火箭發射升空。運載火箭由三級火箭組成。一級和二級火箭的推進劑為偏二甲肼(C2H8N2)和四氧化二氮(N2O4),其反應的化學方程式為:C2H8N2+2N2O4=3N2+2X+4H2O,則X的化學式為;三級火箭的推進劑為液氫和液氧,請從微觀角度分析能將氣體壓縮成液體的原因:。
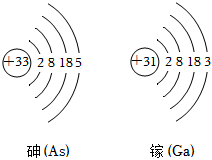
(2)進入太空后,動力由太陽能電池提供。神舟飛船使用的太陽能電池是砷化鎵電池,砷、鎵的原子結構示意圖如圖所示,下列有關說法錯誤的是。
A.砷元素屬于非金屬元素
B.鎵原子在化學反應中易失電子
C.兩種元素位于同一周期
D.砷化鎵的化學式為Ga3As5
Ⅱ.航天器使用的材料
(3)制造飛船的主要材料是鋁,燃料艙、載人艙、軌道艙等部件都使用了大量的鋁合金。鋁合金屬于(填“金屬材料”或“合成材料”)。鋁除密度小外,還具有優良的抗腐蝕性能,其原因是(用化學方程式表示)。
(4)飛船上還使用了記憶合金、SiC顆粒增強鋁基復合材料、橡塑材料、超高強度鋼等新材料。其中超高強度鋼材料中錳的金屬活動性比鐵強,請設計一個實驗證明錳的金屬活動性比鐵強:。
Ⅲ.航天器的生命保障系統
(5)飛船中航天員呼吸的氧氣是將從尿處理系統輸送來的水進行電解制取的。寫出電解水的化學方程式。
(6)航天員呼出的二氧化碳是在高溫下通過催化劑的作用與氫氣反應,生成水和甲烷,其中水可以被送往飲用水系統供航天員飲用。若每天航天員能呼出3.3kg二氧化碳,則通過上述反應可產生水的質量是多少?組卷:24引用:2難度:0.5 -
16.硫酸鹽的結晶水合物通常稱為“礬”,我國多部古籍都有記載。
(1)東漢《神農本草經》記載,膽礬能“化鐵為銅”。
膽礬的化學式為CuSO4?5H2O,膽礬受熱失去結晶水的過程屬于(選填“物理“或“化學”)變化;將鐵片浸入硫酸銅溶液可實現“化鐵為銅”,反應的化學方程是,說明鐵的金屬活動性比銅(選填“強”成“弱”)。
(2)唐代《千金翼方》記載,明礬可入藥用。
明礬的化學式為KAl(SO4)2?12H2O,其中含有種金屬元素;K2SO4中K元素的化合價是;
(3)明代《天工開物》記載,綠礬可用黃鐵礦為原料制得。綠礬的化學式為FeSO4?7H2O。FeSO4?7H2O屬于(選填“純凈物“或“混合物”);1molFeSO4中約含有個S原子。組卷:183引用:1難度:0.5 -
17.如圖所示為實驗室中常見氣體制備、凈化、干燥、收集和進行實驗探究的部分儀器(組裝實驗裝置時,可重復選擇儀器),化學小組的同學利用其進行下列化學實驗。
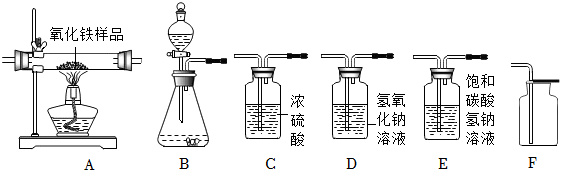
請根據題目要求,回答下列問題:
(1)以石灰石和稀鹽酸為原料,在實驗室中制備并收集一瓶干燥且不含HCl的二氧化碳氣體,按照要求設計實驗裝置,連接儀器,檢查裝置的氣密性,進行實驗。(提示:鹽酸中揮發出的少量HCl氣體可用飽和碳酸氫鈉溶液吸收)
①所選儀器的連接順序為(從左到右填寫儀器序號字母)。
②上述方法制取二氧化碳的化學方程式為。
③向一個收集滿二氧化碳氣體的集氣瓶中,同時放入一張干燥的藍色石蕊試紙和一張濕潤的藍色石蕊試紙,觀察到干燥的試紙不變色,而濕潤的試紙變紅。請敘述出現上述兩種不同現象的原因:
(2)化學小組的同學用一氧化碳氣體(含少量水蒸氣),測定某氧化鐵樣品(雜質為鐵粉)中Fe2O3的質量分數,設計了實驗方案,所選儀器按“CO(含少量水蒸氣)→C→A→D1→D2”的順序連接(D1、D2為氫氧化鈉洗氣瓶),檢查裝置的氣密性,然后進行實驗。(假設發生的化學反應都充分反應)
①該裝置中,洗氣瓶C的作用為
②進行實驗時,檢查完裝置的氣密性,在儀器A硬質玻璃管中放入12g該氧化鐵樣品后,進行以下操作,其中應該先進行的是(填選項序號之一)。
a.用酒精燈加熱
b.通入一氧化碳氣體(含少量水蒸氣)
③反應充分進行后冷卻,測得此時洗氣瓶C增重1.8g,洗氣瓶D1增重6.6g,則12g該氧化鐵樣品中Fe2O3的質量分數為(計算結果精確至0.1%),該氧化鐵樣品中鐵元素與氧元素的質量比為(填最簡整數比)。
④從環保角度考慮,該套實驗裝置還存在明顯的不足之處,你的具體改進建議是。組卷:692引用:3難度:0.4 -
18.人類的生活和生產離不開金屬。了解金屬的性質對科學的利用金屬材料是十分重要的。
(1)用銅制電線是利用銅的導電性和。
(2)為探究鋅、銅、鈧(Sc)的金屬活動性順序,某同學進行了如下三個實驗(金屬片均已打磨且形狀、大小相同,試管中所用5%的鹽酸體積相同)。實驗一 實驗二 實驗三 實驗操作 


實驗現象 ,速率較快無明顯現象 立即產生氣泡,速率更快 實驗結論 實驗一反應的化學方程式為
鋅、銅、鈧的金屬活動性順序(由強到弱)為組卷:25引用:2難度:0.6 -
19.利用Y形實驗裝置進行的系列探究如圖所示。

(1)圖一用于探究分子具有不斷運動的性質,所需藥品分別是。
(2)圖二探究金屬活動性強弱:若固體是銅粉、液體是硝酸銀溶液,傾斜Y形管,使液體與固體接觸,觀察到有銀白色固體析出,溶液由無色變色,說明銅的金屬活動性比銀(選填“強”或“弱”)。
(3)圖三探究燃燒條件:固體是白磷(足量)、液體是80℃熱水,開始白磷不燃燒,傾斜Y形管,熱水與白磷剛接觸,白磷燃燒,繼續傾斜Y形管,直至熱水浸沒白磷,白磷熄滅。得出燃燒條件“需要與氧氣接觸”這一結論的依據是,實驗中80℃熱水的作用之一是。組卷:21引用:2難度:0.5 -
20.實驗中要除去細碎銅屑中的少量細碎鐵屑,某學生設計了兩個方案:

兩個方案中,較好的是(填序號),理由是。你是否有更簡單的方法,若有,請寫出做法:。寫出本實驗有關的化學方程式。組卷:13引用:1難度:0.5
三.計算題(共1小題)
-
21.伊娜老師為了測試六班同學的計算能力,準備了一瓶未知濃度的過氧化氫溶液,曉樓帶領他們小組的同學完成此次實驗,浩南取部分溶液進行了如下實驗,請結合實驗回答下列問題:
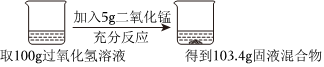
(1)上述實驗過程中發生反應的化學方程式為;
(2)產生氧氣的質量為g;
(3)張揚根據生成的氧氣的質量求解參加反應的過氧化氫質量(x)的比例式;
(4)若熙賀配制上述濃度的過氧化氫溶液200g,需要30%的過氧化氫溶液g;
(5)王妍同學發現化學書上給出了可以用硫酸銅溶液來代替MnO2做此反應的催化劑,于是伊娜老師提出用含80%Cu2S的輝銅礦來煉制實驗所需的硫酸銅,若想制得16g硫酸銅用于實驗,需輝銅礦的質量是g。組卷:6引用:1難度:0.5


