2020-2021學年江蘇省泰州市泰興濟川中學九年級(上)期末化學試卷
發布:2025/7/2 18:0:9
一、單項選擇題(第1~10題,每題只有一個選項符合題意,每小題1分,共10分。)
-
1.如圖是元素周期表中鋁元素的某些信息。由該圖不能獲得的信息是( )

A.鋁元素符號是Al B.地殼中含量最高的金屬元素是鋁 C.相對原子質量是26.98 D.原子序數是13 組卷:130引用:2難度:0.5 -
2.向硝酸銀和硝酸銅的混合溶液中加入一定量鋅粉,反應結束后過濾,得到濾渣和濾液,再向濾渣中加入稀鹽酸,有氣泡產生,下列說法正確的是( )
A.濾液可能呈藍色 B.濾液中的陽離子只有Zn2+ C.濾渣中只有Ag、Cu D.濾液中的陽離子Ag+、Cu2+、Zn2+ 組卷:322引用:4難度:0.5 -
3.下列對某一主題知識歸納全部正確的是( )
A.性質與用途 B.生活常識 銅具有導電性---制造炮彈
干冰易升華---作致冷劑
石蕊遇酸堿變色---作酸堿指示劑鑒別羊毛纖維---點燃嗅聞有燒毛發味
新裝修居室---一定揮發出有毒氣體
人類可利用的氫氣---為三大化石燃料之一C.化學之最 D.初中化學的“三” 最簡單的有機物---氫氣
最輕的氣體---甲烷
最早濕法煉銅的國家---中國單質可分為三類---金屬、非金屬、稀有氣體
有還原性的三種物質---氫氣、一氧化碳、炭
農作物肥料“三要素”---氮、磷、鉀A.A B.B C.C D.D 組卷:43引用:2難度:0.9 -
 4.人體缺氟容易患齲齒病,如圖是氟元素在元素周期表的信息和氟原子結構示意圖,下列說法正確的是( )
4.人體缺氟容易患齲齒病,如圖是氟元素在元素周期表的信息和氟原子結構示意圖,下列說法正確的是( )A.氟的原子核內中子數是9 B.氟元素屬于金屬元素 C.氟原子在化學反應中容易得到1個電子形成F- D.氟的相對原子質量是19.00g 組卷:12引用:2難度:0.7 -
5.下列物質能與水發生置換反應的是( )
A.氧化鈉 B.鈉 C.二氧化硫 D.無水硫酸銅 組卷:17引用:1難度:0.9 -
6.下列四個圖像中,不能正確反映其對應變化關系的是( )
A. 
一定量的鎂條在空氣中點燃生成氧化鎂的質量B. 
加熱高錳酸鉀制取氧氣時剩固體的質量C. 
一定質量的木炭與過量氧氣在密閉容器內加熱使其充分反應D. 
在密閉容器中點燃H2和O2的混合氣體組卷:399引用:4難度:0.6 -
7.下列圖示的實驗操作正確的是( )
A. 
取用液體藥品B. 
轉移蒸發皿C. 
制取H2D. 
稀釋濃硫酸組卷:7引用:1難度:0.6 -
8.下列化學用語表示正確的是( )
A.鋁的元素符號:AL B.2個氫原子:H2 C.氦氣:He D.鎂離子:Mg+2 組卷:6引用:1難度:0.9 -
9.下列各種物質的用途中,利用其物理性質的是( )
A.氧氣供給呼吸 B.熟石灰用于改良酸性土壤 C.稀鹽酸除鐵銹 D.稀有氣體作為燈管制霓虹燈的填充氣 組卷:2引用:1難度:0.6 -
10.酚酞(化學式為C20H14O4)為白色或微帶黃色的細小晶體,實驗室通常將酚酞與酒精配制成溶液用作指示劑。下列說法錯誤的是( )
A.酚酞屬于氧化物 B.酚酞能溶解在酒精中 C.酚酞中碳、氫元素的質量比為120:7 D.1個酚酞分子中有38個原子 組卷:7引用:1難度:0.7
二、不定項選擇題(第11~15題,每題有1個或2個選項符合題意。錯選、多選均不得分,少選得1分。每小題2分,共10分。)
-
11.下列物質中,直接由原子構成的是( )
A.金 B.碘 C.氫氣 D.酒精 組卷:9引用:1難度:0.6 -
 12.如圖是鐵元素在元素周期表中的部分信息及原子結構示意圖。下列有關鐵的說法不正確的是( )
12.如圖是鐵元素在元素周期表中的部分信息及原子結構示意圖。下列有關鐵的說法不正確的是( )A.鐵原子中質子數為26 B.鐵原子在化學反應中易失去電子 C.生鐵的含碳量比鋼的含碳量高 D.鐵與稀鹽酸反應的產物為FeCl3和H2 組卷:70引用:4難度:0.6 -
13.科學家利用太陽光在新型催化劑表面高效分解水,微觀過程如下圖。下列說法正確的是( )

A.該反應為分解反應 B.反應后氫元素和氧元素化合價都升高 C.反應前后分子數目不變 D.產生的氫分子和氧分子的個數比為2:1 組卷:11引用:2難度:0.5 -
14.下列各組溶液,不用其他試劑就能鑒別出來的是( )
A.CuSO4、NaOH、KNO3、NaCl B.K2CO3、NaOH、稀HCl、BaCl2 C.FeCl3、KOH、稀HCl、NaCl D.稀HCl、Na2CO3、稀H2SO4、Na2SO4 組卷:361引用:21難度:0.5 -
15.國產“手撕鋼”的厚度僅0.015毫米,被譽為“百煉鋼做成了繞指柔”,其利用了金屬的( )
A.硬度大 B.導熱性 C.導電性 D.延展性 組卷:201引用:7難度:0.5
三、非選擇題(共40分)
-
16.鉛是一種用途廣泛的重金屬,但它也給人類帶來了災難.進入人體的鉛會嚴重影響神經、腎臟等系統,尤其阻礙兒童的智力發育.考古發現,古羅馬人的遺骸中含有大量的鉛,原來古羅馬貴族慣用鉛制器皿和含鉛化妝品,就連當時的輸水管道也是鉛做的,所以許多學者認為“顯赫一時的古羅馬帝國是因為鉛中毒而快速滅亡的!”目前,我國6成半少兒血鉛含量偏高,有些地方甚至發生兒童群體鉛中毒的惡性事件.
(1)古代煉丹經常用到鉛丹.鉛丹跟硝酸發生如下反應:鉛丹+4HNO3=PbO2+2Pb(NO3)2+2H2O,則鉛丹的化學式是,此化合物中各元素的質量比.
(2)氧化鉛常作為陶釉的成分,以優化陶瓷坯體的性能.但它易溶于醋酸、熱堿,從而使毒鉛溶出,為減少陶釉中的鉛的溶出,現代陶瓷業多將氧化鉛預先制成硅酸鉛熔塊后再使用.請你據此推測硅酸鉛的化學性質:(寫出一條即可).
(3)鉛的化合物多有墜痰、鎮驚、殺蟲和解毒等藥效(如PbS和Pb3O4),有的還用于美白類化妝品(如PbO).但是,醫生一定會嚴格要求使用者“只可暫用,并嚴密觀察”.這是為什么呢?.組卷:25引用:4難度:0.9 -
17.氧氣、二氧化碳的制取與收集是初中重要的化學實驗。如圖是實驗室制取并收集氣體的裝置圖,請你根據如圖回答問題:
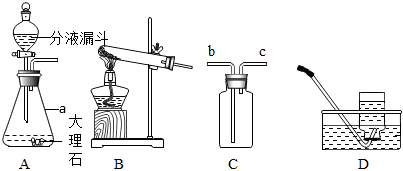
(1)儀器a的名稱是。
(2)若用裝置A制取二氧化碳,分液漏斗中盛裝的藥品是(填化學名稱),發生反應的化學方程式為。若用裝置C收集二氧化碳,氣體應從導管口(選填“b”或“c”)通入。
(3)裝置A與D組合,還可用于實驗室制取氧氣,用裝置D收集氧氣時,要等氣泡時方可收集,以防收集的氧氣不純。
(4)氨氣(NH3)是一種無色、有刺激性氣味、極易溶于水的氣體。實驗室通常用熟石灰和氯化銨固體加熱制取氨氣,實驗室制得的氨氣(選填“能”或“不能”)用裝置D收集。組卷:19引用:2難度:0.6 -
18.A﹣H都是初中常見的物質,其中D為藍色沉淀,A、E是組成元素相同的兩種氣體,F、H為黑色固體.他們之間轉化關系如下圖(反應條件及部分反應物和生成物已略去)
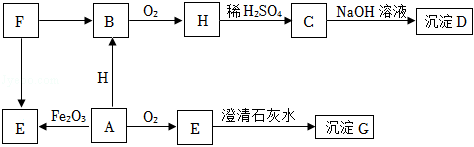
(1)反應F→B屬于(填基本反應類型)
(2)C的化學式是。
(3)寫出下列化學方程式A→EC→D。
(4)答出G的一種用途。
(5)物質H與稀H2SO4反應的現象是。組卷:7引用:1難度:0.5 -
 19.觀察是學習化學的重要方法.我們可以運用自己的感官,也可以借助儀器通過實驗,觀察物質及其變化的條件、現象和結果.下面是甲、乙、丙實驗小組完成的相關實驗.
19.觀察是學習化學的重要方法.我們可以運用自己的感官,也可以借助儀器通過實驗,觀察物質及其變化的條件、現象和結果.下面是甲、乙、丙實驗小組完成的相關實驗.
甲小組:利用如圖1裝置研究燃燒條件(已知白磷的著火點為40℃)
步驟Ⅰ:燒杯中盛有80℃的熱水,分別在燃燒匙和燒杯中導管口放置一小塊白磷,塞緊瓶塞.
步驟Ⅱ:用注射器向瓶內推入適量H2O2溶液
(1)H2O2稀溶液與MnO2接觸時發生反應的化學方程式,二氧化錳起作用.
(2)實驗中,推入H2O2溶液前,燃燒匙和燒杯中水下白磷均不燃燒,原因分別是;推入H2O2溶液后,打開彈簧夾,觀察到燒杯中的現象是.
乙小組:哪些因素影響著過氧化氫分解的速率?
探究實驗1:溫度對化學反應速率的影響
探究實驗2:濃度對化學反應速率的影響過氧化氫溶液濃度 體積 水溫 二氧化錳質量 現象 結論 試管1 5% 5mL 冷水 1g 氣泡緩慢冒出 其它條件相同時溫度越高反應速率越快 試管2 5% 5mL 1g 大量氣泡迅速冒出
丙小組:鎂在空氣中燃燒的化學方程式過氧化氫溶液濃度 體積 二氧化錳質量 現象 結論 試管1 5%(常溫) 5mL 1g 氣泡緩慢冒出 試管2 15%(常溫) 5mL 1g 大量氣泡迅速冒出 ,已知鎂條除了和氧氣反應,還可以和氮氣、二氧化碳發生反應,鎂和氮氣反應的表達式為:3Mg+N2Mg3N2,該反應中氮元素的化合價由0價變為點燃價;鎂和二氧化碳反應的表達式為:2Mg+CO22MgO+C,以上兩個反應說明了:可燃物的燃燒點燃(填“一定”或“不一定”)需要氧氣助燃,倉庫內的鎂條著火,(填“能”或“否”)用二氧化碳滅火.丙組同學將燃著的蠟燭放在如圖1所示的密閉容器中,同時用氧氣傳感器測出密閉容器中氧氣含量的變化如圖2所示,下列說法錯誤的是(填序號).
A.蠟燭燃燒需要氧氣
B.蠟燭燃燒前,密閉容器中氧氣的體積分數為21%
C.蠟燭熄滅后,密閉容器中還有氧氣
D.蠟燭熄滅后,密閉容器中的二氧化碳體積分數為84%組卷:25引用:1難度:0.5 -
 20.自古以來,人類一直在進行與化學有關的實踐,比如煉丹術和煉金術。而近代化學一般從17世紀算起,其標志是元素學說的建立。隨后許多化學家提出的不同理論促使化學學科飛速發展。
20.自古以來,人類一直在進行與化學有關的實踐,比如煉丹術和煉金術。而近代化學一般從17世紀算起,其標志是元素學說的建立。隨后許多化學家提出的不同理論促使化學學科飛速發展。
(1)俄國科學家發現了元素周期律并制作出元素周期表。如圖甲是鈦元素在元素周期表中的一格,鈦原子的質子數為;已知鈦原子的最外層電子數和鈣原子相同,請寫出鈦離子的符號。
(2)法國科學家拉瓦錫第一個定量研究了空氣的組成。實驗室中我們用紅磷燃燒的實驗測定空氣中氧氣的含量,紅磷燃燒時的現象為;該實驗中不能用硫粉代替紅磷,原因是。
(3)拉瓦錫還提出了質量守恒定律。圖乙實驗不能用來驗證質量守恒定律,原因是。
(4)英國科學家道爾頓提出了原子論,請從原子的角度解釋(3)中反應遵守質量守恒定律的原因。
(5)中國科學家侯德榜發明了侯氏制堿法,能同時生產純堿和氯化銨。氯化銨是一種常見的氮肥,化學興趣小組取該化肥樣品11.2g溶解于50g水中,加入100g硝酸銀溶液恰好完全反應后過濾,得到濾液132.5g。請計算該化肥中氯化銨的質量分數。(計算結果精確至0.1%)組卷:9引用:3難度:0.4


