2023-2024學年山西省朔州市部分學校九年級(上)月考化學試卷(12月份)
發布:2025/7/2 20:0:9
一、選擇題(本大題共10個小題,每小題2分,共20分。在每小題給出的4個選項中,只有1個選項符合題目要求,請選出并在答題卡上將該選項涂黑。)
-
1.“中國高鐵,世界第一”,高鐵列車車體材料使用了含鎳不銹鋼,工業上火法煉鎳的原理是C+2NiO
2Ni+CO2↑,則下列說法錯誤的是( )高溫A.反應中碳發生氧化反應 B.將鋼鐵制成新合金,可減緩鋼鐵制品的銹蝕 C.該不銹鋼中還含有鐵和碳 D.該不銹鋼合金的硬度小于純鐵 組卷:15引用:2難度:0.7 -
2.煤油中含有噻吩,噻吩(用X表示)有令人不愉快的氣味,其燃燒的化學方程式可表示為:X+6O2
4CO2+SO2+2H2O,則噻吩X的化學式為( )點燃A.CH4S B.C2H6S C.C4H4S D.C6H6S 組卷:53引用:69難度:0.9 -
3.藍寶石與紅寶石一樣,屬剛玉類寶石,主要成分都是Al2O3(剛玉)。其中鋁元素化合價為( )
A.-3 B.0 C.+2 D.+3 組卷:24引用:2難度:0.6 -
4.甲烷和水反應可以制備水煤氣(混和氣體),其反應的微觀示意圖如圖所示,根據微觀示意圖得出的結論中,你認為不正確的是( )

A.化學反應中分子可分 B.乙屬于氧化物 C.丙可以作燃料 D.反應中甲和丁的分子個數比為1:1 組卷:30引用:6難度:0.9 -
5.下列化學用語正確的是( )
A.氫單質的化學式H B.氦氣的化學式He C.鎂的元素符號mg D.三氧化二鐵的化學式2Fe3O 組卷:6引用:2難度:0.9 -
6.火災是家庭和學校、社會的重要安全隱患之一,為保證我們的人身安全,我們要善于利用學過的知識,采取科學有效的方法保護自己。下列突發事件處理方法正確的是( )
A.電器著火,立即用水撲滅 B.煤氣泄漏,立即開燈查看 C.油鍋著火,立即蓋上鍋蓋 D.房間著火,立即開窗通風 組卷:43引用:3難度:0.8 -
7.宏觀辨識與微觀探析是化學核心素養之一。下列對宏觀事實的微觀推理錯誤的是( )
A.熱脹冷縮——隨著溫度的升降,微粒的大小發生了改變 B.墻內開花墻外可聞到花香——分子在不斷地運動 C.金剛石和石墨的物理性質不同——構成它們的原子排列方式不同 D.氣體可壓縮儲存于鋼瓶中——分子之間有間隔 組卷:21引用:2難度:0.5 -
8.燃燒是人類最早利用的化學變化之一,運用燃燒和滅火的知識是同學們應該具備的基本科學素養。下列滅火的措施或行為你認為錯誤的是( )
A.炒菜時油鍋著火,用滅火毯蓋滅 B.用電器短路造成起火時,用水澆滅 C.堆放雜物的紙箱著火時,用水澆滅 D.戶外野營點燃的篝火,用沙土蓋滅 組卷:31引用:3難度:0.7 -
9.下列圖標不屬于常用危險化學品標志的是( )
A. 
B. 
C. 
D.  組卷:239引用:10難度:0.8
組卷:239引用:10難度:0.8 -
 10.如圖是鐵元素在元素周期表中的部分信息及原子結構示意圖。下列有關鐵的說法不正確的是( )
10.如圖是鐵元素在元素周期表中的部分信息及原子結構示意圖。下列有關鐵的說法不正確的是( )A.鐵原子中質子數為26 B.鐵原子在化學反應中易失去電子 C.生鐵的含碳量比鋼的含碳量高 D.鐵與稀鹽酸反應的產物為FeCl3和H2 組卷:70引用:4難度:0.6
二、工程、技術應用題(本大題共5個小題。化學方程式每空2分,其余每空1分,共16分。)
-
11.2022年11月29日,神舟15號載人飛船搭載火箭,再送3名宇航員進入天宮空間站,與其他3名在軌宇航員成功會師。
(1)火箭通常采用燃燒劑(如航空煤油、酒精、偏二甲肼、液氫)和氧化劑(如液態氧、四氧化二氮等)作為火箭的推進劑。液氫做燃料的優點是;其中偏二甲肼燃燒的化學方程式為:C2H8N2+2N2O44H2O+3N2+2X,則X的化學式為點燃。
(2)酒精作為可再生能源,被很好地利用,酒精燃燒的化學方程式是。
(3)航天員在空間站生活用水除了帶到太空的儲備水,還會循環利用,其中“再生生保”系統收集航天員的尿液和散發到空氣中的水蒸氣,將其凈化為純凈水。
①在日常生活中凈化水的方法有哪些?。
②航天員所需氧氣是通過電解水得到,電解水的基本反應類型是。
(4)天宮空間站的外殼一般采用高強度纖維材料或鈦合金制造,這是利用了鈦合金、的性質。
(5)太空鋁是被廣泛應用的航天材料,已知某工廠從500kg鋁土礦(主要成分是Al2O3)冶煉得到108kg鋁。反應方程式是2Al2O3(熔融)4Al+3O2↑,計算鋁土礦中氧化鋁的質量分數。冰晶石通電組卷:19引用:1難度:0.5
二、工程、技術應用題(本大題共5個小題。化學方程式每空2分,其余每空1分,共16分。)
-
12.科學精神與社會責任,是化學學科素養更高層面的價值追求。在一次實踐活動中,小紅和同學們一起參觀了某鋼鐵公司,大家對礦石選取、治鐵和煉鋼的工藝流程(如圖所示)、生鐵和鋼的區別等有了全新的認識。
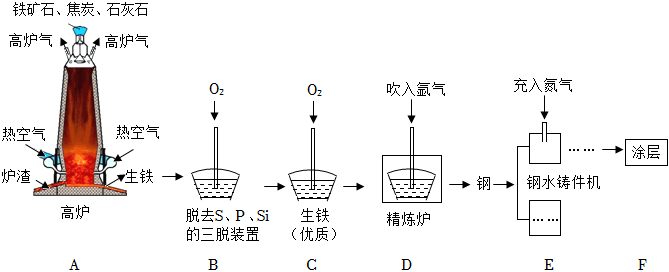
(1)用赤鐵礦石治鐵的反應原理是(用化學方程式表示)。
(2)分析工藝流程,三脫裝置中發生反應的化學方程式分別是、和。
(3)向精煉爐中吹入氬氣使鋼水循環流動,各成分均勻混合,相當于化學實驗中(填一種儀器的名稱)的作用。
(4)在鋼水鑄件機中,高溫下鋼加工成鋼制零件時,充入氮氣的作用是。組卷:10引用:1難度:0.6
三、科普閱讀題(本大題共1個小題。化學方程式每空2分,其余每空1分,共7分。)
-
13.閱讀下列科普短文,回答問題。
“碳中和”是指人類活動的碳排放通過植樹造林和人工手段加以捕集、利用和封存,使排放到大氣中的溫室氣體凈增量為零。高效的CO2捕集和封存技術會為我國2060年實現“碳中和”目標作出巨大貢獻。目前,CO2捕集技術的關鍵是將CO2從排放物中分離出來。分離方法主要分為物理吸收法和化學吸收法。物理吸收法中的一種是用甲醇作溶劑進行吸收;另一種是用活性炭、沸石等對CO2進行吸附性吸收。分離后的CO2可以用來制取甲醇(CH3OH),反應的微觀示意圖如圖1所示。在實際生產中,CH3OH的產率除受濃度、溫度、壓強等因素影響外,還受催化劑CuO質量分數的影響(如圖2)。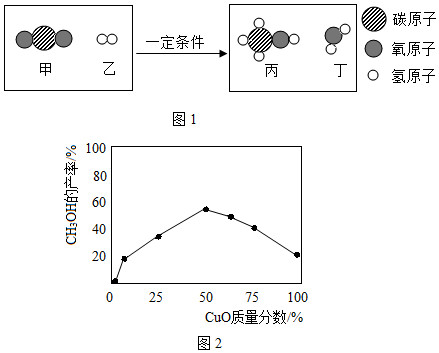
我國科學家們撰文提出“液態陽光”概念,即將太陽能轉化為可穩定存儲并且可輸出的燃料,實現燃料零碳化。隨著科學技術的發展,今后的世界,每天的陽光將為我們提供取之不盡、用之不竭的熱、電,還有可再生燃料!
依據文章內容回答下列問題。
(1)下列說法正確的是(填序號)。
A.碳中和中的“碳”指的是碳單質
B.控制化石燃料的使用可減少碳排放
C.碳中和指的是沒有二氧化碳排放
D.“液態陽光”將實現燃料零碳化
(2)活性炭、沸石等可作吸附劑,則其可能具備的結構特點是。
(3)根據圖1寫出CO2制取甲醇的化學方程式:。
(4)結合資料和圖2信息,甲醇的產率與CuO質量分數關系是。組卷:86引用:6難度:0.7
四、物質性質及應用題(本大題共1個小題。化學方程式每空2分,其余每空1分,共6分。)
-
14.某廢酸液主要含H2SO4和FeSO4,研究人員利用CaCO3消耗部分酸,再加入廉價的電石渣(主要成分為CaO),通過一系列操作可得到磁性鐵,成本較低且有利于保護環境。工藝流程如圖:
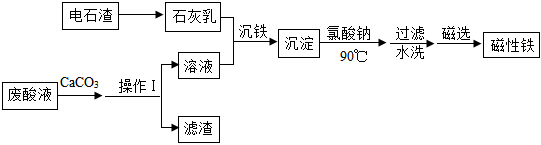
(1)該廢酸液的pH7(填“<”或“>”)。
(2)電石渣轉化為石灰乳的過程會(填“吸收”或“放出”)熱量。
(3)“沉鐵”過程中,溶液中的FeSO4和石灰乳中的Ca(OH)2發生復分解反應,反應的化學方程式為:。
(4)研究發現,“沉鐵”后,溶液的pH對磁性鐵產率的影響如下表。欲獲得高的產率,最適宜的pH為,pH較低時產率較低的主要原因是。
(5)磁性鐵是鐵的一種氧化物,且為磁鐵可的主要成分,其化學式為溶液的pH 6.0 6.5 7.0 7.5 8.0 9.0 產物顏色 黃褐色 黃褐色 較黑 很黑 很黑 灰黑色 產率(%) 43.9 50.6 96.2 93.0 92.3 91.6 。工業上常用磁鐵礦冶煉生鐵,寫出其原理的化學方程式。
某同學發現用生鐵與過量的稀硫酸充分反應后,容器底部總殘留有黑色固體,該黑色固體中一定含有的成分是。組卷:25引用:1難度:0.7
五、定量分析題(本大題共1個小題。(1)2分,(2)4分,共6分。)
-
15.1869年俄國化學家門捷列夫在編制元素周期表時曾預言31號“類鋁”元素,1875年布瓦博得證明了這種元素--鎵(Ga)的存在,并證明了它的化學性質和鋁相似,和鋁的化合價一致。
(1)寫出金屬鎵和硫酸反應的化學方程式。
(2)足量的鎵與100g溶質質量分數為9.8%的硫酸充分反應,生成H2的質量為多少。組卷:77引用:1難度:0.6
六、實驗探究題(本大題共2個小題。化學方程式每空2分,其余每空1分,共15分。)【實驗設計】
-
16.4月23日同學們進行了物理化學實驗考查.化學實驗有“實驗室制取二氧化碳氣體、收集和驗滿”和“配制50g6%的NaCl溶液”兩實驗供抽選.
【檢查藥品與儀器】小文同學抽到了“二氧化碳的制取、收集和驗滿”實驗.下圖是實驗桌上擺放好的該實驗所需的用品.實驗前小文發現其中缺少了一種實驗儀器和一種藥品,請你寫出所缺儀器的名稱;所缺藥品是;寫出該實驗反應的化學方程式.
【實驗操作】如圖是小文實驗時的主要步驟,這些步驟的正確順序是(填字母標號),其中操作有誤的是(填字母標號).
【反思】氨氣極易溶于水,常溫常壓下1體積水可溶解700體積的氨氣,溶解時氨氣與水反應生成一水合氨,溶液顯堿性.氨氣的密度比空氣小.實驗室制氨氣的反應如下:2NH4Cl(固體)+Ca(OH)2(固體)2NH3↑+CaCl2+2H2O.能否用實驗室制取二氧化碳的發生裝置制氨氣?加熱(填“能”或者“否”),實驗室氨氣的收集方法是.組卷:24引用:1難度:0.3
【科學探究】
-
 17.某校課外活動小組,欲測定山洞菜窖中空氣中CO2的體積分數(假設菜窖內空氣 中不含除CO2外的其他酸性氣體)。已知空氣中CO2的體積分數達到5%人會昏厥,該小 組進行了如下實驗:
17.某校課外活動小組,欲測定山洞菜窖中空氣中CO2的體積分數(假設菜窖內空氣 中不含除CO2外的其他酸性氣體)。已知空氣中CO2的體積分數達到5%人會昏厥,該小 組進行了如下實驗:
(1)取樣。他們準備從菜窖中的底部取樣,請你設計用集氣瓶從洞中取回一瓶空氣樣品的方法。(假設洞內CO2濃度是安全的)
(2)測定。用150mL的注射器從廣口瓶中抽取100mL氣樣,按如圖所示的裝置進行實驗將氣體推入甲中。
回答下列問題:
①甲中多孔球泡的作用,甲裝置中NaOH的作用是,寫出化學方程式。
②實驗結束后,量筒內水的體積為99mL,菜窖中底部空氣中CO2的體積分數為。
(3)菜窖中二氧化碳氣體的主要來源是。為降低菜窖中CO2的含量,你認為應采取的措施有。
下面是燈火實驗與石灰水實驗測量CO2體積分數的數據:
方法一:分別向二氧化碳含量不同的空氣中放入燃著的蠟燭。
方法二:分別向二氧化碳含量不同的空氣中加入適量的澄清石灰水。
【實驗現象】
【分析與應用】空氣中二氧化碳 體積分數 0.03% 1% 5% 10% 20% 方法一 正常燃燒 正常燃燒 正常燃燒 燃燒不旺 熄滅 方法二 不變渾濁 變渾濁 變渾濁 變渾濁 變渾濁
(4)上述實驗中,方法一所依據的二氧化碳的性質是;從現象分析在進入久未開啟的菜窖前做傳統的燈火實驗,安全嗎?請說明理由。組卷:26引用:1難度:0.5


