2023年河南省南陽市二十一中中考化學三模試卷
發(fā)布:2025/7/4 14:0:11
一、選擇題(本題包括14個小題,每小題1分,共14分)
-
1.分子、原子、離子等都是構(gòu)成物質(zhì)的微粒,下列物質(zhì)由離子構(gòu)成的一組是( )
A.He B.NH3 C.C60 D.NaCl 組卷:11引用:1難度:0.6 -
2.下列物質(zhì)的變化屬于化學變化的是( )
A.麥子磨成粉 B.玻璃破碎 C.食物腐爛 D.石蠟熔化 組卷:1引用:1難度:0.9 -
3.化學反應前后,肯定沒有變化的是( )
①原子的種類 ②分子種類 ③元素的種類 ④元素的化合價
⑤原子的數(shù)目 ⑥物質(zhì)的種類 ⑦反應前后物質(zhì)的狀態(tài)A.①③⑤ B.①②③④⑤⑦ C.①③④⑤⑦ D.全部 組卷:75引用:2難度:0.5 -
4.下列實驗基本操作正確的是( )
A. 
液體的加熱B. 
傾倒液體C. 
氧氣驗滿D. 
檢查氣密性組卷:7引用:3難度:0.9 -
5.化肥對提高農(nóng)作物的產(chǎn)量具有重要作用。為了增強作物的抗倒伏能力,建議施用的化肥是( )
A.Ca(H2PO4)2 B.NH4HCO3 C.KCl D.CO(NH2)2 組卷:79引用:3難度:0.7 -
6.下列一些化學常識與我們的生活息息相關(guān),其中敘述錯誤的是( )
A.成年人在正常情況下每天要攝入食鹽3-5克 B.正常的雨水的pH值約為5.6 C.醫(yī)用生理鹽水是0.5%的氯化鈉溶液 D.當空氣中二氧化碳的體積分數(shù)達到1%時,對人體就有害處 組卷:17引用:1難度:0.9 -
7.我市某化工廠排放的廢液中含有硫酸銅和硫酸亞鐵.某化學興趣小組的同學取了適量的上述廢液樣品,將一定量鋅粉加入樣品中,充分反應后過濾,得到濾液A和固體B.關(guān)于濾液A所含溶質(zhì)的猜想中,不合理的是( )
A.只有硫酸鋅 B.硫酸鋅、硫酸亞鐵 C.硫酸鋅、硫酸銅 D.硫酸鋅、硫酸亞鐵、硫酸銅 組卷:44引用:1難度:0.9 -
8.下列實驗相關(guān)現(xiàn)象的描述正確的是( )
A.磷在氧氣中燃燒產(chǎn)生大量白色煙霧 B.鐵絲在氧氣中燃燒,火星四射,生成黑色固體 C.硫在空氣中燃燒,發(fā)出明亮的藍紫色火焰 D.蠟燭在氧氣中燃燒生成二氧化碳和水 組卷:733引用:27難度:0.9 -
9.下列氣體中,既能用濃硫酸干燥,也可以用氫氧化鈉干燥的是( )
A.CO2 B.CO C.SO2 D.NH3 組卷:103引用:22難度:0.9 -
10.如圖是探究燃燒條件的實驗裝置圖,下列說法錯誤的是( )

A.Ⅰ中銅片上的白磷燃燒,而紅磷不燃燒,說明燃燒需要溫度達到可燃物的著火點 B.Ⅱ中通入氧氣后,水中的白磷燃燒,說明燃燒需要氧氣 C.Ⅱ中白磷換成紅磷,也能產(chǎn)生相同現(xiàn)象 D.圖中熱水的作用有2個:提高溫度、隔絕氧氣 組卷:16引用:2難度:0.5 -
11.有三個集氣瓶,其中分別盛有空氣、二氧化碳、氧氣,欲鑒別它們,較好的方法是( )
A.用帶火星的木條伸入瓶內(nèi) B.用燃著的木條伸入瓶內(nèi) C.向各瓶中倒入適量的等體積澄清石灰水 D.向各瓶中加入適量的等體積的水 組卷:8引用:3難度:0.9 -
12.為運輸安全,掃描二維碼可下載化學品安全標簽和技術(shù)說明書等,掃描濃硫酸運輸罐車二維碼可看到的圖標是( )
A. 
B. 
C. 
D.  組卷:6引用:2難度:0.6
組卷:6引用:2難度:0.6 -
13.網(wǎng)絡一種減肥食譜:“早餐:雞蛋+水果;午餐:牛肉+蔬菜;晚餐:魚肉+水果”。這種飲食方式由于營養(yǎng)不均衡,會導致嚴重后果。該減肥食譜中缺乏的營養(yǎng)素是( )
A.糖類 B.油脂 C.維生素 D.蛋白質(zhì) 組卷:100引用:5難度:0.8 -
14.如圖是自然界中碳、氧循環(huán)簡圖(X為H2CO3,Y為C6H12O6)。下列說法錯誤的是( )
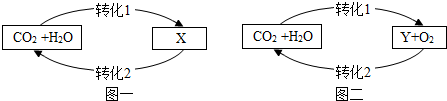
A.圖一中X溶液顯酸性,是形成酸雨的主要原因 B.圖二轉(zhuǎn)化1為二氧化碳和水在光照和葉綠體的作用下轉(zhuǎn)化為葡萄糖(C6H12O6)和氧氣 C.圖一、圖二對比說明,反應物相同,反應條件不同,產(chǎn)物不同 D.碳循環(huán)和氧循環(huán)有利于維持大氣中二氧化碳和氧氣含量的相對穩(wěn)定 組卷:23引用:1難度:0.6
二、填空題(本題包括6個小題,每空1分,共16分)
-
15.請從Fe、KMnO4、O2、H2、H2O2、H2O、MnO2中選擇適當?shù)奈镔|(zhì),按要求寫出化學方程式。
(1)化合反應(產(chǎn)物常溫下呈液態(tài)):。
(2)分解反應(產(chǎn)物有三種):。
(3)實驗室用一種液體制取氧氣:。
(4)火星四射的反應:。
(5)產(chǎn)生兩種氣體的反應:。組卷:44引用:1難度:0.5 -
16.2017年3月27日,疏勒河、黨河時隔六十余年后,“再次重逢會流”,干涸半個多世紀的敦煌哈拉湖也重現(xiàn)碧波,煥發(fā)生機。
(1)要想知道哈拉湖水是否為硬水,可使用檢測。生活中經(jīng)常使用的方法降低水的硬度。
(2)凈化水時,常用到活性炭,其主要作用是。
(3)哈拉湖水變成水蒸氣的過程中,不發(fā)生變化的是(填字母代號)。
A.分子質(zhì)量
B.分子種類
C.分子間隔組卷:74引用:4難度:0.7 -
17.寫出下列反應的化學方程式,并注明反應類型:
(1)鎂帶在空氣中燃燒,反應。
(2)電解水,反應。
(3)氫氣在空氣中燃燒,反應。
(4)加熱銅粉,反應。組卷:6引用:2難度:0.6 -
18.按核電荷數(shù)的增加,依一定規(guī)律將1~18號元素的原子結(jié)構(gòu)示意圖排列成如圖形狀.據(jù)圖填空:
(1)在化學反應中,第一縱行的原子比較容易電子;第六縱行、第七縱行的原子比較容易電子,大部分元素(除H外)都通常達到8個電子的穩(wěn)定結(jié)構(gòu),可見元素的化學性質(zhì)主要決定于原子的數(shù).
(2)從原子結(jié)構(gòu)方面看:同一橫行的原子具有相同的數(shù);同一縱行的原子具有相同的數(shù).
(3)在圖中,和Ne原子核外電子排布相同的兩種陰離子分別為和,3種陽離子的離子符號是、、.組卷:21引用:2難度:0.3 -
 19.如圖是甲、乙、丙三種固體物質(zhì)(均不含結(jié)晶水)的溶解度曲線.
19.如圖是甲、乙、丙三種固體物質(zhì)(均不含結(jié)晶水)的溶解度曲線.
①t1℃時,甲、乙、丙三種物質(zhì)的溶解度大小關(guān)系.
②t1℃時,完全溶解5g丙物質(zhì)至少需要水g.
③t2℃時,將20g甲加入到100g水中,充分攪拌后所得溶液是甲的溶液(填“飽和”或“不飽和”),可以用圖中點(填“a”、“b”、“c”)表示.
④甲溶液中含有少量乙時,可通過的方法提純甲.
⑤將甲、乙的飽和溶液從t2℃降溫到t1℃,對所得溶液的敘述正確的是.
A.都是飽和溶液 B.溶劑質(zhì)量:甲<乙
C.析出固體質(zhì)量:甲>乙 D.溶質(zhì)質(zhì)量分數(shù):甲<乙.組卷:96引用:3難度:0.3 -
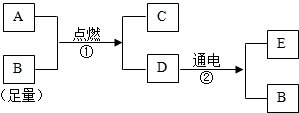 20.圖中A-E是初中化學常見的物質(zhì)已知A和E都可以作燃料,其中A是天然氣的主要成分,請分析回答:
20.圖中A-E是初中化學常見的物質(zhì)已知A和E都可以作燃料,其中A是天然氣的主要成分,請分析回答:
(1)反應①的化學方程式為。
(2)反應②中的產(chǎn)物B通常用檢驗。
(3)E物質(zhì)作燃料的優(yōu)點是(答一條即可)。組卷:4引用:2難度:0.5
三、簡答題(本題包括4個小題,共10分)
-
21.流感發(fā)生時,可用醋對室內(nèi)空氣進行消毒,為了迅速增加室內(nèi)空氣中醋的含量,常采用給醋加熱的方法.
(1)通過對上述事例的分析,關(guān)于溫度與分子運動速率的關(guān)系你能得出什么結(jié)論?
(2)請你從生活或生產(chǎn)實際中,再舉出一個符合上述結(jié)論的事例.組卷:81引用:10難度:0.7 -
22.空氣是寶貴的自然資源。
一、如圖是以空氣等為原料合成尿素【CO(NH2)2】的流程(部分產(chǎn)物略去)。請分析流程并按要求回答相關(guān)問題: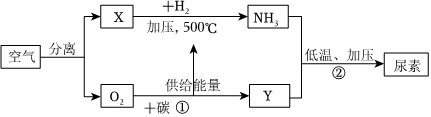
(1)X是空氣中含量最多的氣體,其名稱是,Y是導致“溫室效應”的主要氣體,其化學式是。
(2)分離空氣常用方法有以下兩種。
Ⅰ、分離液態(tài)空氣法:液態(tài)空氣氣化時首先分離出氮氣,并得到色的液態(tài)氧氣,此過程發(fā)生的是(填“物理”或“化學)變化。
Ⅱ、用分子篩分離:分子篩是一種內(nèi)部分布有均勻微小孔徑的固體,通過特制的分子篩把空氣中的氧分子吸入孔穴而與其它分子分離,則分子大小:氮氣氧氣(選填“>”“=”、“<”)。
(3)化學反應①的符號表達式為,該反應基本反應類型是(填“化合”、“分解”)反應。
(4)反應②是NH3(氨氣)與Y在低溫加壓條件下生成尿素的同時還生成水,寫出其反應的符號表達式。
二、從空氣中獲得氮氣,進行氨氣的合成,氨氣是一種重要的化學物質(zhì),可用于制造硝酸和氮肥。工業(yè)合成氨氣的流程如圖1所示,在鐵觸媒作用下,用體積比為1:3的氮氣和氫氣合成氨氣,當容器中氨的含量不再發(fā)生變化時(平衡時),測得氨氣的含量分別與溫度和壓強的關(guān)系如圖2所示。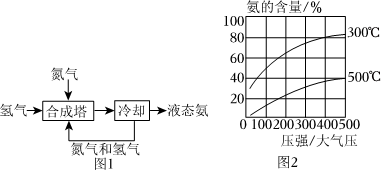
(1)N2是合成氨氣的重要原料。工業(yè)上可從空氣中獲得N2,該方法是利用空氣中各成分的不同將空氣成分進行分離。
(2)從“合成塔”中出來的氣體是(填“純凈物”或“混合物”)。
(3)按下列條件進行合成氨氣反應,平衡時氨氣的含量最高的是(填字母序號)。
A.200大氣壓、300℃
B.200大氣壓、500℃
C.400大氣壓、300℃
D.400大氣壓、500℃組卷:25引用:1難度:0.5 -
23.金屬資源在生產(chǎn)生活中應用十分廣泛,回答下列問題。

(1)“共享單車”方便市民出行,頗受人們的喜愛。
①如圖所示,單車上標示出的部件中由金屬材料制成的是(填字母序號)。
②廢舊單車中金屬部件回收再利用的意義是(寫一點即可)。
(2)某興趣小組的同學設計了如圖實驗方案對廢水進行處理,從中回收金屬銅和硫酸亞鐵晶體,回答下列問題: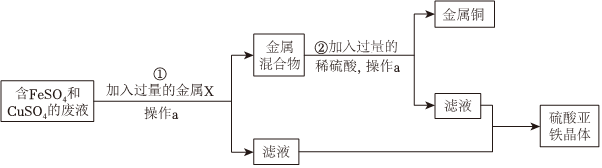
步驟①中,金屬X是,操作a的名稱是,步驟②中,加入過量稀硫酸的目的是。組卷:33引用:2難度:0.5 -
24.如圖是實驗室制取氣體的裝置,請回答下列問題。

(1)儀器①的名稱是。
(2)若用圖A裝置制取氧氣,則發(fā)生反應的化學方程式為,收集氧氣的裝置可選擇E或(填字母),若用A、E制備并收集一瓶氧氣完畢,后續(xù)操作的正確順序是。
①熄滅酒精燈
②將導管從水槽中移出
③將集滿氧氣的集氣瓶在水下蓋好玻璃片,取出后正放在實驗臺上
(3)實驗室制取二氧化碳可選擇的發(fā)生裝置是(填字母),若用D裝置收集二氧化碳,其驗滿方法是。組卷:10引用:1難度:0.6
四、綜合應用題(共10分)
-
25.學習了酸堿鹽的知識后,化學小組通過探究活動進一步理解復分解反應的實質(zhì)。
(1)查閱資料:
一定體積的溶液中,離子的數(shù)目越多,其離子的濃度越大。電導率傳感器用于測量溶液的導電性強弱,能反映離子濃度大小。相同溫度下,同種溶液電導率越大,離子濃度越大。
(2)設計實驗:
實驗一:恒溫條件下,向100mL一定濃度的稀Ba(OH)2溶液中滴加2-3滴無色酚酞試液,再逐滴滴入稀H2SO4溶液,測得溶液的電導率變化如圖1曲線所示。
①寫出反應的化學方程式:
②溶液電導率在b點時幾乎為0,原因是什么?
實驗二:恒溫條件下,向100mL一定濃度的稀Ba(OH)2溶液中滴加2-3滴無色酚酞試液,再逐滴滴入稀Na2SO4溶液,測得溶液的電導率變化如圖2曲線所示。
③通過對圖2曲線的分析,下列說法錯誤的是(填序號)。
A.實驗過程中,溶液由紅色變?yōu)闊o色
B.實驗過程中,溶液中Na+濃度逐漸增加
C.實驗過程中,m~n段電導率降低是由于反應生成了沉淀
D.n點時溶液電導率仍然較大,表明溶液中還存在較多離子
④圖2中的q點時,溶液中含有的離子是(填離子符號)。
(3)得出結(jié)論:
通過比較分析,結(jié)合已學知識可知,復分解反應的實質(zhì)是:參與反應的離子結(jié)合生成了沉淀、氣體或水,導致溶液中離子濃度(填“增大”、“減小”或“不變”)。
(4)拓展反思:
①恒溫條件下,向100mL同濃度的稀Ba(OH)2溶液中滴加稀CuSO4溶液,請你預測,溶液的電導率變化與(填“圖1”或“圖2”)的曲線更接近。
②如圖是向NaOH溶液中逐滴滴加稀鹽酸過程中,不同時間點燒杯中的微觀粒子示意圖,按時間先后排列的順序為(填字母序號)。
(5)某工廠利用熟石灰和純堿反應制備氫氧化鈉,試計算:制備10噸氫氧化鈉固體,至少需要含雜質(zhì)為7.5%的熟石灰是多少噸?組卷:70引用:2難度:0.5


