2019-2020學年廣東省汕頭市潮南區司馬浦鎮九年級(上)期末化學試卷
發布:2025/7/4 20:0:18
一、選擇題.(15小題,共45分)
-
1.貧血的人在平時的飲食中需注意鐵的攝入,這里的“鐵”是指( )
A.分子 B.原子 C.單質 D.元素 組卷:203引用:7難度:0.7 -
2.下列四個圖像中,不能正確反映對應變化關系的是( )
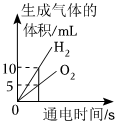
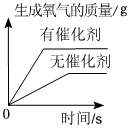
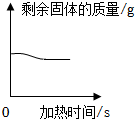
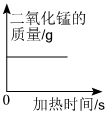
A.通電電解水 B.用等量等濃度的雙氧水制取O2 C.加熱一定質量的高錳酸鉀固體 D.加熱一定質量的氯酸鉀和二氧化錳混合固體 A.A B.B C.C D.D 組卷:24引用:2難度:0.5 -
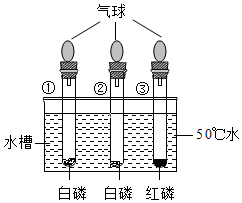 3.如圖實驗探究物質的燃燒條件。試管①充滿N2,試管②、③充滿空氣,同時放入水中,觀察到只有試管②中有白煙產生。下列說法錯誤的是( )
3.如圖實驗探究物質的燃燒條件。試管①充滿N2,試管②、③充滿空氣,同時放入水中,觀察到只有試管②中有白煙產生。下列說法錯誤的是( )A.對比①和②可說明氮氣不支持白磷燃燒① B.對比②和③可說明白磷的著火點低于紅磷 C.對比①和③可說明可燃物燃燒需要與氧氣接觸 D.氣球的作用是緩沖氣壓和防止燃燒產物污染環境 組卷:567引用:9難度:0.8 -
 4.如圖所示為簡易凈水器,其中可吸附雜質、除去臭味的是( )
4.如圖所示為簡易凈水器,其中可吸附雜質、除去臭味的是( )A.小卵石 B.石英砂 C.活性炭 D.蓬松棉 組卷:191引用:6難度:0.6 -
5.下列說法中,正確的是( )
A.只含一種元素的物質一定為純凈物 B.金剛石和石墨是由不同種元素組成的 C.金剛石和石墨都是黑色晶體 D.金剛石和石墨的化學性質基本相同 組卷:9引用:2難度:0.9 -
6.集氣瓶裝滿某氣體,可能是下列氣體中的某一種:①氧氣 ②空氣 ③氮氣,將燃著的木條伸入瓶中,火焰立即熄滅,則該瓶氣體是( )
A.① B.② C.②或③ D.③ 組卷:20引用:2難度:0.9 -
7.下列屬于緩慢氧化的是( )
A.爆炸 B.鐵生銹 C.紙燃燒 D.水結冰 組卷:9引用:2難度:0.8 -
8.生活中用到的下列物質,屬于純凈物的是( )
A.調味用的食醋 B.取暖用的煤炭 C.“千足金”飾品中的金 D.炒菜用的鐵鍋 組卷:53引用:4難度:0.9 -
9.已知X和Y元素的原子序數分別為7和18,下列關于X和Y的說法正確的是( )
A.X在化學反應中易得電子 B.X原子的最外層電子數是7 C.Y原子可得到一個電子形成Y- D.X是氮元素,Y是氖元素 組卷:28引用:8難度:0.6 -
10.無色透明普通玻璃,其主要成分又稱為鈉鈣玻璃,化學式為Na2CaSi6O14,其中硅元素的化合價為( )
A.+4 B.+3 C.+2 D.+1 組卷:3引用:1難度:0.7 -
11.下列現象屬于化學變化的是( )
A.鋼鐵在潮濕的空氣里生銹 B.電燈泡通電時發熱,發光 C.把塊狀的石灰石粉碎成粉末 D.水在加熱時有小氣泡產生 組卷:25引用:7難度:0.9 -
12.下列實驗操作或記錄正確的是( )
A.用10 mL量筒量取了8.65 mL的水 B.把氯化鈉固體直接放在天平的托盤上稱量 C.用漏斗向酒精燈里添加酒精 D.實驗時未經洗凈的滴管可直接再吸取別的試劑 組卷:39引用:13難度:0.9 -
13.在一密閉容器內加入甲、乙、丙、丁四種物質,在一定條件下發生化學反應,反應前后各物質的質量變化如圖所示。下列說法不正確的是( )

A.該反應為分解反應 B.丙可能為該反應的催化劑 C.參加反應的乙與生成的丁的質量比為3:2 D.乙的相對分子質量是甲的3倍 組卷:22引用:4難度:0.6 -
14.化學反應依據不同的分類標準可分為不同類型。反應前后有元素化合價變化的化學反應是氧化還原反應。酸雨形成的原因主要有兩種:①3NO2+H2O═2HNO3+X ②2SO2+O2+2H2O
2H2SO4,下列說法不正確的是( )粉塵A.反應①中X的化學式為NO B.反應①、②都屬于氧化還原反應 C.化石燃料的燃燒是導致酸雨的“罪魁” D.反應①、②中涉及的氧化物共有5種 組卷:43引用:3難度:0.5 -
15.在氧氣中完全燃燒2.8g某物質,生成8.8g二氧化碳和3.6g水,該物質的化學式可能是( )
A.CH4 B.C2H4 C.CH4O D.C2H4O 組卷:123引用:3難度:0.4
二、填空題.(15分)
-
16.結合如圖回答下列問題
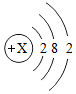
(1)鎂離子的符號是;
(2)X的值為;
(3)鎂元素位于元素周期表中第周期;
(4)鎂元素在化合物中通常顯示的化合價為價。組卷:25引用:1難度:0.7 -
17.將太湖水轉變為飲用水的過程示意圖如圖:

(1)“活性炭”的作用是。
(2)經過超濾膜后得到的飲用水屬于(填”混合物”或”純凈物”)。
(3)檢驗凈化后的水是軟水,常用的試劑是。
(4)下列圖標表示“國家節水標志”的是(填序號)。 組卷:23引用:4難度:0.6
組卷:23引用:4難度:0.6
三、實驗題.(20分)
-
18.學習了氧氣和二氧化碳的實驗室制法之后,老師布置了“實驗室制取乙炔”的任務,檢驗同學們的學習效果。
已知:
1.在常溫下,塊狀固體碳化鈣(CaC2)與水反應生成乙炔氣體,乙炔是一種無色、無味、無毒的氣體,密度比空氣略小,微溶于水,易燃燒。
2.碳化鈣(CaC2)與水反應非常劇烈,容易暴沸。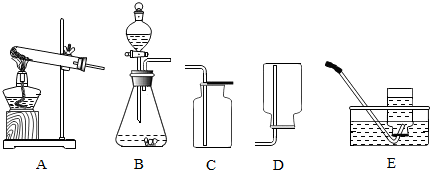
(1)制取乙炔的發生裝置是(填序號,下同),收集裝置。
(2)做乙炔性質實驗前,必須先。
(3)已知CaC2+2H2O=Ca(OH)2+(乙炔)↑,請將空格內乙炔的化學式寫出來。
(4)為了防止反應過程中的“暴沸”現象,你采取的措施是。組卷:8引用:2難度:0.7 -
19.20℃時,將鎂條放入飽和(溶質質量分數約為17.7%)的Na2CO3溶液中,觀察到持續產生較多氣泡,且有白色沉淀生成。實驗小組對其進行探究。
【查閱資料】①鎂能與水緩慢反應生成氫氣。
②Na2CO3、K2CO3溶液均顯堿性,其溶液中除金屬離子、CO32-外,還有OH-。
實驗1:探究反應產生的氣體
【猜想與假設】
Ⅰ.氣體是H2
Ⅱ.氣體是CO2
Ⅲ.氣體是H2和CO2
【進行實驗】取適量鎂條、100mL飽和Na2CO3溶液,按如圖所示方案進行實驗。
實驗2:探究持續產生較多氣體的原因編號 1-1 1-2 裝置 
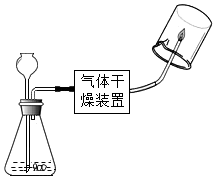
實驗現象 澄清石灰水 氣體被點燃,燒杯內壁有小液滴生成
【猜想與假設】Na2CO3溶液中的某一種離子促進了鎂與水的反應,從而產生較多氣體。
【進行實驗】20℃時,利用圖示裝置分別完成下列實驗,記錄如下:
【解釋與結論】裝置 編號 實驗操作 實驗現象 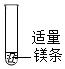
2-1 向試管中加入2mL 17.7%的Na2CO3溶液 持續產生較多氣泡 2-2 向試管中加入2mL 1%的Na2CO3溶液 有少量氣泡 2-3 向試管中加入2mL 17.7%的K2CO3溶液 持續產生較多氣泡 2-4 向試管中加入2mL 17.7%的X溶液 無明顯現象 2-5 向試管中加入2mL 1%的X溶液 無明顯現象
(1)依據實驗1-1、1-2的現象,可得出猜想Ⅰ正確。
①補全實驗1-1的現象。
②實驗1-2中有小液滴生成的原因是(用化學方程式解釋)。
(2)實驗2-4、2-5中加入的X是。
(3)得出“Na2CO3溶液濃度越大,反應更劇烈”的結論,依據的實驗是(填編號)。
(4)實驗2的結論是。
【反思與評價】
(5)欲進一步檢驗反應產生的白色沉淀中是否含有碳酸鹽,所需試劑是。組卷:98引用:4難度:0.5
四、綜合能力題.(10分)
-
20.圖中A~I表示初中化學常見的物質,其中A、C、E、F為單質,其余均為氧化物。B中兩種元素的原子個數之比為2:5;D的相對分子質量為40;F在空氣中燃燒時產生淡藍色火焰。圖中“—”表示兩端的物質間能發生化學反應;“→”表示物質間存在轉化關系;部分反應物生成物和反應條件已略去:
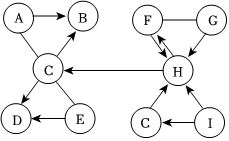
(1)G的顏色是色。
(2)寫出下列反應的化學方程式。
①A→B:。
②C與E:。
③H→F:。組卷:70引用:1難度:0.5
五、計算題.(10分)
-
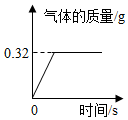 21.過氧化鈉(Na2O2)能與二氧化碳反應產生氧氣,因此可用于呼吸面具或潛水艇中作為氧氣的來源。現有2g過氧化鈉樣品(雜質不參加反應),與一定量的二氧化碳完全反應,生成氣體質量與時間的關系如圖所示,發生反應的化學方程式為2Na2O3+2CO2═2Na2CO3+O2。請計算:
21.過氧化鈉(Na2O2)能與二氧化碳反應產生氧氣,因此可用于呼吸面具或潛水艇中作為氧氣的來源。現有2g過氧化鈉樣品(雜質不參加反應),與一定量的二氧化碳完全反應,生成氣體質量與時間的關系如圖所示,發生反應的化學方程式為2Na2O3+2CO2═2Na2CO3+O2。請計算:
(1)生成氧氣的質量是g。
(2)樣品中過氧化鈉的質量。組卷:12引用:1難度:0.5


