2021-2022學年河南省開封市蘭考縣第二高級中學高二(上)期中化學試卷
發布:2024/11/16 16:30:6
一、單項選擇題(每題3分16小題共48分)
-
1.下列物質的水溶液中,除了水分子外,不存在其他分子的是( )
A.NaHSO4 B.CH3COONH4 C.H2S D.NH3?H2O 組卷:6引用:2難度:0.7 -
2.改變下列條件,只對化學反應速率有影響,一定對化學平衡沒有影響的是( )
A.催化劑 B.濃度 C.壓強 D.溫度 組卷:44引用:3難度:0.7 -
3.最新報道:科學家首次用X射線激光技術觀察到CO與O在催化劑表面形成化學鍵的過程.反應過程的示意圖如下:
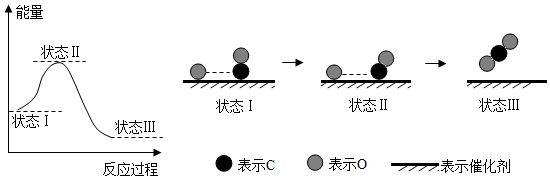
下列說法正確的是( )A.CO和O生成CO2是吸熱反應 B.在該過程中,CO斷鍵形成C和O C.狀態Ⅰ→狀態Ⅲ表示CO與O2反應的過程 D.CO和O生成了具有極性共價鍵的CO2 組卷:523引用:8難度:0.9 -
 4.由N2O和NO反應生成N2和NO2的能量變化如圖所示。下列說法不正確的是( )
4.由N2O和NO反應生成N2和NO2的能量變化如圖所示。下列說法不正確的是( )A.反應生成1molN2時轉移2mole- B.反應物的總能量大于生成物的總能量 C.N2O(g)+NO(g)═N2(g)+NO2(g) ΔH=-139kJ?mol-1 D.斷鍵吸收的總能量大于成鍵釋放的總能量 組卷:5引用:2難度:0.8 -
5.下列關于電離平衡常數(K)的說法中正確的是( )
A.電離平衡常數(K)越小,表示弱電解質電離能力越弱 B.電離平衡常數(K)與溫度無關 C.相同溫度下,不同濃度的同一弱電解質,其電離平衡常數(K)不同 D.多元弱酸各步電離平衡常數相互關系為K1<K2<K3 組卷:25引用:1難度:0.5 -
6.已知:H2(g)+F2(g)═2HF(g) 的能量變化如圖所示,下列有關敘述中正確的是( )

A.氟化氫氣體分解生成氫氣和氟氣的反應是放熱反應 B.1 mol H2與1 mol F2反應生成2 mol液態HF放出的熱量小于270 kJ C.在相同條件下,1 mol H2與1 mol F2的能量總和大于2 mol HF氣體的能量 D.斷裂1 mol H-H鍵和1 mol F-F 鍵放出的能量大于形成2 mol H-F鍵放出的能量 組卷:67引用:12難度:0.9 -
7.如圖是恒溫下某化學反應的反應速率隨反應時間變化的示意圖.下列敘述與示意圖不相符合的是( )

A.反應達平衡時,正反應速率和逆反應速率相等 B.該反應達到平衡狀態Ⅰ后,增大反應物濃度,平衡發生移動,達到平衡狀態Ⅱ C.該反應達到平衡狀態Ⅰ后,減小反應物濃度,平衡發生移動,達到平衡狀態Ⅱ D.同一種反應物在平衡狀態Ⅰ和平衡狀態Ⅱ時濃度不相等 組卷:438引用:47難度:0.7
二、非選擇題(52分)
-
22.某氮肥廠氨氮廢水中的氮元素多以NH4+和NH3?H2O 的形式存在,該廢水的處理流程中,NH4+在微生物的作用條件下經過兩步反應被氧化成NO3-.兩步反應的能量變化示意圖如下:

1molNH4+(aq)全部氧化成NO3-(aq)的熱化學方程式是。組卷:19引用:4難度:0.7 -
23.氨是一種重要的化工產品,是氮肥工業、有機合成工業以及制造硝酸、銨鹽和純堿等的原料。
(1)在一定溫度下,在固定體積的密閉容器中進行可逆反應:N2+3H2?2NH3.該可逆反應達到平衡的標志是。
A.3v(H2)正=2v(NH3)逆
B.單位時間生成m mol N2的同時消耗3m mol H2
C.容器內的總壓強不再隨時間而變化
D.混合氣體的密度不再隨時間變化
E.a molN≡N鍵斷裂的同時,有6amolN-H鍵斷裂
F.N2、H2、NH3的分子數之比為1:3:2
(2)某化學研究性學習小組模擬工業合成氨的反應。在容積固定為2L的密閉容器內充入1molN2和3molH2,加入合適催化劑(體積可以忽略不計)后在一定溫度壓強下開始反應,并用壓力計監測容器內壓強的變化如表:
則從反應開始到25min時,以N2表示的平均反應速率=反應時間/min 0 5 10 15 20 25 30 壓強/MPa 16.80 14.78 13.86 13.27 12.85 12.60 12.60 ;該溫度下平衡常數K=;
(3)利用合成氣(主要成分為CO、CO2和H2)在催化劑的作用下合成甲醇,主要反應如下:
①CO(g)+2H2(g)?CH3OH(g)△H=-99kJ?mol-1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-58kJ?mol-1
③CO2(g)+H2(g)?CO(g)+H2O(g)△H
圖1中能正確反映平衡常數K隨溫度變化關系的曲線是;反應③的△H=kJ?mol-1。
(4)合成氣的組成n(H2)/n(CO+CO2)=2.60時體系中的CO平衡轉化率α(CO)與溫度和壓強的關系如圖2所示。圖中的壓強p1、p2、p3由大到小的順序為;α(CO)隨溫度升高而減小,其原因是。組卷:5引用:3難度:0.4


