2021-2022學年江蘇省無錫市惠山區陽山中學九年級(下)月考化學試卷(3月份)
發布:2024/4/20 14:35:0
一、單項選擇題。(每小題只有一個選項符合題意)
-
1.我國第十四個五年規劃和2035年遠景目標綱要第十一篇是《推動綠色發展,促進人與自然和諧共生》。下列有利于實現該目標的是( )
A.大量使用化肥,增加農作物收成 B.參與植樹造林,擴大植被面積 C.大量使用一次性餐盒,保證飲食衛生 D.大力發展火力發電,滿足用電需求 組卷:157引用:11難度:0.7 -
2.下列歷史典故中發生了化學變化的是( )
A.火燒赤壁 B.司馬光砸缸 C.刻舟求劍 D.鐵杵磨成針 組卷:480引用:85難度:0.8 -
3.下列關于空氣成分的說法不正確的是( )
A.氮氣充入食品包裝中以防腐 B.稀有氣體可制成多種用途的電光源,如霓虹燈 C.氧氣約占空氣總體積的 45D.二氧化碳在大氣中含量上升,導致溫室效應增強 組卷:6引用:1難度:0.7 -
4.表格的四種食物的近似pH,你認為胃酸過多的患者不宜多吃的食物是( )
食物 蘋果汁 豆漿 玉米粥 雞蛋清 pH 2.9~3.3 7.4~7.9 6.8~8.0 7.6~8.0 A.蘋果汁 B.豆漿 C.玉米粥 D.雞蛋清 組卷:601引用:34難度:0.6 -
5.化學與我們的生活密切相關。下列有關說法不正確的是( )
A.如果人體缺乏維生素C,會引起壞血病 B.如果人體缺乏碘元素,會導致甲狀腺腫大 C.醬油中加入鐵元素,可以預防缺鐵性貧血 D.可用甲醛溶液浸泡海產品,以延長保質期 組卷:2引用:1難度:0.7 -
6.下列有關燃燒與滅火的說法正確的是( )
A.為防止森林大火蔓延可開挖隔離帶,其目的是隔絕可燃物 B.房屋失火,消防隊員用水撲滅是因為降低了可燃物的著火點 C.汽油放置在空氣中沒有燃燒是因為汽油不是可燃物 D.用燈帽蓋滅酒精燈是因為降低了可燃物的溫度 組卷:188引用:72難度:0.9 -
 7.磷元素對生命活動有重要意義,其相關信息如圖所示。下列有關磷元素的說法正確的是( )
7.磷元素對生命活動有重要意義,其相關信息如圖所示。下列有關磷元素的說法正確的是( )A.是農作物必需的營養元素 B.相對原子質量為30.97g C.原子核外有16個電子 D.屬于金屬元素 組卷:33引用:2難度:0.6 -
8.如圖所示實驗操作正確的是( )
A. 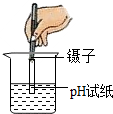
測溶液的pHB. 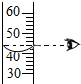
讀出液體體積C. 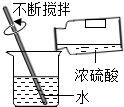
稀釋濃硫酸D. 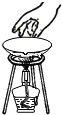
移走蒸發皿組卷:124引用:21難度:0.7 -
9.自來水廠凈水過程如圖所示。下列說法正確的是( )
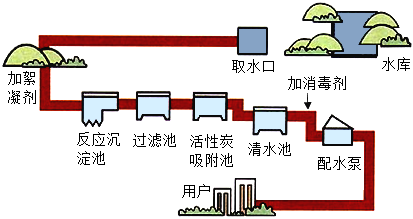
A.經過濾池,水中雜質離子都已經除去 B.吸附池中的活性炭可長期使用,無需更換 C.加消毒劑是為了殺死水中的細菌 D.經該凈水過程,用戶得到的是純水 組卷:300引用:5難度:0.7
二、解答題(共8小題,滿分40分)
-
27.訂書釘是生活中常用的文具,主要成分是鐵,其表面鍍有鎂、鋅、銅中的一種,為探究是哪種金屬,進行以下實驗:
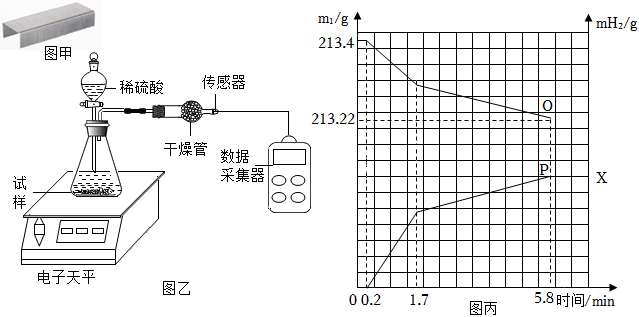
【實驗步驟】
①取一塊訂書釘(40根釘),如圖甲所示,浸入95%酒精中,一段時間后從表面取下一層膠水薄膜;
②用棉花擦去酒精,待干燥后稱量質量為13.4g;
③將其放入圖乙所示裝置,并在干燥管口用氫氣傳感器測量氫氣的質量,同時記錄電子天平顯示的質量變化(如圖丙所示);
④5.8min時停止反應取出裝置剩余訂書釘,洗滌、干燥、稱量、剩余訂書釘質量為7.8g。
根據實驗操作,分析實驗數據,請回答:
(1)步驟1中使用的95%酒精屬于(填“純凈物”或“混合物”)。
(2)從訂書釘的外觀看,可以首先排除的金屬是。
(3)圖丙中,表示電子天平讀數的曲線是點所在的曲線(填“O”或“P”),P點縱坐標X的值為。
(4)0~0.2min不產生氫氣的原因主要是。
(5)1.7min后錐形瓶中發生的主要反應的化學方程式為。
(6)通過所給數據分析,訂書釘表面鍍的金屬是(填化學式)。
(7)金屬鋁也是生活中常用的金屬材料,化學興趣小組的同學把用砂紙打磨過的鋁片迅速放入氣密性良好的軟塑料瓶中,利用氧氣濃度傳感器測得瓶內氧氣含量的變化情況如圖所示。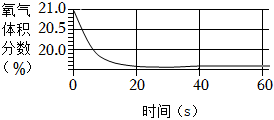
請說明實驗過程中瓶內氧氣含量先減少后基本不變的原因。組卷:26引用:1難度:0.7 -
28.碳酸氫鈉(NaHCO3))是一種重要的化工原料。某化學興趣小組同學對碳酸氫鈉的性質進行探究。
【查閱資料】
①2%碳酸氫鈉的溶解度如下:
②碳酸氫鈉固體在潮濕的空氣中久置或受熱分解均生成Na2CO3、H2O和CO2。溫度 10℃ 20℃ 30℃ 40℃ 溶解度 8.1g 9.6g 11.1g 12.7g
【實驗探究】
探究1:NaHCO3溶液與鹽酸反應的熱效應
室溫下(20℃),邊攪拌邊向盛有0.5gNaHCO3固體的燒杯中加入10mL水,測得溫度為18.5℃;恢復至室溫后,向燒杯中加入過量10mL質量分數為20%的鹽酸(20℃),攪拌,測得溫度為20.8℃。
(1)實驗中配制的NaHCO3溶液(填“是”或“不是”)飽和溶液。
(2)由上述實驗可知:NaHCO3固體溶于水(填“放熱”或“吸熱”)。
探究2:NaHCO3溶液與CaCl2溶液的反應
分別向10mL0.5%和5%NaHCO3溶液中滴加10%的CaCl2溶液,發現均有白色渾濁出現,通過傳感器測得CO2濃度與時間的關系如圖-1、2所示。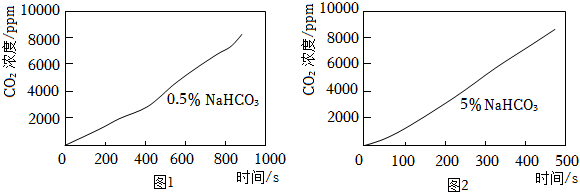
(3)若用5%NaHCO3溶液配制100g0.5%NaHCO3溶液,需要5%NaHCO3的質量為。
(4)由如圖得出的實驗結論是。
(5)該條件下,NaHCO3溶液和CaCl2溶液反應的化學方程式為:2NaHCO3+CaCl2═2NaCl++H2O。
探究3:久置的NaHCO3樣品中NaHCO3含量的測定
將一瓶在潮濕空氣中久置的NaHCO3樣品(假設只有NaHCO3和Na2CO3)混合均勻后,稱取19.0g混合物,加熱至恒重,稱其質量為15.9g。
(6)①計算樣品中NaHCO3的質量分數(寫出計算過程,結果精確至0.01%)。
②若上述測定過程中未加熱至恒重,則測得NaHCO3的質量分數將(填“偏大”、“偏小”或“無影響”)。組卷:35引用:1難度:0.6


