2021-2022學年山東省濟南市萊蕪四中高二(上)第一次質檢化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共10小題,每小題3分。每小題只有一個選項符合題意
-
1.已知有如下反應,H-H、O=O和O-H鍵的鍵能分別為436 kJ?mol-1、496 kJ?mol-1和462 kJ?mol-1,則a為( )
C(s)+H2O(g)═CO(g)+H2(g) ΔH=akJ?mol-1
2C(s)+O2(g)═2CO(g) ΔH=-220kJ?mol-1A.+130 B.+118 C.+350 D.+332 組卷:112引用:1難度:0.7 -
2.已知熱化學方程式 N 2 (g)+3H 2 (g)?2NH 3 (g)ΔH=-Q kJ?mol-1 (Q>0),下列說法中正確的是( )
A.1molN2 (g)和3molH2 (g)具有的能量之和低于2molNH3 (g)具有的能量 B.將一定量 N2(g)和 H2(g)置于某密閉容器中充分反應后放出熱量QkJ,則此過程中有3molH 2 被氧化 C.擴大體積,平衡向逆反應方向移動,上述熱化學方程式中的Q值減小 D.將1molN2(g)和 3molH2(g)置于一密閉容器中充分反應后放出QkJ的熱量 組卷:1引用:2難度:0.7 -
3.下列有關金屬腐蝕與防護的說法正確的是( )
A.純銀器表面在空氣中因電化學腐蝕漸漸變暗 B.當鍍錫鐵制品的鍍層破損時,鍍層仍能對鐵制品起保護作用 C.在海輪外殼連接鋅塊保護外殼不受腐蝕是采用了犧牲陽極的陰極保護法 D.可將地下輸油鋼管與外加直流電源的正極相連以保護它不受腐蝕 組卷:462引用:93難度:0.7 -
4.在一密閉容器中反應aA(g)?bB(g)達平衡后,測得c(B)為1mol/L。如保持溫度不變,將容器體積變為原來的2倍,重新達到新的平衡時,c(B)變為0.4mol/L,則下列說法正確的是( )
A.平衡向正反應方向移動 B.物質A的轉化率增大 C.物質B的質量分數增大 D.a>b 組卷:23引用:2難度:0.8 -
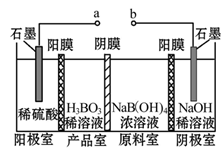 5.硼酸( H3BO3) 為一元弱酸,H3BO3可以通過電解的方法制備。其工作原理如圖所示(陽膜和陰膜分別只允許陽離子、陰離子通過)。下列說法錯誤的是( )
5.硼酸( H3BO3) 為一元弱酸,H3BO3可以通過電解的方法制備。其工作原理如圖所示(陽膜和陰膜分別只允許陽離子、陰離子通過)。下列說法錯誤的是( )A.a與電源的正極相連接 B.陽極的電極反應式為:2H2O-4e-═O2↑+4H+ C.[B(OH)4]-穿過陰膜進入產品室,Na+穿過陽膜進入陰極室 D.當電路中通過3mol電子時,可得到1molH3BO3 組卷:2引用:1難度:0.5 -
6.關于下列各裝置圖的敘述中,不正確的是( )

A.用裝置①精煉銅,則a極為粗銅,電解質溶液為CuSO4溶液 B.裝置②的總反應是:Cu+2Fe3+=Cu2++2Fe2+ C.裝置③中鋼閘門應與外接電源的負極相連 D.裝置④中的鐵釘幾乎沒被腐蝕 組卷:897引用:81難度:0.5
三、非選擇題:本題共5小題,共50分。
-
19.高鐵電池是一種新型可充電電池,與普通電池相比,該電池能較長時間保持穩定的放電電壓。高鐵電池的總反應式為3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH。充電放電
請回答下列問題:
(1)高鐵電池的負極材料是,放電時負極反應式為。
(2)放電時,正極發生(填“氧化”或“還原”)反應;正極反應式為。放電時,(填“正”或“負”)極附近溶液的堿性增強。
(3)充電時,陽極反應式為,陽極附近溶液的堿性(填“增強”“減弱”或“不變”)。組卷:109引用:4難度:0.6 -
20.(1)氯堿工業上利用電解精制飽和食鹽水的方法制取氯氣、氫氣、燒堿和氯的含氧酸鹽等一系列化工產品。如圖是離子交換膜法電解食鹽水的示意圖,圖1中的離子交換膜只允許陽離子通過。試回答下列問題:
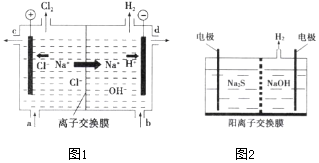
①離子交換膜的作用為、。
②精制飽和食鹽水從圖中( 填“a”、“b”、“c”或“d”,下同)處補充,氫氧化鈉溶液從圖中處收集。
(2)MnO2可作超級電容器材料。用惰性電極電解MnSO4溶液可制得MnO2,其陽極的電極反應式為。
(3)硫化氫的轉化是資源利用和環境保護的重要研究課題之一。將吸收H2S后的燒堿溶液加入如圖2所示的電解池的陽極區進行電解,電解過程中陽極區發生如下反應:S2--2e-═S (n-1)S+S2-═Sn2-
①寫出電解時陰極的電極反應式:。
②用稀硫酸酸化電解后陽極區的溶液可得到硫單質,其離子方程式為。組卷:47引用:2難度:0.5


