2013-2014學年山東省濟寧市微山二中高三(上)化學寒假作業(二)
發布:2024/4/20 14:35:0
一、選擇題
-
1.元素的原子結構決定其性質和周期表中的位置。下列說法正確的是( )
A.元素原子的最外層電子數等于元素的最高化合價 B.多電子原子中,在離核較近的區域內運動的電子的能量較高 C.P、S、Cl得電子能力和最高價氧化物對應水化物的酸性均依次增強 D.元素周期表中位于金屬和非金屬分界線附近的元素屬于過渡元素 組卷:392引用:80難度:0.7 -
2.以下有關原子結構及元素周期律的敘述正確的是( )
A.第IA族元素銫的兩種同位素137Cs比133Cs多4個質子 B.同周期元素(除0族元素外)從左到右,原子半徑逐漸減小 C.第ⅦA族元素從上到下,其氫化物的穩定性逐漸增強 D.同主族元素從上到下,單質的熔點逐漸降低 組卷:330引用:47難度:0.9 -
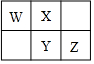 3.W、X、Y、Z四種短周期元素在元素周期表中的相對位置如圖所示,W的氣態氫化物可與其最高價含氧酸反應生成離子化合物,由此可知( )
3.W、X、Y、Z四種短周期元素在元素周期表中的相對位置如圖所示,W的氣態氫化物可與其最高價含氧酸反應生成離子化合物,由此可知( )A.X、Y、Z中最簡單氫化物穩定性最弱的是Y B.Z元素氧化物對應水化物的酸性一定強于Y C.X元素形成的單核陰離子還原性大于Y D.Z元素單質在化學反應中只表現氧化性 組卷:1889引用:60難度:0.9 -
4.下列關于原子結構、元素性質的說法正確的是( )
A.非金屬元素組成的化合物中只含共價鍵 B.ⅠA族金屬元素是同周期中金屬性最強的元素 C.同種元素的原子均有相同的質子數和中子數 D.ⅦA族元素的陰離子還原性越強,其最高價氧化物對應水化物的酸性越強 組卷:398引用:56難度:0.7
二、綜合題
-
11.五種短周期元素A、B、C、D、E的原子序數依次增大,A和C同族,B和D 同族,C離子和B離子具有相同的電子層結構。A和B、D、E均能形成共價型化合物。A和B形成的化合物在水中呈堿性,C和E形成的化合物在水中呈中性。回答下列問題:
(1)五種元素中,原子半徑最大的是,非金屬性最強的是(填元素符號);
(2)由A和B、D、E所形成的共價型化合物中,熱穩定性最差的是(用化學式表示);
(3)A和E形成的化合物與A和B形成的化合物反應,產物的化學式為,其中存在的化學鍵類型為;
(4)D最高價氧化物的水化物的化學式為;
(5)單質D在充足的單質E中燃燒,反應的化學方程式為;D在不充足的E中燃燒,生成的主要產物的化學式為;
(6)單質E與水反應的離子方程式為。組卷:1965引用:32難度:0.5 -
12.A、B、C、D、E五種短周期元素,原子序數E>D>A>B>C,且A、B、D、E同周期,A、C同主族,A的原子結構示意圖如圖,
 B的最外層電子數比K層電子多1,D元素的主族序數是周期序數的2倍,E的單質是黃綠色氣體;據此填空:
B的最外層電子數比K層電子多1,D元素的主族序數是周期序數的2倍,E的單質是黃綠色氣體;據此填空:
(1)指出元素A在周期表中的位置,其氣態氫化物的化學式為.
(2)D和E兩種元素相比較,非金屬性較強的是(填元素符號),
可以驗證該結論的是(填寫字母序號);
A.比較這兩種元素的常見單質的熔沸點 B.比較這兩種元素的氣態氫化物的熔沸點
C.比較這兩種元素的氣態氫化物的穩定性 D.比較這兩種元素置換能力的強弱
(3)C、D、E三種元素最高價氧化物的水化物的酸性由強到弱的順序:.(填寫化學式)組卷:39引用:5難度:0.5


