2022-2023學年安徽省合肥一中高一(下)期中化學試卷
發布:2024/6/4 8:0:5
一、單項選擇題(本大題共16題,每題3分,共48分)
-
1.科學生產中蘊藏著豐富的化學知識。化學改善人類的生活,創造美好的世界。下列生產、生活情境中涉及的原理錯誤的是( )
選項 生產生活情境 原理 A 太陽能電池板被廣泛應用 利用單晶硅的光電性質 B 葡萄酒中通常添加少量SO2 既可以殺菌,又可以防止營養成分被氧化 C 世博停車場安裝催化光解設施,可處理汽車尾氣中CO和NOx NOx和CO發生反應生成無毒氣體 D “明如鏡、聲如磐”的瓷器,可由黏土經高溫燒結而成 主要化學成分是SiO2 A.A B.B C.C D.D 組卷:34引用:1難度:0.7 -
2.設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.標準狀況下,2.24L H2O中含有共價鍵數目為2NA B.Na2O2與水反應時,生成0.1mol O2時轉移的電子數為0.1NA C.過量銅與含0.4mol HNO3的濃硝酸反應,電子轉移數大于0.2NA D.2mol SO2和 1mol O2在一定條件下充分反應后,混合物的分子數為2NA 組卷:52引用:2難度:0.8 -
3.下列有關實驗操作、現象和解釋或結論都正確的是( )
選項 實驗操作 現象 解釋或結論 A 常溫下,Fe、Al分別放入濃H2SO4中 無明顯現象 Fe、Al與濃H2SO4發生鈍化 B 過量的Fe粉中加入稀HNO3,充分反應后,滴入KSCN溶液 溶液呈紅色 稀HNO3將Fe氧化為Fe3+ C 將SO2通入氯化鋇溶液中 出現白色沉淀 SO2與氯化鋇反應生成亞硫酸鋇難溶物 D 用玻璃棒蘸取濃HNO3點到紅色石蕊試紙上 試紙變藍色 濃HNO3具有酸性 A.A B.B C.C D.D 組卷:18引用:2難度:0.6 -
4.下列關于電子式的表述正確的是( )
A.NaClO的電子式為 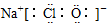
B.SCl2的電子式為: 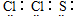
C.用電子式表示HCl的形成過程為: 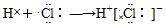
D.已知SCN-中每個原子都達到8電子結構,則其電子式為 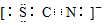 組卷:83引用:7難度:0.9
組卷:83引用:7難度:0.9 -
5.下列表示對應化學反應的離子方程式正確的是( )
A.向FeCl3溶液中通入SO2氣體使溶液淺黃色變淺:SO2+2H2O+2Fe3+=2Fe2++4H++SO42- B.向 Ba(NO3)2溶液中通入SO2氣體出現白色沉淀:Ba2++SO2+H2O=BaSO3↓+2H+ C.在含有等物質的量的Fe(NO3)2和KI的混合溶液中滴入稀鹽酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O D.向Fe(NO3)3溶液中滴入NaHSO3溶液:3SO32-+2NO3-+2H+=3SO42-+2NO↑+H2O 組卷:104引用:2難度:0.7 -
 6.可逆反應mA(g)+nB(g)?pC(g)+gD(g)的v-t圖象如圖甲,若其他條件都不變,只是在反應前加入合適的催化劑,則其v-t圖象如圖乙。
6.可逆反應mA(g)+nB(g)?pC(g)+gD(g)的v-t圖象如圖甲,若其他條件都不變,只是在反應前加入合適的催化劑,則其v-t圖象如圖乙。
①a1=a2
②a1<a2
③b1=b2
④b1<b2
⑤t1>t2
⑥t1=t2
⑦兩圖中陰影部分面積相等
⑧乙圖陰影部分面積更大
以上正確的為( )A.①③⑥⑦ B.①④⑥⑧ C.②③⑤⑧ D.②④⑤⑦ 組卷:89引用:1難度:0.6
二、填空題(本大題共3題,共52分)
-
18.某化學課外興趣小組用如圖所示裝置進行實驗,制備某氣體并驗證其性質。請回答下列問題:

(1)若裝置A中分液漏斗盛裝濃硫酸,圓底燒瓶盛裝銅片。
①裝置A中發生反應的化學方程式為。
②實驗中,取一定質量的銅片和一定體積18mol?L-1的濃硫酸在圓底燒瓶中共熱,直到反應完畢,發現燒瓶中還有銅片剩余,該小組學生根據所學的化學知識認為還有一定量的硫酸剩余。
a.有一定量的余酸但未能使銅片完全溶解,你認為原因是。
b.下列藥品中能用來證明反應結束后的燒瓶中確有余酸的是(填標號)。
A.鐵粉
B.BaCl2溶液
C.銀粉
D.NaHCO3溶液
(2)若裝置A中分液漏斗盛裝濃硫酸,圓底燒瓶盛裝木炭。
①裝置A中發生反應的化學方程式為。
②設計實驗證明裝置C中含有CO2時,所需的試劑有(填標號)。
aNaOH溶液
b.澄清石灰水
c.品紅溶液
d.濃溴水
e.酸性KMnO4溶液
(3)若裝置A中分液漏斗盛裝濃鹽酸,圓底燒瓶盛裝MnO2粉末。
①裝置B的作用是貯存多余的氣體。當D處有明顯的現象后,關閉止水夾K并移去酒精燈,但由于余熱的作用,A處仍有氣體產生,此時B中現象是。
②D中品紅溶液的現象為,加熱試管時溶液的現象為。
(4)裝置D中試管口放置的棉花中浸了一種液體,可適用于(1)(2)(3)小題中實驗,該液體是。組卷:48引用:4難度:0.6 -
19.一定條件下,容積2L的密閉容器中,將2mol/L氣體和1molM氣體混合,發生如下反應:2L(g)+M(g)?aQ(g)+R(s),10s時反應達到平衡,生成0.4molR,測得Q的濃度為0.4mol?L-1。計算:
(1)化學方程式中a的值為。
(2)前10s內用M表示的化學反應速率為,平衡時體系的壓強與反應前的壓強之比為。
(3)一定能使該反應的速率增大的措施有。
A.其他條件不變,及時分離出產物
B.向體系中加入適量R
C.保持溫度不變,將容器的體積壓縮
D.保持壓強不變,充入氣體M
(4)可認定上述可逆反應在一定條件下已達到化學平衡狀態的是(選填序號)。
A.體系壓強不再變化
B.混合氣體的平均相對分子質量不再變化
C.混合氣體的密度不再變化
D.v正(L)=2v逆(M)
E.c(L):c(M):c(Q)=2:1:2
(5)ZulemaBorjas等設計的一種微生物脫鹽池的裝置如圖所示。其中,CH3COO-中C的平均化合價為0價。X為(填寫“陽”或“陰”)離子交換膜,負極反應為。組卷:27引用:1難度:0.6


