2021-2022學年天津一中高一(下)期末化學試卷
發布:2024/12/28 13:30:3
一、選擇題(共48分,每題只有1個正確選項)
-
1.廣東一直是我國對外交流的重要窗口,館藏文物是其歷史見證。下列文物主要由硅酸鹽制成的是( )
文物 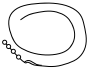



選項 A.南宋鎏金飾品 B.蒜頭紋銀盒 C.廣彩瓷咖啡杯 D.銅鍍金鐘座 A.A B.B C.C D.D 組卷:410引用:2難度:0.7 -
2.我國提出爭取在2030年前實現碳達峰、2060年前實現碳中和,這對于改善環境、實現綠色發展至關重要。“碳中和”是指CO2的排放總量和減少總量相當。下列措施中能促進碳中和最直接有效的是( )
A.將重質油裂解為輕質油作為燃料 B.大規模開采可燃冰作為新能源 C.通過清潔煤技術減少煤燃燒污染 D.研發催化劑將CO2還原為甲醇 組卷:913引用:27難度:0.8 -
3.化學與生活密切相關。下列敘述不正確的是( )
A.可以用熱的堿性溶液洗滌沾有油脂的器皿 B.糯米中的淀粉水解后就釀成了酒 C.用灼燒的方法鑒別人造絲和蠶絲織物 D.“地溝油”不能食用但可以用來制肥皂 組卷:42引用:2難度:0.7 -
4.下列說法正確的是( )
A.電解熔融態的AlCl3冶煉金屬鋁 B.接觸法制硫酸時,煅燒黃鐵礦(含FeS2)得到三氧化硫 C.晶體硅的導電性介于導體和絕緣體之間,常用于制造光導纖維 D.用石灰石-石膏法對燃煤煙氣進行脫硫,同時可得到石膏(CaSO4?2H2O) 組卷:146引用:2難度:0.7 -
5.下列說法不正確的是( )
A.乙醇和乙二醇(CH2OHCH2OH)互為同系物 B.C70和納米碳管互為同素異形體 C.氟利昂的結構式為 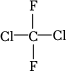 ,它只有1種結構
,它只有1種結構D.丙酮( 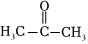 )和環氧丙烷(
)和環氧丙烷(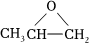 )互為同分異構體組卷:78引用:2難度:0.7
)互為同分異構體組卷:78引用:2難度:0.7 -
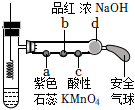 6.若將銅絲插入熱濃硫酸中進行如圖(a~d均為浸有相應試液的棉花)所示的探究實驗,下列敘述正確的是( )
6.若將銅絲插入熱濃硫酸中進行如圖(a~d均為浸有相應試液的棉花)所示的探究實驗,下列敘述正確的是( )A.Cu與濃硫酸反應,只體現H2SO4的酸性 B.a處變紅,說明SO2是酸性氧化物 C.b或c處褪色,均說明SO2具有漂白性 D.冷卻后,將水慢慢加入試管中,觀察到溶液呈藍色 組卷:85引用:3難度:0.7 -
7.電鍍廢液中Cr2
可通過下列反應轉化成鉻黃( PbCrO4):Cr2O2-7(aq)+2Pb2+(aq)+H2O(l)?2PbCrO4(s)+2H+(aq)△H<0。該反應達平衡后,改變條件,下列說法正確的是( )O2-7A.移走部分PbCrO4固體,Cr2 轉化率升高O2-7B.加入少量NaOH固體,自然沉降后,溶液顏色變淺 C.升高溫度,該反應的平衡常數K增大 D.加入少量K2Cr2O7固體后,溶液中c(H+)不變 組卷:76引用:4難度:0.5
二、非選擇題
-
20.高效利用能源并且減少CO2的排放,對完成“碳中和”的目標有重要意義。
Ⅰ、可用下列方法把CO2轉化成甲醇燃料
(1)CO2(g)+3H2(g)?CH3OH(g)+H2O(g) ΔH1=-49.0kJ?mol-1
(2)CO2(g)+H2(g)?CO(g)+H2O(g) ΔH2=+41.1kJ?mol-1
反應(1)在(選填“高溫”、“低溫”或“任意溫度”)下,易自發進行。
Ⅱ、利用CO2與H2合成甲醇涉及的主要反應如下:
a.CO2(g)+3H2(g)?CH3OH(g)+H2O(g) ΔH1
b.CO2(g)+H2(g)?Co(g)+H2O(g) ΔH2=+41kJ?mol-1
試回答下列問題:
(1)已知CO(g)+2H2(g)?CH3OH(g) ΔH3=-99kJ?mol-1,則ΔH1=kJ?mol-1。
(2)向剛性容器中充入一定量的CO2和H2,在不同催化劑(Cat.1,Cat.2)下經相同反應時間,CO2的轉化率和甲醇的選擇性[甲醇的選擇性=×100%]隨溫度的變化如圖所示:n(CH3OH)n(CO)+n(CH3OH)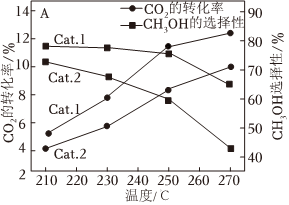
①由圖可知,催化效果Cat.1Cat.2(填“>”“<”或“=”)。
②在210~270℃間,CH3OH的選擇性隨溫度的升高而下降,請寫出一條可能原因。
(3)一定條件下,向剛性容器中充入物質的量之比為1:3的CO2和H2發生上述反應。有利于提高甲醇平衡產率的條件是(填標號)。
A.高溫高壓
B.低溫高壓
C.高溫低壓
D.低溫低壓組卷:33引用:1難度:0.6 -
21.2021年我國制氫量位居世界第一,煤的氣化是一種重要的制氫途徑。回答下列問題:
在一定溫度下,向體積固定的密閉容器中加入足量的C(s)和1molH2O(g),起始壓強為0.2MPa時,發生下列反應生成水煤氣:
Ⅰ.C(s)+H2O(g)?CO(g)+H2(g) ΔH1=+131.4kJ?mol-1
Ⅱ.CO(g)+H2O(g)?CO2(g)+H2(g) ΔH2=-41.1kJ?mol-1
(1)下列說法正確的是。
A.平衡時向容器中充入惰性氣體,反應Ⅰ的平衡逆向移動
B.混合氣體的密度保持不變時,說明反應體系已達到平衡
C.將炭塊粉碎,可加快反應速率
D.平衡時H2的體積分數可能大于23
(2)反應平衡時,H2O(g)的轉化率為50%,CO的物質的量為0.1mol。此時反應Ⅰ的平衡常數Kp=MPa(以分壓表示,分壓=總壓×物質的量分數)。組卷:31引用:1難度:0.6


