滬教版九年級下冊《第7章 應用廣泛的酸、堿、鹽》2021年單元測試卷(福建省龍巖市新羅區蓮東中學)
發布:2024/4/20 14:35:0
一、選擇題
-
1.鑒別下列各組物質,括號中選用的試劑或方法,不正確的是( )
A.KMnO4 和KClO3(觀察顏色) B.NaOH溶液和稀H2SO4溶液(酚酞試液) C.Ca(OH)2溶液和NaOH溶液(稀鹽酸) D.C2H5OH和NaCl溶液(聞氣味) 組卷:22引用:6難度:0.7 -
2.某金屬加工廠生產過程中的廢液含有少量硝酸銀和硝酸銅,為回收利用資源和防止污染,該廠向廢液中加入一定量的鋅粉,反應停止后過濾,向濾出的固體中加入少量稀鹽酸,無氣泡產生.則下列有關說法中,正確的是( )
A.濾出的固體中一定含有銀和銅,一定不含鋅 B.濾出的固體中一定含有銀,可能含有銅和鋅 C.濾液中一定含有硝酸鋅,一定沒有硝酸銀和硝酸銅 D.濾液中一定含有硝酸鋅,可能有硝酸銀和硝酸銅 組卷:1307引用:23難度:0.7 -
3.有四種物質的溶液:①Ba(OH)2、②Na2SO4、③HNO3、④FeCl3,不用其他試劑就可將它們逐一鑒別出來,其鑒別順序是( )
A.④③②① B.④①②③ C.①③④② D.①④②③ 組卷:430引用:91難度:0.9 -
4.分別將下列各組物質同時加到水中,能大量共存的是( )
A.NaCl、AgNO3、Na2SO4 B.HCl、NaCl、Na2CO3 C.Na2SO4、KNO3、NaOH D.Ba(OH)2、NaCl、(NH4)2SO4 組卷:21引用:1難度:0.5 -
5.下列鹽中不能由金屬與酸發生置換反應直接得到的是( )
A.ZnCl2 B.FeSO4 C.Mg(NO3)2 D.CuSO4 組卷:20引用:5難度:0.6 -
6.為得到純凈的物質,某同學設計下表中的除雜方法,其中方法正確的是( )
物質 所含雜質 除去雜質的方法 A NaCl溶液 Na2CO3 加入稀硫酸至不再產生氣泡 B CuO粉末 C 加入過量稀鹽酸,充分反應 C N2氣體 O2 將氣體緩緩通過灼熱的銅網 D CaO CaCO3 加入足量的稀鹽酸 A.A B.B C.C D.D 組卷:14引用:1難度:0.5 -
7.分別將下列各組物質同時加到足量的水中,能得到無色透明溶液的是( )
A.NaNO3、Ba(OH)2、HNO3 B.H2SO4、NaNO3、Na2SO4 C.H2SO4、NaNO3、FeSO4 D.CaCl2、Na2SO4、BaCl2 組卷:97引用:7難度:0.7 -
8.除去下列物質中的少量雜質(括號內是雜質),所用試劑及方法均正確的是( )
A.銅粉(碳粉)--在空氣中灼燒 B.氯化亞鐵溶液(氯化銅)--加過量的鐵粉、過濾 C.氫氧化鈉(碳酸鈉)--加適量的稀鹽酸、蒸發 D.一氧化碳(二氧化碳)--通過足量的氫氧化鈉溶液、干燥 組卷:64引用:21難度:0.7 -
9.下列氣體中,既可以用濃硫酸干燥,又可以用氫氧化鈉固體干燥的是( )
A.氯化氫 B.氨氣 C.氫氣 D.二氧化碳 組卷:37引用:5難度:0.9 -
10.有四瓶溶液分別是Ba(OH)2、Na2CO3、HCl、(NH4)2SO4中的一種,為了區別它們,編號為①②③④,做如下三個實驗.請你根據實驗內容及現象,確定①②③④依次是( )
實驗內容 ①+③ ②+③ ②+④ 實驗現象 有無色無味氣體產生 有白色沉淀產生 有白色沉淀和刺激性氣味的氣體產生 A.Na2CO3、Ba(OH)2、HCl、(NH4)2SO4 B.HCl、Ba(OH)2、(NH4)2SO4、Na2CO3 C.Na2CO3,(NH4)2SO4,Ba(OH)2,HCl D.HCl,Ba(OH)2,Na2CO3,(NH4)2SO4 組卷:84引用:9難度:0.5 -
11.在托盤天平兩邊各放一只等質量的燒杯,在兩只燒杯里分別加入50g溶質質量分數為7.3%的稀鹽酸,將天平調節至平衡;然后向左右兩燒杯中分別加入一定質量的下列各組物質,充分反應后,天平發生偏轉的是( )
A.1.8g鋁粉和1.8g鐵粉 B.4.2g碳酸鎂和2g硝酸銀 C.5.6g鐵粉和5.6g鋅粉 D.10g碳酸鈣和5.6g氧化鈣 組卷:2546引用:24難度:0.5 -
12.比較推理是化學學習中常用的思維方法,下列有關物質的比較推理中正確的是( )
A.中和反應有鹽和水生成,有鹽和水生成的反應一定是中和反應 B.氯化鈉和碳酸鈉都屬于鹽,氯化鈉溶液呈中性,碳酸鈉溶液也呈中性 C.鐵和銅都屬于金屬,鐵能與稀硫酸反應產生氫氣,銅也能與稀硫酸反應產生氫氣 D.中和反應屬于復分解反應,稀硫酸與氨水發生的反應也屬于復分解反應 組卷:29引用:3難度:0.9 -
13.下列物質間的轉化不能通過一步反應直接實現的是( )
A.NaNO3→NaCl B.CuSO4→FeSO4 C.Ca(OH)2→NaOH D.CuO→Cu(OH)2 組卷:34引用:6難度:0.7 -
14.用下列方法鑒別各組無色溶液,能夠達到目的是( )
待鑒別溶液 試劑(均為溶液) A 稀HCl和稀H2SO4 AgNO3 B HCl、NaOH和KNO3 酚酞 C AgNO3和Na2SO4 BaCl2 D Ca(OH)2、NaOH、稀硫酸 Na2CO3 A.A B.B C.C D.D 組卷:33引用:9難度:0.7 -
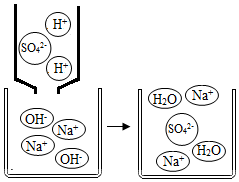 15.如圖是氫氧化鈉溶液與稀硫酸恰好完全反應的微觀示意圖,由此得出的結論不正確的是( )
15.如圖是氫氧化鈉溶液與稀硫酸恰好完全反應的微觀示意圖,由此得出的結論不正確的是( )A.反應結束時溶液的pH=7 B.反應前后元素的種類沒有變化 C.反應中Na+和SO42-結合生成Na2SO4分子 D.該反應的實質是H+和OH-結合生成H2O分子 組卷:15引用:1難度:0.6
二、解答題
-
46.已知A、B、C、D、E、F六種物質有如下圖所示的轉化關系,其中A發生分解反應可生成B和C,B和足量的F反應生成D,而D和E相互反應又生成了A和F,則各物質的化學式分別可能是:

A,B,
C,D,
E,F.組卷:34引用:2難度:0.5 -
 47.研究性學習:探究實驗室中久置的NaOH的變質程度
47.研究性學習:探究實驗室中久置的NaOH的變質程度
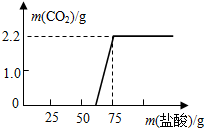
【研究方案】先稱取13.3g的NaOH樣品(雜質為Na2CO3),配成溶液,然后向溶液中逐滴加入質量分數為14.6%的稀鹽酸,根據生成CO2的質量測定Na2CO3的質量.從而進一步確定樣品中NaOH的變質程度.
【解決問題】實驗測得加入稀鹽酸的質量與產生CO2氣體的質量關系如圖所示.
填寫下表:(計算結果保留小數點后一位)
【繼續探究】求實驗過程中與NaOH反應所用鹽酸的質量.Na2CO3的質量/g 變質NaOH的質量/g NaOH的變質程度
(用質量分數表示)
【發現問題】根據“與NaOH反應所用鹽酸的質量”,對照圖象,你發現了什么問題?組卷:105引用:26難度:0.3


