2020-2021學年河北省秦皇島一中高一(下)期末化學試卷
發布:2024/4/20 14:35:0
一、單項選擇題(本題有15小題,每題2分,共30分。每小題只有一個正確答案)
-
1.化學創造美好生活。下列生產活動中,沒有運用相應化學原理的是( )
選項 生產活動 化學原理 A 利用氫氟酸刻蝕石英制作藝術品 氫氟酸可與SiO2反應 B 利用海水制取溴和鎂單質 Br-可被氧化、Mg2+可被還原 C 用聚乙烯塑料制作食品保鮮膜 聚乙烯燃燒生成CO2和H2O D 公園的鋼鐵護欄涂刷多彩防銹漆 鋼鐵與潮濕空氣隔絕可防止腐蝕 A.A B.B C.C D.D 組卷:3引用:1難度:0.7 -
2.在綠色化學工藝中,理想狀態是反應物中的原子全部轉化為欲制得的產物,即原子利用率為100%,在用CH3C≡CH合成CH2=C(CH3)COOCH3的過程中,欲使原子利用率達到最高,還需要其他的反應物有( )
A.CO2和H2O B.CO和CH3OH C.CH3OH和H2 D.H2和CO2 組卷:25引用:2難度:0.9 -
3.化學與社會、生產、生活緊切相關.下列說法正確的是( )
A.石英只能用于生產光導纖維 B.從海水中提取物質都必須通過化學反應才能實現 C.為了增加食物的營養成分,可以大量使用食品添加劑 D.“地溝油”禁止食用,但可以用來制肥皂 組卷:655引用:33難度:0.9 -
4.下列說法正確的是( )
A.烷烴的通式為CnH2n+2,隨n的增大,碳元素的質量分數逐漸減小 B. 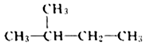 和
和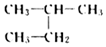 互為同分異構體
互為同分異構體C.丙烷的比例模型為 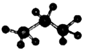
D.分子式為C2H6和分子式為C5H12的烷烴的一氯代物的數目可能相同 組卷:170引用:6難度:0.7 -
5.設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.78g苯和乙炔的混合物中含有碳氫鍵數目為6NA B.100g 46%的乙醇水溶液中含NA個氧原子 C.一定條件下,1mol N2與3mol H2充分反應生成的NH3分子數為2NA D.1mol羥基所含電子數為7NA 組卷:3引用:1難度:0.6 -
6.下列說法正確的是( )
A.乙酸分子中羧基上的氫原子較乙醇中羥基上的氫原子更活潑 B.蛋白質溶液遇醋酸鉛可產生沉淀,加入大量的水,沉淀還可溶解 C.酯類物質在堿性條件下的水解反應叫皂化反應 D.只要醇分子中與羥基相連的碳原子上有氫原子,就可以被催化氧化生成醛類物質 組卷:3引用:1難度:0.7 -
7.元素鉻(Cr)的幾種化合物存在下列轉化關系,下列判斷不正確的是( )

A.反應①表明Cr2O3有酸性氧化物的性質 B.反應②利用了H2O2的氧化性 C.反應②的離子方程式為2CrO2-+3H2O2+2OH-═2CrO42-+4H2O D.反應①②③中鉻元素的化合價均發生了變化 組卷:194引用:7難度:0.8 -
8.下列依據熱化學方程式得出的結論正確的是( )
A.已知 NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ?mol-1,則含 40.0 g NaOH 的稀溶液與稀 醋酸完全中和,放出小于 57.3 kJ 的熱量 B.已知 2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ?mol-1,則氫氣的燃燒熱為 241.8 kJ?mol-1 C.已知 2C(s)+2O2(g)═2CO2(g)△H=a 2C(s)+O2(g)═2CO(g)△H=b,則 a>b D.已知 P(白磷,s)═P(紅磷,s)△H<0,則白磷比紅磷穩定 組卷:7引用:6難度:0.5
三、填空題(本題有4小題,共55分)
-
 23.某化學課外小組設計了如圖所示的裝置制取乙酸乙酯(圖中夾持儀器和加熱裝置已略去)。請回答下列問題:
23.某化學課外小組設計了如圖所示的裝置制取乙酸乙酯(圖中夾持儀器和加熱裝置已略去)。請回答下列問題:
(1)水從冷凝管的(填“a”或“b”)處進入。
(2)已知下列數據:
又知溫度高于140℃時發生副反應:2CH3CH2OH→CH3CH2OCH2CH3+H2O乙醇 乙酸 乙酸乙酯 98%濃硫酸 熔點/℃ -117.3 16.6 -83.6 - 沸點/℃ 78.5 117.9 77.5 338.0
①該副反應屬于反應(填字母)。
a.加成 b.取代 c.酯化
②考慮到反應速率等多種因素,用上述裝置制備乙酸乙酯時,反應的最佳溫度范圍
是(填字母)。
a.T<77.5℃b.T>150℃c.115℃<T<130℃
(3)上述實驗中飽和碳酸鈉溶液的作用是(填字母):
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在飽和碳酸鈉溶液中的溶解度比在水中更小,有利于分層析出
D.加速酯的生成,提高其產率。
(4)欲分離出乙酸乙酯,應使用的分離方法是(填操作方法名稱,下同),所用到的儀器為,進行此步操作后,所得有機層中的主要無機物雜質是水,在不允許使用干燥劑的條件下,除去水可用的方法。
(5)若實驗所用乙酸質量為6.0g,乙醇質量為5.0g,得到純凈的產品質量為4.4g,則乙酸乙酯的產率是。
(6)乙二酸和乙二醇也能發生酯化反應,寫出生成環酯的化學反應方程式組卷:25引用:3難度:0.6 -
24.綠水青山就是金山銀山”。近年來,綠色發展、生態保護成為中國展示給世界的一張新“名片”。
(1)硫酸工業排出的尾氣(主要含SO2)有多種處理方式。
①寫出用過量氨水吸收尾氣的離子方程式:。
②尾氣也可用軟錳礦漿(MnO2)吸收,寫出如圖所示“反應1”的化學方程式:。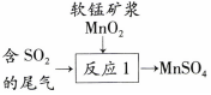
(2)治理汽車尾氣中NO和CO的方法之一是在汽車的排氣管上裝一個催化轉化裝置,使NO和CO在催化劑作用下轉化為無毒物質。寫出該反應的化學方程式:。
(3)某工廠擬綜合處理含NH4+廢水和工業廢氣(主要含N2、Cl2、NO),設計了如下流程: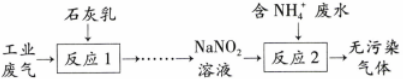
①“反應1”用于吸收Cl2,“反應1”的化學方程式為。
②“反應2”的離子方程式為。
(4)為實現燃煤脫硫,向煤中加入漿狀Mg(OH)2,使燃料產生的SO2轉化為穩定的鎂化合物,寫出該反應的化學方程式:。組卷:33引用:3難度:0.6


