2021-2022學年湖北省武漢市新洲區部分學校高一(上)期末化學試卷
發布:2024/12/20 9:0:3
一、選擇題:在每小題給出的四個選項中,只有一項是符合題目要求的;本題共15小題,每小題3分,共45分。
-
1.古詩詞是古人為我們留下的寶貴精神財富,下列詩句不涉及氧化還原反應的是( )
A.爐火照天地,紅星亂紫煙 B.千淘萬漉雖辛苦,吹盡狂沙始到金 C.熬膽礬鐵釜,久之亦化為銅 D.爆竹聲中一歲除,春風送暖入屠蘇 組卷:28引用:8難度:0.7 -
2.實驗室配制250mL0.1mol?L-1NaOH溶液時肯定不需要的儀器是( )
A. 
B. 
C. 
D.  組卷:29引用:3難度:0.9
組卷:29引用:3難度:0.9 -
3.下表中用途與其性質或原理對應關系不正確的是( )
選項 現象或事實 解釋 A Na2O2常用于潛水艇或呼吸面具供氧劑 Na2O2與CO2反應產生O2 B 常用鋁箔做包裝材料 金屬鋁有好的延展性 C FeCl3溶液可用于刻制印刷銅電路板 FeCl3與Cu發生反應2Fe3++Cu=2Fe2++Cu2+ D 用小蘇打治療胃酸過多 Na2CO3可中和胃酸 A.A B.B C.C D.D 組卷:295引用:7難度:0.5 -
4.體檢時的一些指標常用物質的量濃度表示(可將元素近似折算成相應離子)。根據如圖相關數據,下列分析不正確的是( )
項目名稱 結果 狀態單位 參考值范圍 總鈣 TCa 2.57 mmol?L-1 2.1~2.7 磷 P 1.51↑ mmol?L-1 0.8~1.5 鎂 Mg 0.95 mmol?L-1 0.75~1.25 鉀 K 儀器故障維修 mmol?L-1 3.5~5.5 鈉 Na mmol?L-1 135~160 氯 Cl mmol?L-1 95~105 A.1mmol?L-1=1.0×10-3mol?L-1 B.可用焰色試驗測定鉀離子的含量 C.表中各元素均以化合態存在于人體內 D.若某人10mL血清樣本中含鈣離子1.2mg,則其鈣含量略偏高 組卷:14引用:1難度:0.5 -
5.下列有關反應的離子方程式正確的是( )
A.氯氣溶于水:Cl2+H2O═H++Cl-+HClO B.將鐵單質投入FeCl3溶液中:Fe3++Fe═2Fe2+ C.將濃鹽酸與MnO2混合加熱:MnO2+2H++2Cl- Mn2++Cl2↑+H2O△D.過氧化鈉投入水中:Na2O2+2H2O═O2↑+2OH-+2Na+ 組卷:37引用:1難度:0.7 -
6.設NA表示阿伏加德羅常數的值。下列敘述正確的是( )
A.在常溫常壓下,1.7g NH3含有的原子數為0.4NA B.標準狀況下,2.24L CCl4含有的共價鍵數目為0.4NA C.0.2mol?L-1Na2SO4溶液中,Na+的數目為0.4NA D.50mL 12mol?L-1鹽酸與足量MnO2共熱,轉移的電子數為0.3NA 組卷:37引用:7難度:0.6
二、非選擇題:本題共4小題,共55分。
-
18.硫酸亞鐵晶體(FeSO4?7H2O)在醫藥上常用作補血劑。某課外小組的同學欲測定該補血劑中鐵元素的含量。實驗步驟如下:
①取5片補血劑研細,加入足量的1mol/LH2SO4溶液,充分反應后過濾。
②向濾液中加入一定量的H2O2溶液。
③向步驟②的溶液中加入足量的NaOH堿性溶液后,得到紅褐色懸濁液。
④將此濁液經過系列操作后,最終得到ag紅棕色固體。
請回答下列問題:
(1)證明經步驟①得到的濾液中含有Fe2+的方法是:。
(2)證明步驟①得到的濾液中含有SO42-的方法:。
(3)步驟②加入H2O2發生反應的離子方程式是。
(4)步驟④中一系列操作為過濾、、灼燒、冷卻、稱量。得到的紅棕色固體的用途為(任寫一種):。
(5)若實驗中鐵元素無損耗,則每片補血劑中含鐵元素的質量為g(用含a的式子表示)。組卷:14引用:1難度:0.5 -
19.如圖是元素周期表的一部分,圖中所列的字母分別代表某一種化學元素。完成下列填空。(填元素符號或化學式)

(1)元素B在元素周期表中的位置是第周期第族,A、B、C三種元素原子半徑從大到小的順序是。
(2)D簡單離子的結構示意圖為,D、E中金屬性較強的元素是。
(3)D單質在空氣中燃燒可生成淡黃色粉末X(D2O2),X常用作呼吸面具和潛水艇中的供氧劑,可選用合適的化學試劑和如圖所示實驗裝置證明X有提供氧氣的作用。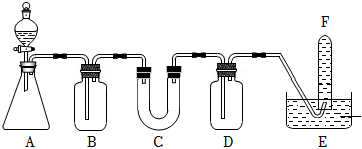
①裝置A使用石灰石與稀鹽酸反應制取CO2,裝置B中飽和NaHCO3溶液的作用是除去。
②裝置C中X與CO2反應的化學方程式是,裝置D盛放NaOH溶液的作用是除去。
③為檢驗試管F收集的氣體,應,若出現現象,即證明X可作供氧劑。組卷:133引用:5難度:0.5


