2020-2021學年安徽省六安市霍邱二中高三(上)開學化學試卷
發布:2024/11/16 10:30:2
一、單選題(共16小題,每小題3分,共48分)
-
1.《夢溪筆談》中記載有:“信州鉛山縣有苦泉,流以為澗。挹其水熬之,則成膽礬。烹膽礬則成銅;熬膽礬鐵釜,久之亦化為銅。”下列對文中內容的解釋正確的是( )
A.“苦泉”可使蛋白質變性 B.膽礬的化學式為CuSO4 C.膽礬受熱不能分解 D.膽礬與鐵通過復分解反應可煉銅 組卷:149引用:9難度:0.5 -
2.下列有關物質的分類與性質的說法正確的是( )
A.液氯、冰醋酸、C4H8均屬于純凈物 B.SO3、SiO2均屬于酸性氧化物 C.已知:H3RO2+NaOH(足量)═NaH2RO2+H2O,則H3RO2為三元酸,NaH2RO2為酸式鹽 D.往任何膠體中加入任何電解質都能使膠體粒子聚沉 組卷:41引用:5難度:0.7 -
3.下列示意圖中,白球代表氫原子,黑球代表氦原子,方框代表容器,容器中間有一個可以上下滑動的隔板(其質量可忽略不計)。其中能表示等質量的氫氣與氦氣的是( )
A. 
B. 
C. 
D.  組卷:594引用:33難度:0.7
組卷:594引用:33難度:0.7 -
4.分類是學習和研究化學的一種常用的科學方法,下列分類合理的是( )
①根據酸分子中含有H原子個數將酸分為一元酸、二元酸等
②堿性氧化物一定是金屬氧化物
③根據丁達爾現象可將分散系分為膠體、溶液和濁液
④SiO2能與NaOH溶液反應生成Na2SiO3和水,SiO2是酸性氧化物。A.②③ B.②④ C.①②④ D.②③④ 組卷:31引用:5難度:0.9 -
5.在含有下列各離子組的溶液中,能大量共存且溶液為無色透明的是( )
A.Na+、Cu2+、Cl-、 SO2-4B.Ba2+、K+、OH-、 NO-3C.K+、Ca2+、 、NH+4CO2-3D.H+、Ca2+、Cl-、 HCO-3組卷:3引用:3難度:0.9 -
6.常溫下,下列各組離子在指定溶液中能大量共存的是( )
A.0.1mol?L-1氨水溶液:Na+、K+、OH-、NO3- B.0.1mol?L-1鹽酸溶液:Na+、K+、SO42-、SiO32- C.0.1mol?L-1KMnO4溶液:NH4+、Na+、NO3-、I- D.0.1mol?L-1AgNO3溶液:NH4+、Mg2+、Cl-、SO42- 組卷:1413引用:20難度:0.5 -
7.下列表示不正確的是( )
A.乙烯的結構式: 
B.甲酸甲酯的結構簡式:C2H4O2 C.2-甲基丁烷的鍵線式: 
D.甲基的電子式:  組卷:385引用:22難度:0.7
組卷:385引用:22難度:0.7
二、填空題(共5小題,共52分)
-
20.高鐵酸鉀(K2FeO4)是一種易溶于水,高效的多功能水處理劑。工業上通常先制得高鐵酸鈉,然后在一定溫度下,向高鐵酸鈉溶液中加入KOH至飽和,從而使高鐵酸鉀析出。
(1)高鐵酸鉀中鐵元素的化合價為,推測其具有的化學性質是。
(2)高鐵酸鉀與水反應生成O2、Fe(OH)3(膠體)和KOH。
①該反應的離子方程式為。
②高鐵酸鉀作為水處理劑起到的作用是。
(3)①在無水條件下制備高鐵酸鈉的主要反應為2FeSO4+aNa2O2═2Na2FeO4+bX+2Na2SO4+cO2↑,該反應中物質X的化學式為,b與c的關系是。
②一定溫度下,向高鐵酸鈉溶液中加入KOH至飽和可析出高鐵酸鉀,原因是。
(4)在堿性條件下,由氯化鐵、氯氣可制備出高鐵酸鉀,寫出該反應的離子方程式:。組卷:15引用:2難度:0.6 -
21.元素X的基態原子中的電子共有7個能級,且最外層電子數為1,X原子的內層軌道全部排滿電子,在氣體分析中,常用XCl的鹽酸溶液吸收并定量測定CO的含量,其化學反應如下:2XCl+2CO+2H2O═X2Cl2?2CO?2H2O.
(1)X基態原子的電子排布式為.
(2)C、H、O三種原子的電負性由大到小的順序為.
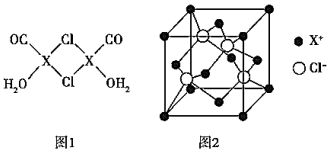
(3)X2Cl2?2CO?2H2O是一種配合物,其機構如圖1所示:
①與CO為互為等電子的分子是.
②該配合物中氯原子的雜化方式為.
③在X2Cl2?2CO?2H2O中,每個X原子能與其它原子形成3個配位鍵,在圖中用“→”標出相應的配位鍵.
(4)阿伏加德羅常數的測定有多種方法,X射線衍射法就是其中一種,通過對XCl晶體的X射線衍射圖象的分析,可以得出XCl的晶胞如圖2所示,則距離每個X+最近的Cl-的個數為,若X原子的半徑為a pm,晶體的密度為pg/cm3,試通過計算阿伏加德羅常數NA=(列計算式表達)組卷:11引用:3難度:0.9


