2021-2022學年湖南省百所學校大聯考高三(上)期中化學試卷
發布:2024/12/29 22:30:3
一、選擇題:本題共10小題,每小題3分,共30分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.傳統文化是中華文明的重要組成部分。下列關于傳統文化摘錄的化學解讀錯誤的是( )
選項 傳統文化摘錄 化學解讀 A 墻角數枝梅,凌寒獨白開。遙知不是雪,為有暗香來 分子是不斷運動的 B 千淘萬灘雖辛苦,吹盡狂沙始到金 黃金的化學性質很穩定 C 紛紛燦爛如星隕,??喧豗似火攻 焰色反應是物理變化 D 有硇水者,翦銀塊投之,則旋而為水 “硇水”指鹽酸 A.A B.B C.C D.D 組卷:21引用:4難度:0.7 -
2.據西漢東方朔所撰的《神異經?中荒經》載,“西北有宮,黃銅為墻,題曰:地皇之宮。”文中“黃銅”的主要成分是銅鋅,還含少量錫、鉛。下列說法錯誤的是( )
A.金屬活動性:Zn>Pb>Sn>Cu B.用黃銅制作的高洪太銅鑼應置于干燥處保存 C.黃銅器能與稀硝酸發生反應 D.可用灼燒法區分黃銅和黃金首飾 組卷:37引用:8難度:0.7 -
3.下列各組離子能大量共存的是( )
A.Fe3+、Na+、SO42-、SCN- B.H+、K+、CH3COO-、Cl- C.NH4-、K-、I-、Br- D.Cu2+、Mg2+、SO32-、ClO- 組卷:4引用:1難度:0.7 -
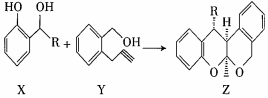 4.我國科學家仿生催化合成四環色烯縮酮(Z)的反應原理如圖,已知:R為經基。下列說法正確的是( )
4.我國科學家仿生催化合成四環色烯縮酮(Z)的反應原理如圖,已知:R為經基。下列說法正確的是( )A.X苯環上的一氯代物只有2種 B.Y的分子式為C11H10O C.Z分子中所有原子可能共平面 D.X、Y、Z均能發生加成反應 組卷:31引用:5難度:0.6 -
5.下列操作不能達到目的的是( )
A.  制備乙酸乙酯
制備乙酸乙酯B.  探究硅酸和碳酸的酸性強弱
探究硅酸和碳酸的酸性強弱C. 
探究NaHCO3溶液的穩定性D.  驗證鈉在氧氣中燃燒組卷:12引用:6難度:0.5
驗證鈉在氧氣中燃燒組卷:12引用:6難度:0.5 -
6.下列離子方程式正確的是( )
A.向NaHCO3飽和溶液中滴加CaCl2飽和溶液:Ca2++2 ═CaCO3↓+CO2↑+H2OHCO-3B.向稀硝酸中滴加Na2S2O3溶液:2H++S2 ═S↓+SO2↑+H2OO2-3C.向新制氯水中滴加少量的FeBr2溶液:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- D.向NH4Cl溶液中加入小顆粒鈉:2Na+2H2O═2Na++2OH-+H2↑ 組卷:33引用:10難度:0.7
三、非選擇題:本題共4小題,共54分。
-
17.以廢鎳觸媒(含NiO、MgO、CaO、Al2O3、Fe2O3及SiO2)為原料制備硫酸鎳的工藝流程如圖:

已知:①NiS不溶于水或稀硫酸;NiS+2O2NiSO4。△
②該工藝流程條件下,有關金屬離子開始沉淀和完全沉淀時的pH見下表:
回答下列問題:金屬離子 Ni+ Fe3+ Al3+ Mg2+ 開始沉淀時的pH 6.4 2.2 4.1 9.6 完全沉淀時的pH 8.4 3.5 5.4 11.6
(1)“酸溶”時,Al2O3溶解的化學方程式為。
(2)“濾渣1”的成分是(填化學式)。
(3)“濾液1”的pH約為1.8,在“調節pH”時用氨水逐步調節pH至6.3,依次析出的是(填化學式)。
(4)從“沉鎳”到“溶解”還需經過的操作是,“溶解”時用0.01mol?L-1的硫酸而不用水的原因是。
(5)“濾渣4”并入濾渣(填“1”、“2”或“3”)可實現再利用。
(6)某工廠用2t該廢鎳觸媒(NiO含量為75%)制備硫酸鎳,設整個流程中Ni的損耗率為20%,最終得到NiSO4?6H2O的質量為t。組卷:30引用:8難度:0.7 -
18.工業上,裂解正丁烷可以獲得乙烯、丙烯等化工原料。
反應1:C4H10(g,正丁烷)?CH4(g)+C3H6(g)ΔH1
反應2:C4H10(g,正丁烷)?C2H6(g)+C2H1(g)ΔH2
已知幾種共價鍵的鍵能如下表: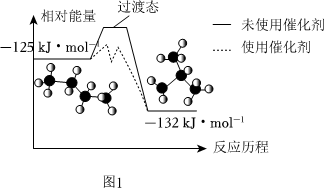
(1)根據上述數據估算,ΔH1=共價鍵 C-H C=C C-C 鍵能/(kJ?mol-1) 413 614 347 kJ?mol-1。
(2)正丁烷和異丁烷之間轉化的能量變化如圖1所示。
①正丁烷氣體轉化成異丁烷氣體的熱化學方程式為。
②下列有關催化劑的敘述錯誤的是(填標號)。
A.能改變反應途徑
B.能降低反應焓變
C.能加快反應速率
D.能增大平衡常數
(3)向密閉容器中投入一定量的正丁烷,發生反應1和反應2,測得正丁烷的平衡轉化率(α)與壓強(p)、溫度(T)的關系如圖2所示。
①p1、p2、p3由小到大的順序為。
②隨著溫度升高,三種不同壓強下正丁烷的平衡轉化率趨向相等,原因是。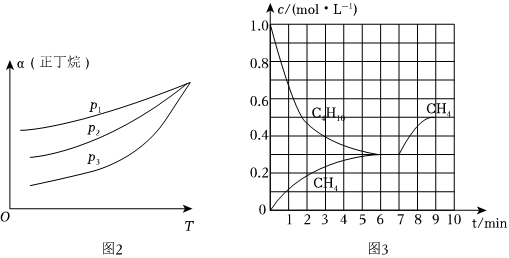
(4)在一定溫度下,向密閉容器中投入正丁烷,同時發生反應1和反應2。測得部分物質的濃度與時間的關系如圖3,平衡時壓強為17akPa。
①7min時改變的條件可能是(填標號)。
A.增大壓強
B.增大正丁烷的濃度
C.加入催化劑
②該溫度下,反應1的平衡常數Kp=kPa。(提示:組分分壓=總壓×)該組分的物質的量各組分的總物質的量組卷:32引用:5難度:0.5


