2021-2022學年遼寧省大連市金普新區示范性高中聯合體高三(上)第二次段考化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共15小題,每小題3分,共45分。每小題只有一項符合題目要求
-
1.我國四川廣漢的三星堆遺址距今已有3000~5000年歷史,2021年3月20日,三星堆遺址新出土了多達500多件重要文物,如黃金面具、絲綢“黑炭”、青銅神樹、陶瓷碎片等。下列有關敘述錯誤的是( )
A.考古時利用 C測定文物的年代,146C的中子數為8146B.黃金面具、青銅神樹的成分均為純金屬 C.絲綢轉化為“黑炭”的過程涉及化學變化 D.三星堆中含有大量的陶瓷碎片,屬于無機非金屬材料 組卷:48引用:9難度:0.8 -
2.下列反應的離子方程式書寫正確的是( )
A.SO2通入漂白粉溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO B.向0.1mol/LAgNO3溶液中加入過量氨水:Ag++NH3?H2O=AgOH↓+NH4+ C.向FeCl3溶液中加入KSCN溶液:Fe3++3SCN-=Fe(SCN)3↓ D.向NaHSO4溶液中加入過量的Ba(OH)2溶液:Ba2++OH-+H++SO42-=BaSO4↓+H2O 組卷:15引用:2難度:0.7 -
3.25℃時,下列各溶液中一定能大量共存的離子組是( )
A.加入Al能放出H2的溶液中:K+、NO3-、Cl-、HCO3- B.pH=2的溶液中:K+、AlO2-、SiO32-、SO42- C.澄清透明的溶液中:Cu2+、Mg2+、SO42-、NO3- D.0.1mol/L的Fe(NO3)2溶液中:Na+、H+、K+、Cl- 組卷:13引用:3難度:0.6 -
4.下列物質的性質變化規律正確的是( )
A.F2、Cl2、Br2、I2的熔、沸點逐漸升高 B.HF、HCl、HBr、HI的沸點順序為HI>HBr>HCl>HF C.金剛石的硬度高于晶體硅,但熔點、沸點低于晶體硅 D.NaF、NaCl、NaBr、NaI的熔點依次升高 組卷:18引用:2難度:0.5 -
5.設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.標準狀況下,11.2L苯中含有分子的數目為0.5NA B.pH=1的H3PO4溶液中,含有0.1NA個H+ C.在常溫常壓下,0.1mol鐵與0.1molCl2充分反應,轉移的電子數為0.3NA D.標準狀況下,22.4LNO和11.2LO2混合后氣體的分子總數小于NA 組卷:16引用:3難度:0.8 -
 6.在酸性條件下,黃鐵礦(FeS2)催化氧化的反應方程式為2FeS2+7O2+2H2O═2Fe2++4+4H+,實現該反應的物質間轉化如圖所示。下列分析錯誤的是( )SO2-4
6.在酸性條件下,黃鐵礦(FeS2)催化氧化的反應方程式為2FeS2+7O2+2H2O═2Fe2++4+4H+,實現該反應的物質間轉化如圖所示。下列分析錯誤的是( )SO2-4A.反應Ⅰ的離子方程式為4Fe(NO)2++O2+4H+═4Fe3++4NO+2H2O B.反應Ⅱ的氧化劑是Fe3+ C.反應Ⅲ是氧化還原反應 D.黃鐵礦催化氧化中NO作催化劑 組卷:85引用:11難度:0.5
二、非選擇題:包括4個小題,共55分。
-
18.鐵(Fe)、鈷(Co)、鎳(Ni)是第四周期第VIII族的元素,在化學上稱為鐵系元素,其化合物在生產生活中應用廣泛。
(1)基態Ni原子的核外價層電子排布圖為。
(2)鐵系元素能與CO形成Fe(CO)5、Ni(CO)4等金屬羰基化合物。已知室溫時Fe(CO)5為淺黃色液體,沸點103℃,則Fe(CO)5中含有的化學鍵類型包括。
A.極性共價鍵
B.離子鍵
C.配位鍵
D.金屬鍵
(3)以甲醇為溶劑,Co2+可與色胺酮分子配位結合形成對DNA具有切割作用的色胺酮鈷配合物(合成過程如下所示)。色胺酮分子中所含元素(H、C、N、O)第一電離能由大到小的順序為,色氨酮分子中N原子的雜化類型為。X射線衍射分析顯示色胺酮鈷配合物晶胞中還含有一個CH3OH分子,CH3OH是通過作用與色胺酮鈷配合物相結合。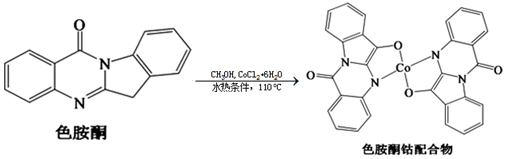
(4)LiFePO4常用作鋰離子電池的正極材料,其陰離子PO43-的空間構型為。
(5)Fe、Co、Ni與Ca都位于第四周期且最外層電子數相同,但相應單質的熔點,Fe、Co、Ni明顯高于Ca,其原因是。組卷:11引用:1難度:0.5 -
19.疫情期間,公共場所需要經常進行消毒,75%的醫用酒精和84消毒液都能有效消滅病毒。某化學興趣小組探究84消毒液(有效成分為NaClO)與75%醫用酒精能否反應,進行如下實驗:
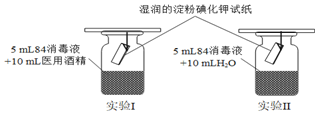
(1)實驗室制備84消毒液的化學方程式為。
(2)將25mL無水乙醇配成75%醫用酒精,下列儀器中不需要使用的有(填序號)。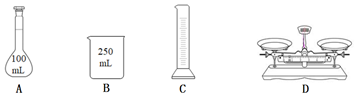
(3)實驗結果:實驗Ⅰ的淀粉碘化鉀試紙在3 min時變藍,實驗Ⅱ的淀粉碘化鉀試紙在8 min時變藍。
①實驗Ⅰ中,使濕潤的淀粉碘化鉀試紙變藍的物質是(寫化學式)。
②實驗II中,濕潤的淀粉碘化鉀試紙也變藍的原因可能是。
③通過對比實驗Ⅰ和Ⅱ的現象,可以說明84消毒液與75%醫用酒精能夠反應,理由是。
(4)為了測定84消毒液與醫用酒精1:1反應后溶液中殘留的NaClO的含量(假設反應生成的氣體已全部逸出),小組進行了如下實驗:取7.45 mL反應后溶液(密度約1 g?mL-1)于錐形瓶,加入過量KI溶液和適量硫酸,在冷暗處靜置4-5min后,再加入少量淀粉指示劑,用0.1000 mol?L-1 Na2S2O3標準液滴定,消耗標準液體積為24.00 mL。(已知:I2+2S2O32-═2I-+S4O62-)
①NaClO與KI反應的離子方程式為。
②判斷滴定終點的方法是,上述實驗中84消毒液與醫用酒精1:1反應后溶液中殘留的NaClO的質量分數為(計算結果保留兩位有效數字)。組卷:9引用:6難度:0.5


