2022年廣東省廣州市華南師大附中高考化學押題試卷(三)
發布:2024/4/20 14:35:0
一、選擇題:本題共16小題,共44分。第1~10小題,每小題2分;第11~16小題,每小題2分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.化學是推動科技進步和現代社會文明的重要力量。下列有關說法錯誤的是( )
A.制造“蛟龍號”潛水艇載人艙的鈦合金是金屬材料 B.天和核心艙舷窗使用的耐輻射石英玻璃的主要成分為Na2SiO3 C.利用化石燃料燃燒產生的CO2合成聚碳酸酯可降解塑料,有利于實現“碳中和” D.我國“硅-石墨烯-鍺晶體管”技術已獲重大突破,C、Si、Ge都是主族元素 組卷:33引用:1難度:0.6 -
2.我國科學家首次在實驗室中實現從二氧化碳到淀粉的全合成,合成路徑如圖所示。下列表示相關微粒的化學用語正確的是( )

A.淀粉的分子式:(C6H12O6)n B.DHA的最簡式:CH2O C.FADH的電子式: 
D.CO2的比例模型:  組卷:23引用:5難度:0.8
組卷:23引用:5難度:0.8 -
3.NA為阿伏加德羅常數的值,下列敘述正確的是( )
A.12g金剛石中含有的碳碳鍵數目為NA B.1L0.5mol?L-1FeCl3溶液中Fe3+的數目為0.5NA C.1LpH=2的CH3COOH溶液中H+數目為0.01NA D.0.5molCH4與足量Cl2在光照條件下充分反應得到CH3Cl的數目為0.5NA 組卷:14引用:3難度:0.6 -
4.進行化學實驗時應規范實驗操作,強化安全意識。下列做法正確的是( )
A.金屬鈉失火使用濕毛巾蓋滅 B.酒精燈加熱平底燒瓶時不墊石棉網 C.CCl4萃取碘水實驗完成后的廢液直接排入下水道中 D.制取硝基苯用到的試劑苯應與濃硝酸分開放置并遠離火源 組卷:11引用:3難度:0.7 -
5.下列有關不同價態含硫化合物的說法錯誤的是( )

A.工業接觸法制備硫酸涉及的轉化為FeS2→X→Y→Z B.實驗室制備乙炔中的硫化氫雜質可用M溶液除去 C.黃鐵礦的主要成分為FeS2,該化合物中陰陽離子個數比為1:1 D.硫在過量氧氣中燃燒能夠生成Y 組卷:44引用:5難度:0.8 -
6.下列說法中錯誤的是( )
A.水汽化和水分解兩個變化過程中都破壞了共價鍵 B.酸性強弱:三氟乙酸>三氯乙酸>乙酸 C.基態碳原子核外有三種能量不同的電子 D.區分晶體和非晶體最可靠的科學方法是對固體進行X射線衍射實驗 組卷:69引用:10難度:0.7
二、非選擇題:本題共4小題,共56分。
-
19.尿素[CO(NH2)2]是首個由無機物人工合成的有機物。
(1)已知:①2NH3(g)+CO2(g)═NH2CO2NH4(s) ΔH=-159.5kJ?mol-1
②NH2CO2NH4(s)═CO(NH2)2(s)+H2O(g) ΔH=+116.5kJ?mol-1
則氨氣與二氧化碳氣體合成固態尿素和氣態水的熱化學方程式為。
(2)一定條件下,向容積恒定為2L的密閉容器中加入0.10molCO2和0.40molNH3,發生反應2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g),60min達到平衡,反應中CO2的物質的量隨時間變化如表所示:
①60min時,上述反應的平均反應速率v(CO2)=時間/min 0 20 60 80 n(CO2)/mol 0.10 0.06 0.04 0.04 。
②NH3的平衡轉化率為。
(3)一定條件下,恒容容器中,若原料氣中的NH3和CO2的物質的量的比值=x,發生反應2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g),x與CO2的平衡轉化率(α)的關系如圖1所示:n(NH3)n(CO2)
①α隨著x增大而增大的原因是。
②若A點平衡時容器內總壓強為p0kPa,則上述反應的平衡常數Kp=。(用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)
(4)以惰性電極電解尿素[CO(NH2)2]的堿性溶液可制取氫氣,裝置如圖2所示。該裝置陽極的電極反應式為,若兩極共收集到氣體22.4L(標準狀況),則消耗的尿素的質量為(忽略氣體的溶解)。 組卷:48引用:1難度:0.5
組卷:48引用:1難度:0.5 -
20.2021年諾貝爾生理學或醫學獎頒發給發現溫度和觸覺感受器的兩位科學家,其中溫度感受器的發現與辣椒素有關。辣椒素Ⅰ的一種合成路線如圖(部分試劑或產物略)。
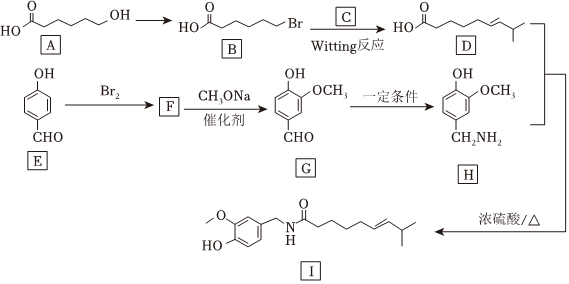
已知:R1-CH2BrR1-CH═CH-R2。R2-CHO反應
(1)A的分子式為;由A生成B的反應類型為。
(2)D中的官能團名稱為;C的結構簡式為。
(3)F→G的化學反應方程式為。
(4)G的同分異構體中,同時符合下列條件的有種(不含立體異構),其中核磁共振氫譜為五組峰的結構簡式為。
①能與FeCl3溶液發生顯色反應;
②能與飽和碳酸氫鈉溶液反應放出氣體。
(5)利用Wittig反應,設計以溴化芐( )為原料合成
)為原料合成 的路線 (無機試劑任選,不考慮產物的立體異構)。組卷:22引用:1難度:0.5
的路線 (無機試劑任選,不考慮產物的立體異構)。組卷:22引用:1難度:0.5


