2022-2023學年吉林省長春市農安十中高一(上)期末化學試卷
發布:2024/12/15 6:0:2
一、單選題(本大題共15小題,每小題3分)
-
1.下列關于膠體的敘述不正確的是( )
A.膠體區別于其他分散系的本質特征是分數質的微粒直徑在1nm~100nm之間 B.用平行光照射CuSO4溶液和Fe(OH)3膠體,可以加以區分 C.Fe(OH)3膠體帶正電 D.樹林中的晨曦,該現象與丁達爾效應有關 組卷:25引用:2難度:0.6 -
2.下列屬于氧化還原反應的是( )
A.NaOH+HCl═NaCl+H2O B.Zn+2HCl═ZnCl2+H2↑ C.2NaHCO3 Na2CO3+H2O+CO2↑加熱D.CuO+2HCl═CuCl2+H2O 組卷:118引用:9難度:0.9 -
3.向盛有Cl2的三個集氣瓶甲、乙、丙中各注入①水、②AgNO3溶液、③NaOH溶液中的一種,振蕩后,實驗現象如圖所示,則集氣瓶甲、乙、丙中注入的液體分別是( )
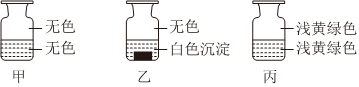
A.③①② B.②①③ C.③②① D.①③② 組卷:33引用:1難度:0.7 -
4.下列敘述正確的是( )
A.BaSO4難溶于水,但BaSO4是電解質 B.Cl2是活潑的非金屬單質,常溫下可以與Na、Fe等金屬發生化合反應 C.氧化還原反應中所有元素的化合價都發生變化 D.金剛石和石墨互為同素異形體,物理性質相同 組卷:25引用:4難度:0.6 -
5.某同學向一新制的FeSO4溶液中逐滴滴加NaOH溶液直至過量,生成的白色沉淀迅速變成灰綠色,一段時間后,有紅褐色物質生成.下列說法正確的是( )
A.灰綠色沉淀為Fe(OH)2 B.紅褐色物質灼燒后可得到鐵單質 C.在隔絕空氣的條件下進行上述實驗,可長時間觀察Fe(OH)2沉淀的顏色 D.沉淀顏色變化的過程中未發生氧化還原反應 組卷:95引用:4難度:0.7 -
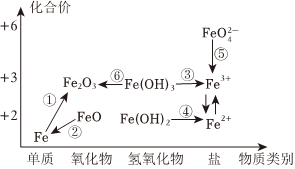 6.元素的價類二維圖是我們學習元素及其化合物相關知識的重要模型和工具,它指的是以元素的化合價為縱坐標,以物質的類別為橫坐標所繪制的二維平面圖像。鐵元素的價類二維圖如圖,其中箭頭表示部分物質間的轉化關系,下列說法錯誤的是( )
6.元素的價類二維圖是我們學習元素及其化合物相關知識的重要模型和工具,它指的是以元素的化合價為縱坐標,以物質的類別為橫坐標所繪制的二維平面圖像。鐵元素的價類二維圖如圖,其中箭頭表示部分物質間的轉化關系,下列說法錯誤的是( )A.Fe3O4是一種黑色有磁性的鐵的氧化物,可由Fe、水蒸氣高溫反應制得 B.為實現Fe2+向Fe3+的轉化,可向含Fe2+的溶液中通入Cl2或者滴加H2O2溶液 C.由圖可預測:高鐵酸鹽( )具有強氧化性,可將Fe2+轉化為Fe3+FeO2-4D.FeO、Fe2O3、Fe3O4均可與酸反應,只生成一種鹽和水 組卷:152引用:6難度:0.7
二、填空題(本大題共4小題)
-
18.氯可形成多種含氧酸鹽,廣泛應用于殺菌、消毒及化工領域。
Ⅰ.實驗室中利用如圖甲裝置(部分裝置省略)制備KClO和NaClO,探究其氧化還原性質。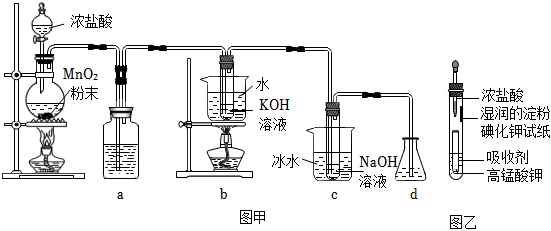
回答下列問題:
(1)盛放MnO2粉末的儀器名稱是,a中的試劑為。
(2)寫出HClO的電子式。
(3)d的作用是,可選用試劑(填標號)。
A.Na2S溶液
B.NaCl溶液
C.Ca(OH)2溶液
D.稀H2SO4
(4)反應結束后,取出b中試管,經冷卻結晶,,洗滌,干燥,得到KClO3晶體。
(5)一位同學設計了一套用濃鹽酸和高錳酸鉀固體制取少量氯氣并能比較氯氣與碘單質氧化性強弱的微型裝置,如圖乙所示。能說明氯氣的氧化性強于碘單質的實驗現象是。組卷:11引用:1難度:0.5 -
19.我國化學家侯德榜發明了聯合制堿法,對世界制堿工業做出了巨大貢獻。聯合制堿法的主要過程如圖所示。
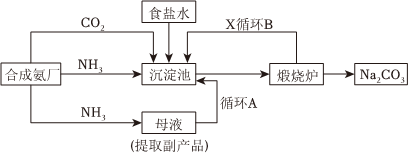
沉淀池反應:NaCl+CO2+NH3+H2ONaHCO3↓+NH4Cl。低溫
(1)“侯氏制堿法”譽滿全球,其中的“堿”為(填化學式),俗稱。
(2)實驗室模擬“侯氏制堿法”,下列操作未涉及的是。
A.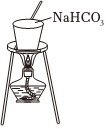 B.
B.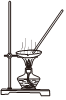 C.
C.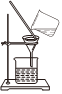 D.
D.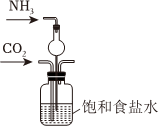
(3)煅燒爐中發生反應的化學方程式為。
(4)使用原料氯化鈉的利用率從70%提高到90%以上,主要是設計了(填上述流程中的編號)的循環,流程中物質X為(填化學式)。
(5)該流程提取的副產品為(填化學式),其用途(寫一種)。
(6)簡單的檢驗方案的一般敘述過程為:①取試樣,②加檢驗試劑,③現象,④結論。為驗證產品純堿中含有雜質NaCl,簡單的檢驗方案是:取少量試樣溶于水后,。組卷:30引用:2難度:0.6


