2023年江蘇省常州市中考化學調研試卷
發布:2024/4/20 14:35:0
一、選擇題(本題包括20小題,共40分。每小題只有一個選項符合題意。請將正確答案前的序號按對應的題號填涂在答題紙上)
-
1.勞動課正式成為中小學的一門獨立課程。下列勞動實踐中包含化學變化的是( )
A.菜園澆水 B.烘焙糕點 C.淘米洗菜 D.縫制荷包 組卷:41引用:4難度:0.8 -
2.二十大報告提出持續深入打好藍天、碧水、凈土保衛戰。下列行為符合報告要求的是( )
A.燃放煙花爆竹,增強節日氣氛 B.推廣秸稈綜合利用,杜絕露天焚燒 C.多用一次性餐盒,保證干凈衛生 D.廢棄電池深埋處理,減少環境污染 組卷:74引用:8難度:0.8 -
3.“卜弋魚圓制作技藝”入選第五批常州市非遺目錄。“卜弋魚圓”所含的主要營養物質是( )
A.糖類 B.油脂 C.蛋白質 D.維生素 組卷:24引用:4難度:0.8 -
4.華為發布了全球首款采用塑料制作柔性屏幕的5G折疊手機。塑料屬于( )
A.金屬材料 B.合成材料 C.復合材料 D.無機非金屬材料 組卷:100引用:7難度:0.6 -
5.肥田粉的主要成分是硫酸銨【(NH4)2SO4】,硫酸銨屬于( )
A.混合物 B.酸 C.堿 D.鹽 組卷:19引用:1難度:0.9 -
6.勤洗手能有效保護自己,減少病毒和細菌的入侵。下列常用于手部消毒的物質為( )
A.稀鹽酸 B.燒堿溶液 C.75%的酒精 D.石灰水 組卷:12引用:1難度:0.6 -
7.芋頭皮上含一種皂角素的堿性物質,皮膚沾上會奇癢難忍。生活中的下列物質可用來止癢的是( )
A.肥皂(pH=10.0) B.牙膏(pH=9.0) C.洗潔精(pH=7.5) D.食醋(pH=2.5) 組卷:38引用:1難度:0.7 -
8.煤氣中添加少量有臭味的乙硫醇(C2H5SH),可以提醒人們預防煤氣泄漏。乙硫醇在煤氣燃燒過程中也可充分燃燒,其反應方程式為2C2H5SH+9O2
4CO2+2X+6H2O,則X的化學式為( )點燃A.SO2 B.SO3 C.CO D.H2SO4 組卷:77引用:7難度:0.9 -
9.古代造紙,為保證成漿效果通常會在蒸煮原料時往漿水中加入草木灰(主要成分為K2CO3)和石灰水,其中反應之一是K2CO3+Ca(OH)2=CaCO3↓+2KOH,該反應的類型為( )
A.化合反應 B.分解反應 C.置換反應 D.復分解反應 組卷:40引用:2難度:0.6
三、(本題包括5小題,共40分)
-
28.我國向世界承諾在2060年實現“碳中和”。中國科學院提出了“液態陽光”概念,即將太陽能轉化為可穩定存儲并且可輸出的燃料甲醇,達到燃料零碳化。如圖1是利用化學鏈燃燒產生的高濃度CO2制備甲醇的流程圖。
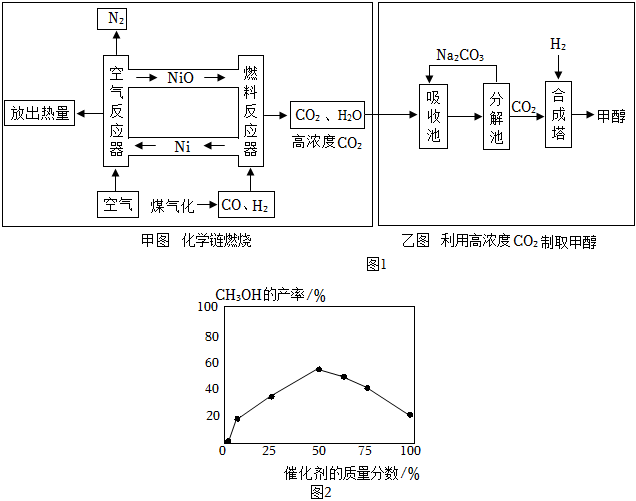
(1)圖1甲圖是利用鎳(Ni)進行化學鏈燃燒的流程圖。與CO、H2直接在空氣中燃燒方式相比,化學鏈燃燒排放出的CO2濃度更高的原因是。
(2)圖1乙圖是利用高濃度CO2制取甲醇的流程圖。吸收池內,飽和碳酸鈉溶液吸收高濃度CO2生成碳酸氫鈉;分解池內,碳酸氫鈉受熱分解放出CO2;合成塔內,利用新型催化劑實現人工“光合作用”,將CO2與H2O反應生成甲醇(CH3OH)。
①分解池內碳酸氫鈉分解的化學方程式是。
②合成塔內生成甲醇的化學反應方程式是。
(3)在實際生產中,甲醇的產率除受濃度、溫度、壓強等因素影響外,還受催化劑質量分數的影響。由圖2可知,當其它條件一定時,催化劑質量分數為時,甲醇的產最高。
(4)根據本題,下列說法正確的是(填序號)。
a.“碳中和”中的“碳”指的是碳單質
b.“碳中和”指的是沒有碳排放
c.“液態陽光”將實現燃料零碳化
d.控制化石燃料的使用可減少碳排放組卷:85引用:1難度:0.5 -
29.我國企業用10年時間,自主研發出海水鎂資源綜合利用專利技術,生出碳酸鎂水合物,并以此為中間體制備各類鎂產品,填補了我國高端鎂產品生產空白。
環節一、探尋海水之“鎂”
(1)已知某海域海水中總的含鹽量約為3.5%,鹽中鎂元素的質量分數約為3.7%,則海水中鎂元素的質量分數約為(保留兩位有效數字),由此可知,用海水曬鹽后的鹵水來提取鎂,而不直接用海水的主要原因是。
環節二、制備三水合碳酸鎂
工業上從弱堿性鹵水(主要成分為MgCl2)中獲取MgCO3?3H2O的一種方法如圖1:
(2)過濾需要用到的玻璃儀器有燒杯、玻璃棒和。
(3)沉淀過程的pH隨時間的變化如圖2所示,沉淀過程的操作為(填標號)。
a.向NaOH溶液中滴加鹵水,同時通入CO2
b.向鹵水中滴加NaOH溶液,同時通入CO2
c.向NaOH溶液中通入CO2至飽和,然后滴加鹵水,同時繼續通入CO2
d.向鹵水中通入CO2至飽和,然后滴加NaOH溶液,同時繼續通入CO2
環節三、測定MgCO3?3H2O的純度
【查閱資料】①Mg5(OH)2(CO3)4?4H2O也可表示為Mg(OH)2?4MgCO3?4H2O,其相對分子質量為466,能與硫酸反應生成CO2;②沉淀法測物質含量,沉淀質量越大,誤差越小。
【實驗步驟】利用如圖3所示裝置(圖中夾持儀器略去)進行實驗,以確定MgCO3?3H2O的純度。
依據實驗過程回答下列問題。
(4)C中反應的化學方程式為;D中堿石灰的作用為。
(5)下列措施中不能提高測定準確度的是(填序號)。
a.在加入硫酸之前應排凈裝置內CO2氣體
b.在AB之間增添盛有濃硫酸的洗氣裝置
c.為了縮短實驗時間,快速滴加硫酸
d.在C裝置左側導管末端增添多孔球泡
(6)小智認為應將C中Ca(OH)2溶液換成Ba(OH)2溶液,理由一:氫氧化鋇的溶解度大,形成溶液的濃度大,使CO2被吸收的更完全;理由二。
(7)實驗中準確稱取三份7.5g樣品,進行三次測定,測得生成CaCO3沉淀的平均質量為5.0g,則樣品中MgCO3?3H2O的純度為。若獲取樣品中含有少量Mg5(OH)2(CO3)4?4H2O,則樣品中MgCO3?3H2O的純度(填“偏大”“不變”或“偏小”)。組卷:9引用:1難度:0.3


