2021-2022學年廣西欽州市高一(下)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共10小題,每小題3分,共30分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.明代李時珍的《本草綱目》中關于燒酒有如下記載:“近時惟以糯米,或粳米,或黍,或林,或大麥蒸熟,和曲釀翁中七日,以甑蒸取。”下列說法錯誤的是( )
A.糯米、粳米、大麥等谷物中均含有淀粉 B.古法釀酒工藝中有多種酶參與催化反應 C.酒化酶將葡萄糖轉化為乙醇時,溫度越高反應速率一定越快 D.“以甑蒸取”過程中涉及蒸餾操作 組卷:16引用:2難度:0.7 -
2.科技改變生活。下列說法錯誤的是( )
A.北京冬奧會火炬“飛揚”的外殼由碳纖維復合材料制成,具有“輕、固、美”的特點 B.“奮斗者”號載人潛水器成功坐底,深度10909m,所用的合金潛孔鉆頭硬度與熔、沸點均此其單一組分高 C.“雷霆之星”速滑服采用銀離子抗菌技術,可有效防護細菌侵入 D.國產大飛機C919用到的氮化硅陶瓷,該陶瓷屬于新型無機非金屬材料 組卷:8引用:2難度:0.6 -
3.下列有機物的化學用語正確的是( )
A.羥基的電子式: 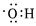
B.聚氯乙烯的結構簡式: 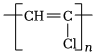
C.四氯化碳的電子式 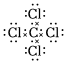
D.比例模型  可表示CH4分子,也可表示CCl4分子組卷:10引用:2難度:0.7
可表示CH4分子,也可表示CCl4分子組卷:10引用:2難度:0.7 -
4.H2(g)+2ICl(g)→2HCl(g)+I2(g)能量曲線如圖。描述正確的是( )

A.反應①為放熱反應,反應②為吸熱反應 B.若加入催化劑可降低反應熱 C.熱化學方程式為H2(g)+2ICl(g)=2HCl(g)+I2(g),ΔH=+218kJ/mol D.若反應的生成物為2HCl(g)+I2(s),則反應熱數值將變大 組卷:18引用:1難度:0.6 -
5.下列關于物質關系的說法不正確的是( )
A.1H和2H屬于同位素 B.HOCH2-CH2OH和CH3OH屬于同系物 C.金剛石和石墨屬于同素異形體 D.正丁烷和異丁烷屬于同分異構體 組卷:15引用:2難度:0.9 -
6.NA表示阿伏加德羅常數的值。下列敘述正確的是( )
A.1mol甲基中所含有的電子數為9NA B.標準狀況下,2.24L己烷所含有的碳原子數為0.6NA C.5.6g鐵與足量氯氣反應轉移電子數為0.2NA D.1molCH3CH2COOH和2molCH3OH在濃硫酸作用下反應生成的酯分子數為NA 組卷:24引用:2難度:0.6
三、非選擇題:(沒有特別說明條件下每空2分,共54分)
-
17.我國向世界鄭重承諾力爭在2030年前實現碳達峰,在2060年前實現碳中和。在實現碳達峰和碳中和的過程中化學發揮著重要的作用。
Ⅰ.以TiO2為催化劑的光熱化學循環分解CO2的反應:2CO2(g)=2CO(g)+O2(g)為溫室氣體減排提供了一個新途徑,該反應轉化過程及各分子化學鍵完全斷裂時的能量變化如圖所示: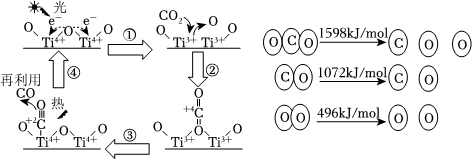
(1)根據數據計算,2CO2(g)=2CO(g)+O2(g),△H=kJ/mol
(2)將一氧化碳與氧氣的反應設計成燃料電池,工作原理如圖所示,該裝置中電解質為氧化釔-氧化鈉,其中O2-可以在固體介質NASICON中自由移動。
工作時,負極電極反應式
Ⅱ.科學家開發高效多功能催化劑,高選擇性利用CO2和H2制備CH4,實現廢舊物資循環利用。反應原理是CO2(g)+4H2(g)?CH4(g)+2H2O(g)。
(1)在恒溫恒容條件下充入CO2和H2發生上述反應。
①下列情況表明該反應已達到平衡狀態的是(填標號)。
A.混合氣體的密度不隨時間變化
B.混合氣體的總壓強不隨時間變化
C.混合氣體的平均摩爾質量不隨時間變化
D.CH4和H2O(g)的濃度之比不隨時間變化
②其他條件相同,只改變下列一個條件,能提高CH4生成速率的是(填標號)。
A.降低溫度
B.再充入H2
C.充入N2
D.及時移走部分H2
(2)在恒容密閉容器中充入一定量CO2和H2發生上述反應,測得一定時間內CO2的轉化率與催化劑Cat1、Cat2以及溫度的關系如圖,催化效率較高的是(填“Cat1”或“Cat2”),理由是。
(3)在某溫度下,向一容積為2L的恒容密閉容器中充入1molCO2和4molH2,發生上述反應,測得氣體總壓強變化如圖。
0~10min內,v(H2)=mol?L-1?min-1;0~5min內v(H2)(填“大于”“小于”或“等于”)5~10min內v(H2)。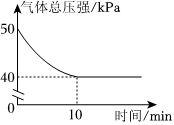 組卷:14引用:2難度:0.6
組卷:14引用:2難度:0.6 -
18.下列關系圖中(部分反應產物可能略去),A是一種氣態烴,其密度在標準狀況下是H2的14倍,C與F以物質的量之比2:1反應生成G。
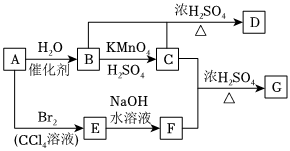
已知反應:R-X+NaOH(ag)R-OH+NaX(R代表烴基,X代表鹵素原子)△
(1)A生成B的反應類型是反應,C的化學名稱為。
(2)寫出F所含官能團的名稱。
(3)寫出D的結構簡式。
(4)寫出A生成B的化學方程式。
寫出C與F反應生成G的化學方程式。
(5)H和B為相對分子質量相差28的同系物,且H發生催化氧化反應可以氧化成醛,則H的同分異構體有種。組卷:12引用:2難度:0.6


