2020-2021學年安徽師大附中高二(下)月考化學試卷(3月份)
發布:2024/11/2 22:30:2
一、單選題(本大題有20小題,每小題3分,共60分)
-
1.下列說法正確的是( )
A.烷烴的通式為CnH2n+2,隨n的增大,碳元素的質量分數逐漸減小 B. 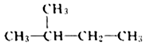 和
和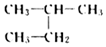 互為同分異構體
互為同分異構體C.丙烷的比例模型為 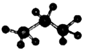
D.分子式為C2H6和分子式為C5H12的烷烴的一氯代物的數目可能相同 組卷:167引用:6難度:0.7 -
2.丁烷廣泛應用于家用液化石油氣,下列敘述中不正確的是( )
A.CH3CH2CH2CH3分子中四個碳原子排列成一條直線 B.C4H10 與C5H12互為同系物 C.丁烷在常溫下是氣體 D.C4H10的一氯代物有4種 組卷:18引用:1難度:0.8 -
3.有4種碳架如下的烴,下列說法正確的是( )
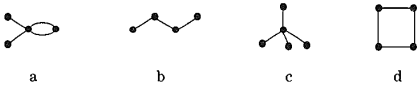
A.a和d都能使KMnO4褪色 B.b和c是同系物 C.a和b都能發生加成反應 D.只有b和c能發生取代反應 組卷:17引用:2難度:0.5 -
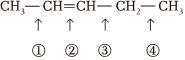 4.已知:2R1-14CH=CH-R2→R1-14CH=CH-R1+R2-14CH=CH-R2,則CH3-CH=CH-CH2-CH3發生此類反應時斷裂的化學鍵是( )
4.已知:2R1-14CH=CH-R2→R1-14CH=CH-R1+R2-14CH=CH-R2,則CH3-CH=CH-CH2-CH3發生此類反應時斷裂的化學鍵是( )A.①③ B.①④ C.② D.②③ 組卷:10引用:3難度:0.7 -
5.有機物的結構可用“鍵線式”簡化表示,如CH3-CH=CH-CH3可簡寫為
 .有機物X的鍵線式為
.有機物X的鍵線式為 ,下列說法中不正確的是( )
,下列說法中不正確的是( )A.X的化學式為C8H8 B.有機物Y是X的同分異構體,且屬于芳香烴,則Y的結構簡式為 
C.X能使酸性高錳酸鉀溶液褪色 D.X與足量的H2在一定條件下反應可生成環狀的飽和烴Z,Z的一氯代物有4種 組卷:43引用:10難度:0.9 -
6.下列說法正確的是( )
A.乙烯能使溴水和酸性高錳酸鉀溶液褪色,其褪色原理相同 B.甲烷與氯氣在光照條件下的反應屬于置換反應 C.工業上可以通過乙烯與氯氣發生加成反應制取氯乙烷 D.除去乙烷中的乙烯得到純凈的乙烷,可依次通過KMnO4(H+)溶液、NaOH溶液和H2SO4(濃) 組卷:15引用:2難度:0.7 -
7.下列說法正確的是(NA表示阿伏加德羅常數)( )
A.1mol 聚乙烯含有的原子數目為6NA B.20℃時,1L己烷完全燃燒后恢復至原狀態,生成氣態物質分子數為 6NA22.4C.2.8g乙烯和丙烯的混合氣體中所含碳原子數為0.2NA D.1mol甲基含10NA個電子 組卷:12引用:1難度:0.7 -
8.把m molC2H4和n molH2混合于密閉容器中,與適當的條件下生成了PmolC2H6.若將所得的混合氣體完全燃燒生成CO2和H2O,需要O2( )
A.3Pmol B.(m+n)mol C.(m+ +3P)moln2D.(3m+ )moln2組卷:24引用:3難度:0.7
二、填空題
-
 23.乙苯是重要的化工產品。某課題組擬制備乙苯:
23.乙苯是重要的化工產品。某課題組擬制備乙苯:
查閱資料如下:有機物 苯 溴乙烷 乙苯 沸點/℃ 80 38.4 136.2
①幾種有機物的沸點:
②化學原理: +CH3CH2BrAlCl380℃
+CH3CH2BrAlCl380℃ +HBr
+HBr
③氯化鋁易升華、易潮解
步驟1:連接裝置并檢查氣密性(如圖所示夾持裝置省略)。
步驟2:用酒精燈微熱燒瓶。
步驟3:在燒瓶中加入少量無水氯化鋁、適量的米和溴乙烷。
步驟4:加熱.充分反應半小時。
步驟5:提純產品。
(1)步驟2:“微熱”燒瓶的日的是。
(2)本實驗步驟4的加熱方式宜采用。
(3)盛有蒸餾水的H裝置中干燥管的作用是。確認本裝置G中已發生反應的方法是。
(4)提純產品的操作步驟有:
①過濾;
②用稀鹽酸;
③用少量蒸餾水清洗;
④加入大量無水氯化鈣;
⑤用大量水洗;
⑥蒸餾并收集136.2℃餾分。
先后操作順序為。(填序號)組卷:3引用:1難度:0.7 -
24.釩具有廣泛用途。黏土釩礦中,釩以+3、+4、+5價的化合物存在,還包括鉀、鎂的鋁硅酸鹽,以及SiO2、Fe3O4。采用如圖工藝流程可由黏土釩礦制備NH4VO3。
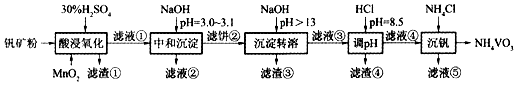
該工藝條件下,溶液中金屬離子開始沉淀和完全沉淀的pH如下表所示。
回答下列問題:金屬離子 Fe3+ Fe2+ Al3+ Mn2+ 開始沉淀pH 1.9 7.0 3.0 8.1 完全沉淀pH 3.2 9.0 4.7 10.1
(1)“酸浸氧化”需要加熱,其原因是。
(2)“酸浸氧化”中,VO+和VO2+被氧化成VO2+,同時還有離子被氧化。寫出VO+轉化為VO2+反應的離子方程式。
(3)“中和沉淀”中,釩水解并沉淀為V2O5?xH2O,隨濾液②可除去金屬離子K+、Mg2+、Na+、,以及部分的。
(4)“沉淀轉溶”中,V2O5?xH2O轉化為釩酸鹽溶解。濾渣③的主要成分是。
(5)“調pH”中有沉淀生產,生成沉淀反應的化學方程式是。
(6)“沉釩”中析出NH4VO3晶體時,需要加入過量NH4Cl,其原因是。組卷:979引用:5難度:0.5


