2023-2024學年天津二十一中高三(上)期中化學試卷
發布:2024/10/10 2:0:2
一、選擇題:(共12題,每題只有一個正確答案)
-
1.化學與生產、生活及環境密切相關,下列說法錯誤的是( )
A.江河入海口形成的三角洲與膠體聚沉有關 B.葡萄酒中通常含有微量SO2,既可以殺菌又可以防止營養成分被氧化 C.“碳九”(石油煉制中獲取的九個碳原子的芳烴)均屬于苯的同系物 D.國產飛機C919用到的氮化硅陶瓷是新型無機非金屬材料 組卷:14引用:1難度:0.7 -
2.下列有關物質的性質與用途具有對應關系的是( )
A.Al2O3熔點較高,可用于制耐火材料 B.FeCl3具有酸性,可用于蝕刻線路板上的銅 C.氨氣具有還原性,可用作制冷劑 D.四氯化碳密度比水大,可用于碘水中的碘萃取劑 組卷:23引用:2難度:0.6 -
3.硫和氮及其化合物對人類生存和社會發展意義重大,但也造成了不少環境問題,下列說法正確的( )
A.雷雨天氣空氣中的少量N2可轉化為NO2并隨雨水落下 B.PM2.5(微粒直徑約為2.5×10-6m)含氮分散質分散在空氣中形成氣溶膠,能產生丁達爾效應 C.二氧化硫有毒,嚴禁將其添加到任何食品和飲品中 D.“酸雨”是由大氣中的碳、氮、硫的氧化物溶于雨水造成的 組卷:82引用:5難度:0.5 -
 4.含硫煤燃燒會產生大氣污染物,為防治該污染,某工廠設計了新的治污方法,同時可得到化工產品,該工藝流程如圖所示,下列敘述不正確的是( )
4.含硫煤燃燒會產生大氣污染物,為防治該污染,某工廠設計了新的治污方法,同時可得到化工產品,該工藝流程如圖所示,下列敘述不正確的是( )A.該過程中可得到化工產品H2SO4 B.該工藝流程是除去煤燃燒時產生的SO2 C.該過程中化合價發生改變的元素只有O和S D.圖中涉及的反應之一為:Fe2(SO4)3+SO2+2H2O═2FeSO4+2H2SO4 組卷:60引用:6難度:0.7 -
5.用溶質質量分數為98%的濃硫酸(ρ=1.84g?cm-3)配制240mL1.84mol?L-1稀硫酸,下列操作正確的是( )
A.將蒸餾水緩慢注入盛有一定量濃硫酸的燒杯中,并不斷攪拌至冷卻 B.必須的定量儀器有250mL容量瓶和托盤天平 C.量取濃硫酸的體積為25.0mL D.先在容量瓶中加入適量水,將量好的濃硫酸注入容量瓶,加水定容 組卷:36引用:2難度:0.7
二、非選擇題:(共4題)
-
15.(1)K2FeO4為紫色固體,易溶于水,微溶于KOH溶液,不溶于乙醇;有強氧化性,在0℃~5℃的強堿性溶液中較穩定,在酸性或中性溶液中快速產生O2。
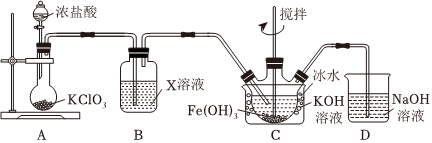
①A中發生反應的離子反應方程式是。
②下列試劑中,裝置B的X溶液可以選用的是。
A.飽和食鹽水
B.濃鹽酸
C.飽和氯水
D.NaHCO3溶液
③C中得到紫色固體和溶液,生成K2FeO4的化學方程式是;若要從反應后的裝置C中盡可能得到更多的K2FeO4固體,可以采取的一種措施是。
(2)高鐵酸鉀與水反應的離子方程式是
4+10H2O═4Fe(OH)3(膠體)+3O2↑+8OH-。FeO2-4
則其作為水處理劑的原理是①,②。
(3)某同學設計如圖裝置制備一定量的Fe(OH)2,并使其能在較長時間內存在。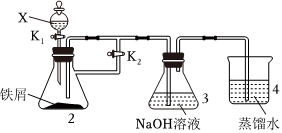
①X不能是硝酸,原因是,裝置4的作用是。
②實驗開始時,開關K2應(填“打開”成“關閉”);這樣操作的目的是。組卷:55引用:3難度:0.4 -
16.某實驗小組欲探究NaHCO3和Na2CO3的性質,發現實驗室里盛放兩種固體的試劑瓶丟失了標簽.于是,他們先對固體A、B進行鑒別,再通過實驗進行性質探究.
(1)分別加熱固體A、B,發現固體A受熱產生的氣體能使澄清石灰水變渾濁.A受熱分解的化學方程式.
(2)稱取兩種固體各2g,分別加入兩個小燒杯中,再各加10mL蒸餾水,振蕩,測量溫度變化;待固體充分溶解,恢復至室溫,向所得溶液中各滴入2滴酚酞溶液.
①發現Na2CO3固體完全溶解,而NaHCO3固體有剩余,由此得出結論:.
②同學們在兩燒杯中還觀察到以下現象.其中,盛放Na2CO3的燒杯中出現的現象是.(填字母序號)
a.溶液溫度升高
b.溶液溫度下降
c.滴入酚酞后呈淺紅色
d.滴入酚酞后呈紅色
(3)如圖所示,在氣密性良好的裝置Ⅰ和Ⅱ中分別放入藥品,將氣球內的固體同時倒入試管中.
①兩試管中均產生氣體,(填“Ⅰ”或“Ⅱ”)的反應程度更為劇烈.
②反應結束后,恢復至室溫,下列說法正確的是.
a.裝置Ⅰ的氣球體積較大
b.裝置Ⅱ的氣球體積較大
c.生成氣體的體積根據鹽酸計算
d.生成氣體的體積根據固體計算
(4)同學們將兩種固體分別配制成0.5mol?L-1的溶液,設計如下方案并對反應現象做出預測:實施實驗后,發現操作1的現象與預測有差異:產生白色沉淀和二氧化碳氣體.則該條件下,NaHCO3溶液與CaCl2溶液反應的離子方程式為.實驗方案 預測現象 預測依據 操作1:向2mL NaHCO3溶液中滴加1mL 0.5mol?L-1CaCl2溶液 無白色沉淀 NaHCO3溶液中的 濃度很小,不能與CaCl2反應.CO2-3操作2:向2mL Na2CO3溶液中滴加1mL 0.5mol?L-1CaCl2溶液 有白色沉淀 Na2CO3溶液中的 濃度較大,能與CaCl2發生反應CO2-3(寫出該反應的離子方程式).組卷:137引用:2難度:0.6


