2023年吉林省吉林市高考化學二模試卷
發布:2024/4/20 14:35:0
一、選擇題(每小題只有一個正確答案,1-10每題2分,11-20每題3分,共50分)
-
1.開發和利用自然資源,必須遵循減量化、再利用和再循環的原則,踐行綠色發展理念。下列做法不值得提倡的是( )
A.選用一次性筷子、紙杯和塑料袋 B.選用回收廢紙制造的紙箱 C.將生活垃圾進行分類處理 D.選乘公共交通工具出行 組卷:11引用:2難度:0.6 -
2.氫能是公認的低碳、綠色清潔能源,氫能開發中一個重要問題是如何制取氫氣。以下研究方向你認為不可行的是( )
A.建設水電站,用電力分解水制取氫氣 B.尋找更多的化石燃料,利用其燃燒放熱,使水分解產生氫氣 C.設法將太陽光聚焦,產生高溫,使水分解產生氫氣 D.尋找特殊的化學物質作催化劑,用于分解水制取氫氣 組卷:24引用:1難度:0.7 -
3.下列物質中,水解的最終產物可以發生銀鏡反應的是( )
A.蔗糖 B.乙酸乙酯 C.油脂 D.蛋白質 組卷:196引用:7難度:0.8 -
4.下列化學用語表示錯誤的是( )
A.次氯酸的電子式: 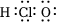
B.丙烷的球棍模型: 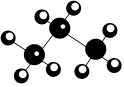
C.鈉原子的原子結構示意圖: 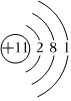
D.原子核內有10個中子的氧原子: O188組卷:26引用:2難度:0.6 -
5.下列氣體中,既可用濃硫酸干燥,又可用堿石灰固體干燥的是( )
A.Cl2 B.NH3 C.SO2 D.H2 組卷:16引用:3難度:0.7 -
6.設NA為阿伏加德羅常數的值。下列說法正確的是( )
A.7.8gNa2O2中所含陰離子數為0.1NA B.1molFeCl3完全反應制成膠體后,其中含有氫氧化鐵膠粒數為NA C.1molN2和3molH2在一定條件下充分反應生成的NH3分子數為2NA D.常溫下pH=2的醋酸溶液中含有的氫離子數為0.1NA 組卷:29引用:1難度:0.7 -
7.用下列實驗裝置完成對應的實驗(部分儀器已省略),能達到實驗目的的是( )
A B C D 裝置 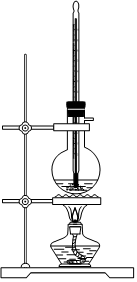
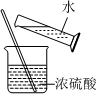
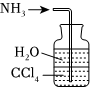
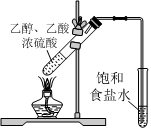
A.蒸餾海水制淡水 B.稀釋濃H2SO4 C.吸收NH3 D.制取乙酸乙酯 組卷:25引用:2難度:0.5 -
8.下列生產活動中涉及的化學原理正確的是( )
選項 生產活動 化學原理 A 使用碳納米管、石墨烯制作新型電池 碳納米管、石墨烯均可燃燒生成CO2 B 侯氏制堿法得到NaHCO3沉淀 NaHCO3溶解度較小 C 利用FeCl3溶液刻蝕印刷電路板 Fe的活動性比Cu強 D 常溫下,可以利用鋼瓶儲存濃H2SO4 常溫下濃H2SO4與Fe不反應 A.A B.B C.C D.D 組卷:23引用:2難度:0.6
二、非選擇題(本大題共4個小題,共50分)
-
23.氮元素在地球上含量豐富,氮及其化合物在工農業生產和生活中有著重要作用。有資料顯示過量的氨氣和氯氣在常溫下可合成巖腦砂(主要成分為NH4Cl),某實驗小組利用下列裝置,制備干燥純凈的氨氣和氯氣并合成巖腦砂的反應進行探究。回答下列問題:

(1)裝置C的名稱是。
(2)裝置A中發生反應的化學方程式為。
(3)裝置E中濃硫酸的作用是。
(4)為了使氨氣和氯氣在D中充分混合,上述裝置的合理連接順序為:a→←b(用小寫字母填寫儀器接口順序)。
(5)檢驗生成物中陽離子的操作方法為。組卷:81引用:3難度:0.7 -
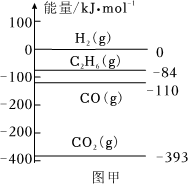 24.清潔能源的綜合利用以及二氧化碳的研發利用,可有效降低碳排放,均是實現“碳達峰、碳中和”的重要途徑,我國力爭于2030年前做到碳達峰,2060年前實現碳中和。
24.清潔能源的綜合利用以及二氧化碳的研發利用,可有效降低碳排放,均是實現“碳達峰、碳中和”的重要途徑,我國力爭于2030年前做到碳達峰,2060年前實現碳中和。
Ⅰ.利用反應:2CO2(g)+C2H6(g)?4CO(g)+3H2(g)可減少CO2的排放。
(1)CO2的結構式為,C2H6分子中極性鍵與非極性鍵的個數比為。
(2)圖甲是298K時相關物質的相對能量,則上述反應的ΔH=kJ/mol。
(3)下列關于該反應的說法錯誤的是。
a.在恒容絕熱的條件下,溫度不再改變,說明該反應已達平衡狀態
b.在恒溫恒壓的條件下,充入稀有氣體氦氣,平衡不移動
c.平衡向右移動,平衡常數K一定增大
d.該反應在高溫條件下自發
(4)該反應的凈反應速率方程:v=k正c2(CO2)?c(C2H6)-k逆c4(CO)?c3(H2)(k正、k逆為速率常數,只與溫度、催化劑、接觸面積有關,與濃度無關)。溫度為T1℃時,k正=0.4k逆,溫度為T2℃時,k正=1.6k逆,則T1T2(填“>”、“<”或“=”)。
Ⅱ.乙烯的產量是衡量一個國家石油化工發展水平的標準。國內第一套自主研發的乙烷裂解制乙烯的大型生產裝置建成。已知該項目中乙烷制乙烯的反應原理為:
主反應:C2H6(g)?CH2=CH2(g)+H2(g)
副反應:2C2H6(g)?CH2=CH2(g)+2CH4(g)
在一定溫度下,在2L恒容密閉容器中充入7molC2H6。進行反應,達到平衡時CH4和H2的體積分數均為20%,則:
(5)乙烷的總轉化率為(保留4位有效數字)。
(6)該溫度下主反應的平衡常數K為mol/L。組卷:46引用:3難度:0.6


