2020-2021學年湖南省長沙市雅禮教育集團高二(下)期末化學試卷
發布:2024/12/28 19:30:2
一、選擇題(本題共14小題,每題2分,共28分,每小題只有一個選項正確。)
-
1.我國大力弘揚中華優秀傳統文化體現“文化自信”。下列有關說法錯誤的是( )
A.制備“白玉金邊素瓷胎,雕龍描鳳巧安排”中的瓷,主要原料為黏土 B.商代后期鑄造出了工藝精湛的司母戊鼎,該鼎屬于銅合金制品 C.成語“百煉成鋼”、“沙里淘金”中均包含了化學變化 D.《本草綱目》中有關于釀酒的記載“凡酸壞之酒,皆可蒸燒”,其描述的過程是蒸餾 組卷:47引用:5難度:0.7 -
2.下列陳述正確并且有因果關系的是( )
A.SiO2有導電性,可用于制備光導纖維 B.NaHCO3能與堿反應,可用作焙制糕點的膨松劑 C.Al2O3具有很高的熔點,可用于制造熔融燒堿的坩堝 D.FeCl3溶液能與Cu反應,可用于蝕刻印刷電路板 組卷:1引用:2難度:0.8 -
3.某溶液中含有CH3COO-、
、SO2-4、SO2-3、HCO-3等五種離子.將過量的Na2O2固體加入其中后,仍能大量存在的離子是( )CO2-3A.CH3COO-、 、SO2-4HCO-3B. 、SO2-4、SO2-3CO2-3C. 、SO2-3HCO-3D.CH3COO-、 、SO2-4CO2-3組卷:6引用:2難度:0.7 -
4.安全是順利進行實驗及避免傷害的保障。下列實驗操作正確且不是從實驗安全角度考慮的是( )
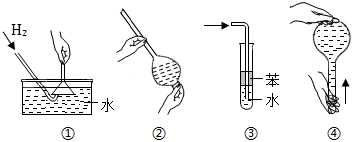
A.操作①:使用稍浸入液面下的倒扣漏斗檢驗氫氣的純度 B.操作②:使用CCl4萃取溴水中的溴時,振蕩后需打開活塞使漏斗內氣體放出 C.操作③:吸收氨氣或氯化氫氣體并防止倒吸 D.操作④:用食指頂住瓶塞,另一只手托住瓶底,把瓶倒立,檢查容量瓶是否漏水 組卷:167引用:21難度:0.9 -
5.氫氧化銅和堿式碳酸銅[Cu2(OH)2CO3]均可溶于鹽酸轉化為氯化銅.在高溫下這兩種化合物均能分解生成氧化銅.溶解25.25g上述混合物,恰好消耗1.0 mol?L-1 鹽酸500mL.灼燒等量的上述混合物,得到的氧化銅質量為( )
A.15 g B.20 g C.30 g D.35 g 組卷:78引用:5難度:0.7 -
6.下列離子方程式中能正確表達反應現象的是( )
A.向偏鋁酸鈉溶液中加入小蘇打溶液,出現白色沉淀:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32- B.酸性KMnO4溶液滴入雙氧水中,得到無色溶液:2MnO4++H2O2+6H+═2Mn2++3O2↑+4H2O C.將鐵棒和銅棒靠緊插入AgNO3溶液中,銅棒表面附著銀白色金屬:2Ag++Cu═Ag+Cu2+ D.NaClO溶液中通入過量的SO2,溶液酸性增強:ClO-+SO2+H2O═HClO+HSO3- 組卷:0引用:1難度:0.6 -
7.設NA為阿伏加德羅常數的值,下列敘述正確的數目有( )
①46g NO2和N2O4混合氣體中含有的原子數為3NA
②標準狀況下22.4L H2中含有的中子數為2NA
③1mol C10H22分子中共價鍵總數為31NA
④1mol Mg與足量O2或N2反應生成MgO或Mg3N2均失去2NA電子
⑤9g重水(D2O)所含有的電子數為5NA
⑥1L 1mol/L的MgCl2溶液中含有的離子數為2NAA.2個 B.3個 C.4個 D.5個 組卷:0引用:1難度:0.9
三、非選擇題(本題包括4小題,共56分)
-
21.氯化亞砜(SOCl2)在科研和工業上應用比較廣泛。回答下列問題:
Ⅰ.工業上利用尾氣SO2與SCl2、Cl2反應合成氯化亞砜。發生如下反應:
①Cl2(g)+SO2(g)?SO2Cl2(g)△H=-471.7kJ?mol-1
②SO2Cl2(g)+SCl2(g)?2SOCl2(g)△H=-5.6kJ?mol-1
567K時,在10L密閉容器中,充入一定量的Cl2、SO2和SCl2,測得初始壓強為p0,反應過程中容器內總壓強(p)隨時間(t)變化(反應達到平衡時的溫度與初始溫度相同)如圖1所示,起始各組分及達平衡時SO2Cl2(g)的物質的量如表。各組分 Cl2 SO2 SCl2 SO2Cl2 SOCl2 起始/mol 0.5 0.5 0.5 0 0 平衡/mol 0.2 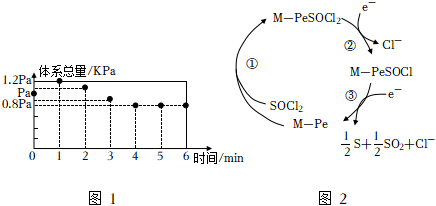
(1)0~1min,圖中數據顯示體系壓強增大的原因是。
(2)0~4min內,v(Cl2)=mol?L-1?min-1,5min時SCl2的轉化率為。
(3)567K時,上述反應②的KP=。
(4)567K下,若擴大容器體積為20L,則平衡時c(SO2)(填“大于”“小于”或“等于”)上述反應平衡時的c(SO2)。
Ⅱ.Li/SOCl2電池是一種高比能量電池,電解液為非水的LiAlC14的SOCl2溶液。正極為金屬酞菁配合物(M-Pe,電池正極催化劑)附著的碳棒。正極催化過程為:SOCl2先與酞菁形成加合物,接著發生加合物的兩步快速的電子轉移,過程如圖2所示。
(5)上述正極催化過程M-PeSOCl2為(填“催化劑”或“中間產物”),放電過程中每轉移1mol電子生成g硫單質。電池總反應的化學方程式為。組卷:11引用:2難度:0.6 -
22.某研究小組以有機物A為原料,合成抗癌藥--拉帕替尼的中間體H的具體路線如圖
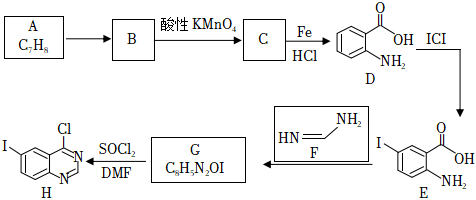
已知:
①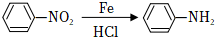
②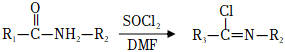
回答下列問題:
(1)C的名稱為。D中所含官能團的名稱為。G的結構簡式為。
(2)B→C的反應類型為。
(3)A分子中共面原子數最多為。
(4)A→B的化學方程式為。
(5)碳原子上連有4個不同原子或基團時,該碳原子為手性碳原子。寫出D與足量H2反應后產物的結構簡式,并用星號(*)標出其中的手性碳原子。
(6)C有多種同分異構體,其中滿足下列條件的同分異構體共有種。
①分子中含有苯環;②分子中含有-NO2(不考慮-O-NO2);③能發生銀鏡反應
其中核磁共振氫譜有3組峰,并且峰面積之比為1:2:2的有機物結構簡式為。組卷:16引用:3難度:0.5


