2021年湖北省武漢市漢陽一中高考化學仿真模擬試卷(六)
發布:2024/4/20 14:35:0
一、選擇題:本題共15小題,每小題3分,共45分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.“嫦娥五號”成功著陸月球,實現了中國首次月球無人采樣返回。下列說法錯誤的是( )
A.運載火箭使用了煤油液氧推進劑,其中煤油是由石油分餾獲得 B.探測器裝有太陽能電池板,其主要成分為二氧化硅 C.上升器用到碳纖維復合材料,主要利用其質輕、強度大和耐高溫性能 D.返回器帶回的月壤中含有3He,與地球上的4He互為同位素 組卷:32引用:1難度:0.8 -
2.某放射性核衰變的過程為
X→14ZY+14Z+1e, 其中第二周期元素X、Y的原子的最外層電子數之和為9。下列有關說法正確的是( )0-1A.該過程為物理變化 B. X原子的中子數為714ZC.X、Y只存在兩種氧化物 D.考古時可利用 X測定一些文物的年代14Z組卷:51引用:1難度:0.4 -
3.已知NA為阿伏加德羅常數的值,下列說法正確的是( )
A.1mol N2與3mol H2反應生成的NH3分子數為2NA B.標準狀況下,22.4L CHCl3中所含C—Cl鍵的數目為3NA C.足量MnO2和80mL 10mol/L濃鹽酸共熱可生成0.2NA個Cl2分子 D.反應5NaClO2+4HCl═4ClO2↑+5NaCl+2H2O,每生成1molClO2轉移電子的數目為NA 組卷:143引用:1難度:0.4 -
4.下列指定反應的方程式正確的是( )
A.在煤中添加石灰石,降低尾氣中SO2濃度:2CaCO3+2SO2+O2 2CaSO4+2CO2加熱B.用小蘇打溶液涂抹蚊蟲叮咬產生蟻酸(HCOOH)處:H++HCO3-═H2O+CO2↑ C.生活中用碳酸鈉做洗滌劑的原理:CO32-+2H2O═H2CO3+2OH- D.用鐵電極電解飽和食鹽水:2Cl-+2H2O 2OH-+Cl2↑+H2↑通電組卷:80引用:1難度:0.6 -
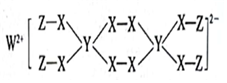 5.2020年某科研團隊發現一種新型漂白劑(結構如圖),其組成元素均為短周期元素,W與X對應的簡單離子的核外電子排布相同,W、Y、Z為不同周期的主族元素,且W、Y、Z最外層電子數之和等于X的最外層電子數,下列說法錯誤的是( )
5.2020年某科研團隊發現一種新型漂白劑(結構如圖),其組成元素均為短周期元素,W與X對應的簡單離子的核外電子排布相同,W、Y、Z為不同周期的主族元素,且W、Y、Z最外層電子數之和等于X的最外層電子數,下列說法錯誤的是( )A.四種元素中X的電負性最大 B.X和Z組成的分子均為非極性分子 C.簡單離子半徑Z<W<X D.Y對應的最高價氧化物對應的水化物是一元弱酸 組卷:61引用:1難度:0.5 -
6.在紫外線的作用下,CF2Cl2可解離出氯原子,氯原子破壞臭氧層的原理如圖所示。下列說法正確的是( )
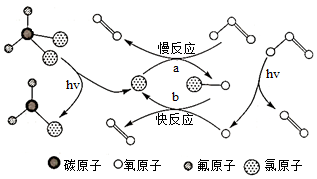
A.一氧化氯自由基是臭氧分解過程的催化劑 B.反應a的活化能低于反應b的活化能 C.臭氧分解的化學方程式可表示為:2O3 3O2氯原子hvD.CF2Cl2分子的空間構型是正四面體形 組卷:33引用:8難度:0.7
二、解答題(共4小題,滿分55分)
-
18.氮氧化物氣體是造成光化學污染的主要氣體,降低氮氧化物氣體的排放是環境保護的重要課題。已知汽車尾氣中的氮氧化物氣體主要涉及如下反應:
ⅰ.N2(g)+O2(g)?2NO(g)△H=+180.5kJ?mol-1;
ⅱ.2NO(g)+O2(g)?2NO2(g)△H=-114.0kJ?mol-1;
ⅲ.2NO2(g)?N2O4(g)△H=-52.7kJ?mol-1。
回答下列問題:
(1)該條件下,N2中N≡N鍵的鍵能為916.5kJ?mol-1,O2中O=O鍵的鍵能為458.0kJ?mol-1,則NO中化學鍵的鍵能為。
(2)向某剛性密閉容器中充入等量的N2和O2,一定溫度下發生上述3個反應。
①下列狀態能說明上述反應達到平衡狀態的是(填字母)。
a.NO濃度不再變化
b.混合氣體的顏色不再變化
c.混合氣體的密度不再變化
d.每消耗2molNO2,同時消耗1molN2O4。
②若起始時容器內總壓強為p1kPa,10s時容器內3個反應達到平衡狀態,此時的總壓強和N2O4的分壓分別為p2kPa和p3kPa;則前10s內N2O4的平均生成速率為kPa?s-1,該溫度下反應ⅲ的平衡常數Kp=kPa-1。
③若升高溫度,平衡體系中NO的體積分數(填“增大”“減小”或“無法確定”),原因為。
(3)反應6NO(g)+4NH3(g)?5N2(g)+6H2O(g)△H<0,是工業上處理氮氧化物的方法之一。向某密閉容器中投入等量的NO和NH3發生上述反應,平衡時,NO和H2O的物質的量隨溫度的變化如圖所示。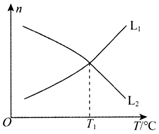
①圖中代表NO物質的量變化的曲線為。
②T1℃下,N2的平衡體積分數為。組卷:99引用:2難度:0.7 -
19.2021年5月,中國空間站“天和”核心艙成功入軌,該核心艙搭載全球最先進的柔性三極砷化鎵太陽能電池陣,現以砷化鎵廢料(主要成分為GaAs,含Fe2O3、SiO2和CaCO3等雜質)中回收鎵(與Al同主族,化學性質相似)和砷,工藝流程如下:
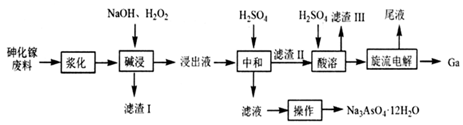
回答下列問題:
(1)“漿化”是將砷化鎵廢料轉變成懸濁液的過程,其目的是。
(2)砷化鎵(GaAs)在“堿浸”時,砷轉化為Na3AsO4進入溶液,該反應的化學方程式為。
(3)“堿浸”的溫度控制在70℃左右,溫度不能過高或過低的原因是;“濾渣I”的成分為(填化學式)。
(4)向浸出液中加H2SO4進行“中和”,調節pH使鎵和硅共沉淀,不同pH時沉淀率如下表所示。根據表中數據可知,“中和”的pH應調節至范圍內,沉淀的效果最好。
(5)“旋流電解”時用惰性電極,在陰極析出高純度的鎵,請寫出陰極電極反應式:pH 鎵沉淀率/% 硅沉淀率/% 砷沉淀率/% 4.0 75.0 89.2 0.02 5.0 98.5 98.6 0.01 6.0 98.9 99.2 0.02 7.0 95.3 99.5 0.06 8.0 86.1 86.3 0.11 9.0 57.4 65.1 0.13 ,則所得“尾液”的溶質主要是(填化學式),可進行循環利用,提高經濟效益。組卷:38引用:1難度:0.5


