2018-2019學年河南省駐馬店市高二(上)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(共16小題,每小題3分,共48分。每小題只有一個選項符合題意)
-
1.下列物質的水溶液因水解而呈酸性的是( )
A.CuCl2 B.Na2CO3 C.CH3COOH D.KHSO4 組卷:82引用:6難度:0.9 -
2.下列說法不正確的是( )
A.增大反應物濃度,可增大單位體積內活化分子總數,從而使有效碰撞次數增大 B.有氣體參加的化學反應,若增大壓強(即縮小反應容器的體積),可增大活化分子的百分數,從而使反應速率增大 C.升高溫度能使化學反應速率增大的主要原因是增大了反應物分子中活化分子的百分數 D.催化劑能增大單位體積內活化分子的百分數,從而成千成萬倍地增大反應速率 組卷:88引用:7難度:0.9 -
3.一定條件下,可逆反應:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1,達到化學平衡狀態時,下列說法一定正確的是( )
A.c(N2):c(H2)=1:3 B.反應放出92.4 kJ的熱量 C.v正(N2)=3v逆(H2) D.容器內氣體分子總數不再發生變化 組卷:36引用:7難度:0.7 -
4.判斷一個化學反應的自發性常用焓判據和熵判據,則在下列情況下,可以判定反應一定自發進行的是( )
A.△H>0,△S>0 B.△H<0,△S>0 C.△H>0,△S<0 D.△H<0,△S<0 組卷:57引用:24難度:0.9 -
5.依據圖判斷,下列說法不正確的是( )
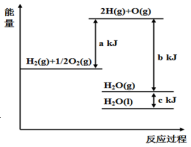
A.1molH2(g)與 molO2(g)所具有的總能量比1molH2O(g)所具有的總能量高12B.H2O(g)生成H2O(l)時,斷鍵吸收的能量小于成鍵放出的能量 C.2molH(g)與1molO(g)生成1molH2O(g)所放出的熱量是bkJ D.液態水分解的熱化學方程式為:2H2O(l)═2H2(g)+O2(g)△H=2(b+c-a)kJ?mol-1 組卷:28引用:8難度:0.7 -
6.下列關于熱化學反應的描述中正確的是( )
A.HCl和NaOH反應的中和熱△H=-57.3kJ?mol-1,則H2SO4和Ca(OH)2反應的中和熱△H=2×(-57.3)kJ?mol-1 B.需要加熱才能發生的反應一定是吸熱反應 C.CO(g)的燃燒熱是283.0kJ?mol-1,則2CO2(g)═2CO(g)+O2(g)反應的△H=+2×283.0kJ?mol-1 D.1 mol甲烷燃燒生成氣態水和二氧化碳所放出的熱量是甲烷的燃燒熱 組卷:46引用:9難度:0.7 -
7.下列敘述中,不能用勒夏特列原理解釋的是( )
A.紅棕色的NO2,加壓后顏色先變深后變淺 B.向橙色K2Cr2O7溶液中加入一定濃度的NaOH溶液后,溶液變為黃色 C.對2HI(g)?H2(g)+I2(g)平衡體系增大壓強使氣體顏色變深 D.溴水中有下列平衡Br2+H2O?HBr+HBrO,當加入AgNO3溶液后,溶液顏色變淺 組卷:48引用:8難度:0.7
二、第Ⅱ卷(非選擇題共52分)
-
20.(1)在25℃下,向濃度均為0.1mol?L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成
沉淀(填化學式),生成該沉淀的離子方程式為.已知25℃時Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20.
(2)向BaCl2溶液中加入AgNO3和KBr,當兩種沉淀共存時,=c(Br-)c(Cl-).[Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10].組卷:87引用:3難度:0.5 -
21.乙二酸俗名草酸,易溶于水,水溶液可以用酸性KMnO4溶液進行滴定:2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O某學習小組的同學設計了如下實驗方法測草酸晶體(H2C2O4?xH2O)中x值。
①稱取1.260g純草酸晶體,將其配制成100.00mL水溶液為待測液;
②取25.00mL待測液放入錐形瓶中,再加入適量的稀H2SO4;
③用濃度為0.1000mol/L的KMnO4標準溶液進行滴定,達到終點時消耗10.00mL;
(1)寫出乙二酸的第一級電離方程式:;
(2)滴定時,KMnO4標準液應裝在式滴定管中;
(3)本實驗滴定達到終點的標志是;
(4)通過上述數據,計算出x=;討論:若滴定終點時俯視滴定管刻度,則由此測得的x值會(填“偏大”、“偏小”或“不變”)。組卷:0引用:1難度:0.5


