2021-2022學年北京五中高一(上)第二次段考化學試卷
發布:2024/10/26 3:30:2
一、選擇題(共14小題,每小題3分,滿分42分)
-
1.藥品“速力菲”中Fe2+會被空氣緩慢氧化,國家規定如果藥物中有超過10%的Fe2+被氧化即不可服用。若要證明該藥品已被氧化,下列試劑能達到實驗目的的是( )
A.新制氯水 B.KSCN溶液 C.酸性KMnO4溶液 D.KCl溶液 組卷:22引用:1難度:0.7 -
2.下列儀器中,配制一定物質的量濃度的溶液時不需要的是( )
A. 
燒杯B. 
容量瓶C. 
膠頭滴管D. 
分液漏斗組卷:12引用:5難度:0.6 -
3.隨著人們對物質組成和性質研究的深入,物質的分類更加多樣化。下列有關說法正確的是( )
A.Na2O2、Al2O3、Fe2O3都是堿性氧化物 B.磁鐵礦、鹽酸、膽礬都是混合物 C.CH3COOH、NH3?H2O、HClO都是弱電解質 D.燒堿、純堿、熟石灰都是堿 組卷:18引用:1難度:0.8 -
4.下列說法正確的是( )
A.膠體區別于其他分散系的本質特征是能發生丁達爾效應 B.合金與各組分金屬相比一般具有更低的熔點 C.生鐵、普通鋼和不銹鋼中的碳含量依次增加 D.因為氯氣溶于水可以導電,所以氯氣是電解質 組卷:13引用:4難度:0.8 -
5.下列推斷正確的是( )
A.鋁粉在氧氣中燃燒生成Al2O3,故鐵絲在氧氣中燃燒生成Fe2O3 B.鐵能從硫酸銅溶液中置換出銅,故鈉也能從硫酸銅溶液中置換出銅 C.鈉與氧氣、水等反應時鈉均作還原劑,故金屬單質參與化學反應時金屬均作還原劑 D.活潑金屬鈉保存在煤油中,故活潑金屬鋁也保存在煤油中 組卷:110引用:8難度:0.7 -
6.下列敘述中正確的是( )
A.NaCl、NaOH和鹽酸都是電解質 B.凡能電離出H+的化合物均屬于酸 C.非金屬氧化物不一定是酸性氧化物,酸性氧化物不一定都是非金屬氧化物 D.將幾滴汽油加入裝有10mL水的試管中,用力振蕩形成膠體 組卷:12引用:2難度:0.8
二、解答題(共5小題,滿分0分)
-
18.我國化學家侯德榜發明的“聯合制堿法”為世界制堿工業做出了巨大貢獻。如圖為聯合制堿法的主要過程(部分物質已略去)。
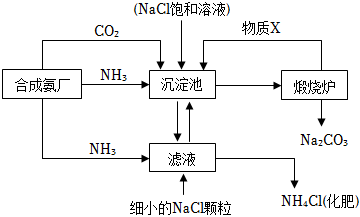
資料:ⅰ.沉淀池中的反應為NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl
ⅱ.溶解度
(1)煅燒爐中反應的化學方程式是物質 NaCl NH4HCO3 NaHCO3 NH4Cl 20℃溶解度/g 36.0 21.7 9.6 37.2 ,物質X是(填化學式)。
(2)下列說法正確的是(填字母)。
A.沉淀池中有NaHCO3析出,因為一定條件下NaHCO3的溶解度最小
B.濾液中主要含有NaCl、Na2CO3和NH4Cl
C.設計循環的目的是提高原料的利用率
(3)工業可用純堿代替燒堿生產某些化工產品,如用飽和純堿溶液與Cl2反應可制得一種在生產生活中常用于漂白、消毒的物質,同時有NaHCO3生成,該反應的化學方程式是。
(4)某純堿樣品中含雜質NaCl,取質量為ag的樣品,加入足量的稀鹽酸,充分反應后,加熱、蒸干、灼燒,得到bg固體物質,則此樣品中Na2CO3的質量分數為。組卷:170引用:8難度:0.7 -
19.一氧化二氯(Cl2O)是一種氯化劑和氧化劑,極易溶于水,與水反應生成HClO,遇有機物易燃燒或爆炸。Cl2O的熔點是-120.6℃,沸點是2.0℃。利用反應2HgO+2Cl2=Cl2O+HgCl2?HgO可制備Cl2O。
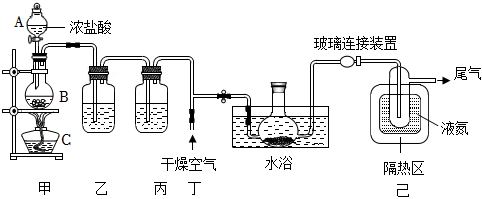
某同學利用如圖裝置制備Cl2O,請回答下列問題:
(1)儀器A的名稱為:;
(2)實驗室常用MnO2固體與濃鹽酸反應制取氯氣,請寫出化學方程式:。
(3)裝置乙中的試劑是;裝置丙的作用是。
(4)反應2HgO+2Cl2=Cl2O+HgCl2?HgO中,每生成0.5molCl2O轉移電子的物質的量為mol。組卷:0引用:1難度:0.5


