2021-2022學(xué)年黑龍江省哈爾濱七十三中高一(上)期末化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(本題含20小題,每題3分,共60分。每題只有一個(gè)選項(xiàng)符合題意)
-
1.下列不能通過氯氣與單質(zhì)直接化合制取的是( )
A.HCl B.CuCl2 C.NaCl D.FeCl2 組卷:22引用:1難度:0.7 -
2.Se是人體必需微量元素,下列有關(guān)
Se和7834Se說法正確的是( )8034A. Se和7834Se是同一種核素8034B. Se和7834Se互為同位素8034C. Se和7834Se分別含有44和46個(gè)質(zhì)子8034D. Se和7834Se都含有34個(gè)中子8034組卷:1098引用:8難度:0.5 -
3.下列含有共價(jià)鍵的物質(zhì)是( )
A.NaCl B.MgCl2 C.H2O D.KI 組卷:22引用:2難度:0.7 -
4.美國和俄羅斯科學(xué)家將大量48Ca離子加速去轟擊人造元素249Cf,從而制造出一種新原子.該原子的原子核包含118個(gè)質(zhì)子和179個(gè)中子。下列有關(guān)該元素的敘述正確的是( )
A.該元素的相對(duì)原子質(zhì)量為297 B.這是一種金屬元素 C.這是一種原子序數(shù)為118的新元素 D.這是一種主族元素 組卷:27引用:1難度:0.9 -
5.下列關(guān)于電解質(zhì)說法正確的是( )
A.能導(dǎo)電的物質(zhì)叫電解質(zhì) B.電解質(zhì)在通電時(shí)發(fā)生電離 C.NaCl晶體不導(dǎo)電,所以NaCl不是電解質(zhì) D.熔融的KOH導(dǎo)電,所以KOH是電解質(zhì) 組卷:113引用:6難度:0.9 -
6.下列說法錯(cuò)誤的是(設(shè)NA為阿伏加德羅常數(shù)的值)( )
A.CH4分子呈正四面體形 B.78g Na2O2晶體中陰陽離子總數(shù)為3NA C.3.4g氨氣中含有N-H鍵的數(shù)目為0.3NA D.1mol Cl2與足量的鐵粉完全反應(yīng),轉(zhuǎn)移的電子數(shù)為2NA 組卷:76引用:3難度:0.8 -
7.下列物質(zhì)性質(zhì)與用途具有對(duì)應(yīng)關(guān)系的是( )
A.NaHCO3受熱易分解,可用于制胃酸中和劑 B.Fe2O3能與酸反應(yīng),可用于制作紅色涂料 C.Na2O2吸收CO2產(chǎn)生O2,可用作呼吸面具供氧劑 D.ClO2具有還原性,可用于自來水的殺菌消毒 組卷:106引用:5難度:0.6
二、填空題(共3小題,滿分40分)
-
22.如表為元素周期表的一部分,請回答有關(guān)問題:
(1)已知元素⑩的一種核素,其中子數(shù)為45,用原子符號(hào)表示該核素為ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0 1 ① 2 ② ③ ④ 3 ⑤ ⑥ ⑦ ⑧ 4 ⑨ ⑩ 。
(2)由元素②和④形成的三核直線形分子的結(jié)構(gòu)式為。
(3)用電子式表示元素⑤和⑦的原子形成的化合物(該化合物含有三個(gè)原子核)的形成過程。
(4)由上述元素④和⑤構(gòu)成的淡黃色固體化合物的電子式為,該化合物所含的化學(xué)鍵類型為(填“離子鍵”、“極性鍵”或“非極性鍵”),若將該固體投入到含有下列離子的溶液中:NO3-、HCO3-、CO32-、SO32-、SO42-、Na+,反應(yīng)完畢后,溶液中上述離子數(shù)目幾乎不變的有。(填離子符號(hào))
(5)元素⑦、⑧、⑨的離子半徑由大到小的順序是(用離子符號(hào)表示);元素⑨的最高價(jià)氧化物的水化物與元素⑥的最高價(jià)氧化物對(duì)應(yīng)的水化物反應(yīng)的離子方程式為。
(6)能比較元素⑦和⑧非金屬性強(qiáng)弱的實(shí)驗(yàn)事實(shí)是。(填字母序號(hào))
a.⑦的氫化物的酸性比⑧的氫化物的酸性弱
b.⑧的單質(zhì)R2與H2化合比⑦的單質(zhì)Q與H2化合容易,且HR的穩(wěn)定性比H2Q強(qiáng)
c.在⑦的氫化物H2Q的水溶液中通少量⑧的單質(zhì)R2氣體可置換出單質(zhì)Q組卷:91引用:2難度:0.5 -
 23.Ⅰ.某同學(xué)為探究元素周期表中元素性質(zhì)的遞變規(guī)律,設(shè)計(jì)了如下系列實(shí)驗(yàn)。
23.Ⅰ.某同學(xué)為探究元素周期表中元素性質(zhì)的遞變規(guī)律,設(shè)計(jì)了如下系列實(shí)驗(yàn)。
(1)將Na、K、Mg、Al各1mol分別投入到足量的同濃度的鹽酸中,試預(yù)測實(shí)驗(yàn)結(jié)果:與鹽酸反應(yīng)最劇烈,與鹽酸反應(yīng)產(chǎn)生的氣體最多(填元素符號(hào))。(2)向Na2S溶液中通入氯氣出現(xiàn)黃色渾濁,可證明Cl的非金屬性比S強(qiáng),反應(yīng)的離子方程式為:。
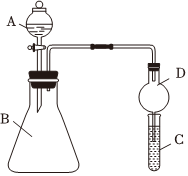
Ⅱ.利用如圖裝置可驗(yàn)證同主族元素非金屬性的變化規(guī)律
(1)儀器A的名稱為。
(2)實(shí)驗(yàn)室中現(xiàn)有藥品:①稀鹽酸 ②稀硝酸 ③Na2SiO3溶液 ④Na2CO3固體,請選擇合適藥品設(shè)計(jì)實(shí)驗(yàn)驗(yàn)證 N、C、Si的非金屬性的變化規(guī)律;裝置A、B中所裝藥品分別為、(填序號(hào))。但有同學(xué)認(rèn)為該裝置有缺陷,如何改進(jìn)?。
Ⅲ.(1)鋁是為數(shù)不多的能與強(qiáng)堿溶液反應(yīng)的金屬,請書寫鋁與氫氧化鈉溶液反應(yīng)的化學(xué)方程式。
(2)消除采礦業(yè)膠液中的氰化物(如KCN,C為+2價(jià)),經(jīng)以下反應(yīng)實(shí)現(xiàn):KCN+H2O2+H2O═A+NH3↑(已配平)。試指出A的化學(xué)式,如此反應(yīng)中有6.72L(標(biāo)準(zhǔn)狀況)氣體生成,轉(zhuǎn)移電子數(shù)目為。組卷:28引用:2難度:0.7


