2021-2022學年吉林省實驗中學高二(下)質檢化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題包括20小題,1—10題,每小題2分;11—20題,每小題2分,共50分。在每小題給出的四個選項中,只有一項符合題目要求。
-
1.生活中的化學無處不在,下列關于生活中的化學描述錯誤的是( )
A.可以用光譜分析的方法來確定太陽的組成元素是否含氦 B.壁虎在天花板上爬行自如是因為壁虎的腳與墻體之間有范德華力 C.汽油不易溶解于水是因為水分子的極性和汽油分子的極性不同 D.“挑盡寒燈夢不成”所看到的燈光和原子核外電子躍遷無關 組卷:82引用:7難度:0.5 -
2.下列有關說法不正確的是( )
A.CH4、C2H4、CO2分子中的鍵角依次增大 B.HF、HCl、HBr分子中共價鍵的鍵長依次增大 C.H2O、H2S、H2Se分子中共價鍵的鍵能依次減小 D.相同條件下,FCH2COOH的酸性弱于CH3COOH 組卷:26引用:1難度:0.7 -
3.下列化學用語的表達正確的是( )
A.原子核內有10個中子的氧原子: O168B.氯原子的結構示意圖: 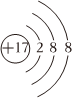
C.Fe3+的最外層電子排布式:3s23p63d5 D.基態銅原子的價層電子排布圖: 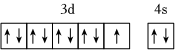 組卷:119引用:9難度:0.5
組卷:119引用:9難度:0.5 -
4.SiF4與SiCl4分子都是正四面體結構。下列判斷正確的是( )
A.鍵長:Si-F>Si-Cl B.鍵能:Si-F>Si-Cl C.沸點:SiF4>SiCl4 D.共用電子對偏移程度:Si-Cl>Si-F 組卷:136引用:7難度:0.7 -
5.下列化合物中含有手性碳原子的是( )
A.CCl2F2 B. 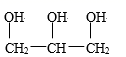
C.CH3CH2OH D. 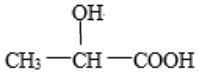 組卷:51引用:3難度:0.8
組卷:51引用:3難度:0.8 -
6.分子有極性分子和非極性分子之分。下列對極性分子和非極性分子的認識正確的是( )
A.只含非極性鍵的分子一定是非極性分子 B.含有極性鍵的分子一定是極性分子 C.非極性分子一定含有非極性鍵 D.O3是極性分子 組卷:24引用:1難度:0.7 -
7.在BrCH=CHBr分子中,C-Br鍵采用的成鍵軌道是( )
A.sp-p B.sp2-s C.sp2-p D.sp3-p 組卷:78引用:13難度:0.9 -
8.徐光憲在《分子共和國》一書中介紹了許多明星分子,如H2O2、CO2、BF3、CH3COOH等。下列說法正確的是( )
A.H2O2分子中的O為sp2雜化 B.CO2 分子中C原子為sp雜化 C.BF3分子中的B原子sp3雜化 D.CH3COOH分子中C原子均為sp2雜化 組卷:254引用:17難度:0.6
二、非選擇題:本題共4題,共50分。
-
23.中國科學技術大學俞書宏教授團隊和高敏銳教授課題組通過室溫過飽和溶液共沉積法,實現了無定形NiFeMo氧化物納米材料的宏量制備,該方法簡便快捷,反應幾分鐘即可一次性生產多達515克的產物,制備的無定形NiFeMo氧化物在堿性條件下展示出優異的OER催化活性,明顯優于結晶型NiFeMo氧化物。根據所學知識回答下列問題:
(1)區別結晶型NiFeMo氧化物和無定形NiFeMo氧化物最可靠的科學方法為,結晶型NiFeMo氧化物能自發呈現多面體外形,這種性質稱為晶體的。
(2)Mo為第五周期元素與Cr同族,則Mo的價層電子排布式為。
(3)配合物Ni(CO)4常溫下為液態,易溶于CCl4,苯等有機溶劑,是獲得高純度納米鎳的原料,Ni(CO)4是(填“極性”或“非極性”)分子。
(4)下列狀態的鐵中,電離最外層的一個電子所需能量最大的是(填編號)。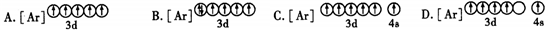
(5)FeCl3中的化學鍵具有明顯的共價性,蒸氣狀態下以雙聚分子存在的FeCl3的結構式為,其中Fe的配位數為。
(6)立方NiO(氧化鎳)晶體的結構如圖所示,其晶胞邊長為a pm,列式表示NiO晶體的密度為g/cm3(不必計算出結果,阿伏加德羅常數的值為NA)。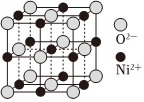 組卷:18引用:4難度:0.4
組卷:18引用:4難度:0.4 -
24.N、P、As、Sb均是第VA族的元素。
(1)上述元素的氫化物的沸點關系如圖所示,沸點:PH3<NH3,其原因是:;沸點:PH3<AsH3<SbH3,其原因是。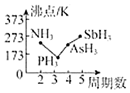
(2)某種磁性氮化鐵的晶胞結構如圖所示,該化合物的化學式為。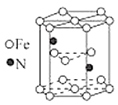
(3)磷化鋁熔點為2000°C,它與晶體硅的晶體類型相同,磷化鋁晶胞結構如圖所示。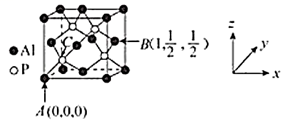
①磷化鋁晶體中磷與鋁微粒間的作用力為。
②圖中A點和B點的原子坐標參數如圖所示,則C點的原子坐標參數為。
③磷化鋁晶體的密度為ρg?cm3,用NA表示阿伏加德羅常數的數值,則該晶胞中距離最近的兩個鋁原子之間的距離為cm(填計算式)。組卷:4引用:1難度:0.5


