2023-2024學年新疆烏魯木齊十二中高三(上)月考化學試卷(8月份)
發(fā)布:2024/9/14 4:0:8
一、單項選擇題(15題每題3分共45分)
-
1.下列關于金屬及其化合物說法不正確的是( )
A.氧化鋁是冶煉金屬鋁的原料,也是一種耐火材料 B.硅酸干凝膠多孔吸水性強,常用作干燥劑,也可用作催化劑載體 C.目前用量最大、用途最廣的合金是鋁合金 D.SO2具有漂白性,常用于漂白紙漿、草帽辮等 組卷:85引用:2難度:0.6 -
2.下列有關化學用語正確的是( )
A.NH4Br的電子式: 
B.S2-的結構示意圖: 
C.N2的結構式:N=N D.原子核內有18個中子的氯原子: Cl3517組卷:19引用:3難度:0.8 -
3.設NA為阿伏加德羅常數(shù)的值,下列敘述正確的是( )
A.100g質量分數(shù)17%的H2O2溶液中極性鍵數(shù)目為NA B.一定條件下,足量N2與6molH2充分反應,生成NH3的分子數(shù)為4NA C.標準狀況下,11.2L一氯甲烷中含有的氯原子數(shù)為0.5NA D.常溫下,1L0.2mol/LNa2C2O4溶液中含 數(shù)目為0.2NAC2O2-4組卷:14引用:2難度:0.8 -
4.下列反應中,其有機產物的分子中含有三個官能團的是( )
A.1mol乙炔與2molHBr發(fā)生加成反應 B.甲苯硝化生成三硝基甲苯 C.1mol苯乙烯與1mol氯化氫發(fā)生加成反應 D.乙烯與水的加成反應 組卷:109引用:2難度:0.5 -
5.向含HCN的廢水中加入鐵粉和K2CO3可制備K4[Fe(CN)6],發(fā)生反應:6HCN+Fe+2K2CO3═K4[Fe(CN)6]+H2↑+2CO2↑+2H2O,下列說法錯誤的是( )
A.依據(jù)反應可知:Ka(HCN)>Ka1(H2CO3);還原性:Fe>H2 B.基態(tài)碳原子和基態(tài)氮原子的未成對電子之比為2:3 C.Fe位于周期表中第Ⅷ族;反應中Fe失去4s2電子 D.離子半徑大小:N3->O2- 組卷:105引用:6難度:0.6 -
6.設NA為阿伏加德羅常數(shù)的值,下列說法不正確的是( )
A.常溫常壓下,20g2H2O含有電子數(shù)為10NA B.環(huán)狀S8(  )分子中含有的S-S數(shù)為8NA
)分子中含有的S-S數(shù)為8NAC.100g質量分數(shù)為46%的酒精溶液含有氧原子數(shù)為4NA D.鋼鐵電化學腐蝕生成0.1molFe2O3?nH2O,則負極反應失電子數(shù)為0.4NA 組卷:13引用:2難度:0.5
二、綜合題(4題共55分,請根據(jù)答題卡題號及分值在各題目的答題區(qū)域內作答,超出答題區(qū)域的答案無效。)
-
18.(1)某蓄電池的正負極標志難以辨別,請設計實驗方案,將蓄電池的正負極辨別出來
。
(2)解釋下列化學反應的反應速率變化關系曲線
①將除去氧化膜的鎂條投入盛有稀鹽酸的試管中,產生氫氣的速率隨時間的變化關系如圖A所示,試解釋原因:。
②過氧化氫在酶的催化作用下的分解速率隨溫度的變化關系如圖B所示,試解釋原因:。
(3)氫能源是最具應用前景的能源之一,高純氫的制備是目前的研究熱點。可利用太陽能光伏電池電解水制高純氫,工作示意圖如圖。通過控制開關連接K1或K2,可交替得到H2和O2。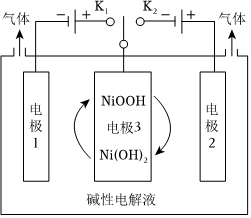
①制H2時,連接。
②改變開關連接方式,可得O2,電極反應式為。
③結合①和②中電極3的電極反應式,說明電極3的作用:。
(4)甲醇燃料電池DMFC可作電腦、汽車的能量來源。在實驗室完成一個實驗,用DMFC電解NaClO3溶液可制取NaClO4溶液,裝置如圖所示(其中DMFC以KOH作電解質)。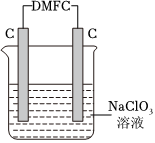
①寫出電源負極電極反應式:。
②寫出電解的總反應化學方程式:。組卷:26引用:1難度:0.5 -
19.化合物H具有類似龍涎香、琥珀香的氣味,香氣淡而持久,被廣泛用作香精的稀釋劑和定香劑。合成該化合物的某種途徑如圖所示。回答下列問題:
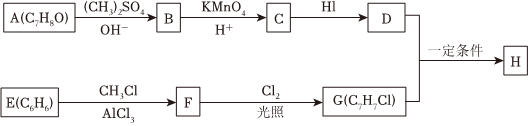
已知以下信息:
① (CH3)2SO4OH-
(CH3)2SO4OH- HI
HI ;
;
②A的苯環(huán)上有四種化學環(huán)境不同的氫原子,且取代基的位置相鄰;
③在D中滴加幾滴FeCl3溶液,發(fā)生反應顯出顏色;
④芳香烴F的相對分子質量介于90~100之間,0.1molF充分燃燒可生成7.2g水;
⑤R1COOH+RCH2ClR1COOCH2R+HCl。一定條件
(1)A的化學名稱是,由C生成D的反應的化學方程式為。
(2)由F生成G的反應的化學方程式為,反應類型為。
(3)H的結構簡式為。
(4)苯環(huán)上有三個取代基且其中兩個與A中所含的官能團相同,同時又能發(fā)生銀鏡反應的C的同分異構體有(不考慮立體異構)種,其分子中有5種化學環(huán)境不同的氫原子,且氫原子個數(shù)之比為1:1:2:2:2的同分異構體的結構簡式是(任寫一種即可)。
(5)苯酚經如圖所示步驟可合成化合物 。
。
反應1所用的試劑為,K的結構簡式為,反應3所用的試劑為。組卷:8引用:1難度:0.5


