2023-2024學年廣西南寧市武鳴高級中學高三(上)開學化學試卷
發布:2024/10/9 1:0:1
一、選擇題:本題共15小題,每小題3分,共45分。每小題只有一個選項符合題目要求。
-
1.中華民族文明源遠流長,眾多珍貴文物折射出五千年璀璨文明。下列文物的主要成分屬于無機非金屬材料的是( )
文物 



選項 A.西漢素紗禪衣 B.清紫檀雕花寶座 C.五羊方尊 D.青玉交龍鈕玉璽 A.A B.B C.C D.D 組卷:62引用:4難度:0.8 -
2.近年來,我國的航天技術發展迅速,天宮、天和、天問、神舟等體現了中國的強大科技力量。下列說法不正確的是( )
A.“天宮二號”部分零部件使用鈦合金,鈦合金中存在金屬鍵 B.“天和號”使用砷化鎵(GaAs)太陽能電池,供電時砷化鎵發生氧化還原反應 C.“天問一號”隔熱材料使用SiO2納米氣凝膠,SiO2屬于酸性氧化物 D.“神舟十三號”耐高溫材料使用酚醛樹脂,酚醛樹脂屬于合成高分子 組卷:126引用:3難度:0.8 -
3.湖南的美食有臭豆腐、蔥油粑粑、糖油坨坨、茶顏悅色等。下列有關敘述錯誤的是( )
A.“臭豆腐”的原材料之一為豆腐,豆腐在制作過程中涉及膠體的聚沉 B.“蔥油粑粑”中的“油”屬于酯類,是高分子 C.“茶顏悅色”中的奶油可通過植物油的氫化獲得 D.我國規定商家不得無償提供塑料袋,目的是減少聚乙烯等難降解的“白色污染” 組卷:16引用:3難度:0.7 -
4.下列有關化學用語表示正確的是( )
A.氨基的電子式: 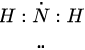 ?
?B.基態鉻原子的價層電子排布式:3d44s2 C.H2O的VSEPR模型: 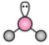
D.葡萄糖的實驗式:C6H12O6 組卷:9引用:2難度:0.7 -
5.設NA為阿伏加德羅常數的值,下列說法錯誤的是( )
A.常溫常壓下,12g金剛石中含有的C-C鍵數目為 2NA B.標準狀況下,11.2LHF含有0.5NA個HF分子 C.30gC2H6中含有極性共價鍵的數目為6NA D.1mol硝基與46g二氧化氮所含的電子數均為23NA 組卷:30引用:2難度:0.8 -
6.常溫下,下列各離子組在指定溶液中能大量存在的是( )
A.無色溶液:K+、 、MnO-4NO-3B.c(Fe3+)=0.1mol/L的溶液:H+、I-、Br- C.使石蕊變紅的溶液: 、NH+4、Cl-NO-3D.pH=13的溶液中:Na+、ClO-、 HCO-3組卷:79引用:2難度:0.6
二、非選擇題:本題共4小題,共55分。
-
18.為了實現“碳達峰”和“碳中和”的目標,將CO2轉化成可利用的化學能源的“負碳”技術是世界各國關注的焦點。?
方法Ⅰ:CO2催化加氫制甲醇。
以CO2、H2為原料合成CH3OH涉及的反應如下:
反應i:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)ΔH1
反應ii:CO2(g)+H2(g)?CO(g)+H2O(g)ΔH2=+41.0kJ?mol-1
反應iii:CO(g)+2H2(g)?CH3OH(g)ΔH3=-90.0kJ?mol-1
(1)計算反應i的ΔH1=。
(2)一定溫度和催化劑條件下,0.73molH2、0.24molCO2和0.03molN2(已知N2不參與反應)在總壓強為3.0MPa的密閉容器中進行上述反應,平衡時CO2的轉化率、CH3OH和CO的選擇性隨溫度的變化曲線如圖所示。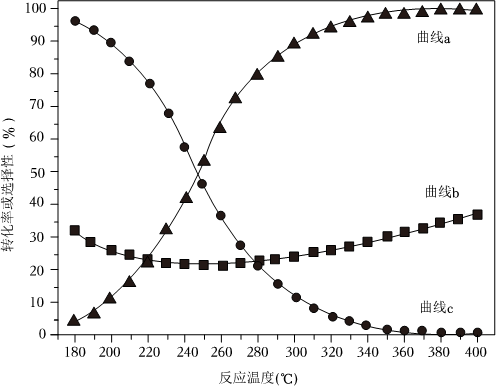 ?
?
①圖中曲線b表示物質的變化(填“CO2”“CH3OH”或“CO”)。
②上述反應體系在一定條件下建立平衡后,下列說法不正確的有(填字母)。
A.降低溫度,反應i~iii的正、逆反應速率都減小
B.向容器中再通入少量N2,CO2的平衡轉化率下降
C.移去部分H2O(g),反應iii平衡不移動
D.選擇合適的催化劑能提高CO2的平衡轉化率
E.平衡時CH3OH的體積分數一定小于50%
③某溫度下,t1min反應到達平衡,測得容器中CH3OH的體積分數為12.5%。此時用CH3OH的分壓表示0-t1時間內的反應速率v(CH3OH)=MPa?min-1。設此時n(CO)=amol,計算該溫度下反應ii的平衡常數Kx=(用含有a的代數式表示)。[已知:分壓=總壓×該組分物質的量分數;對于反應mA(g)+nB(g)?pC(g)+qD(g),Kx=,x為物質的量分數。]xp(C)?xq(D)xm(A)?xn(B)
方法Ⅱ:CO2電解法制甲醇
利用電解原理,可將CO2轉化為CH3OH,其裝置如圖所示: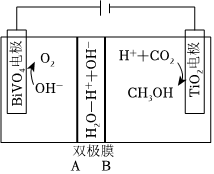
(3)雙極膜B側為(填“陰離子”或“陽離子”)交換膜。
(4)TiO2電極上電極反應方程式:。
方法Ⅲ:CO2催化加氫制低碳烯烴(2~4個C的烯烴)
某研究小組使用Zn-Ga-O/SAPO-34雙功能催化劑實現了CO2直接合成低碳烯烴,并給出了其可能的反應歷程(如圖所示)。H2首先在Zn-Ga-O表面解離成2個H*,隨后參與到CO2的還原過程;SAPO-34則催化生成的甲醇轉化為低碳烯烴。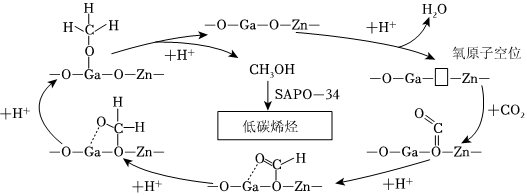 ?
?
注:?表示氧原子空位,*表示吸附在催化劑上的微粒。
(5)理論上,反應歷程中消耗的H*與生成的甲醇的物質的量之比為。組卷:69引用:2難度:0.5 -
19.化合物M是一種治療抑郁癥和焦慮癥的藥物,某研究小組以化合物I為原料合成化合物X的路線如圖(部分反應條件省略):
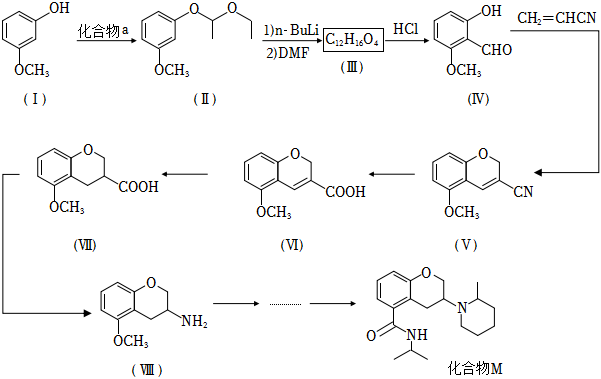
已知: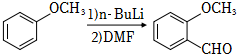
n-BuLi:CH3CH2CH2CH2
LiDMF:HCON(CH3)2
(1)化合物M中含氧官能團有(寫名稱)。
(2)下列說法正確的是。
A.化合物Ⅰ在水中的溶解度比間苯二酚大
B.可以用紅外光譜鑒別化合物Ⅰ和化合物Ⅳ
C.化合物Ⅴ中所有碳原子一定共平面
D.Ⅵ→Ⅶ的反應屬于還原反應
(3)已知Ⅰ→Ⅱ的反應是原子利用率100%的反應,且化合物a能使Br2的CCl4溶液褪色,則化合物a的結構簡式為。
(4)Ⅲ→Ⅳ的化學方程式是。
(5)化合物Ⅷ有多種同分異構體,同時符合下列條件的有種,其中核磁共振氫譜有三組峰,且峰面積之比為9:2:2的結構簡式為。
條件:a)含有一個苯環且苯環上有兩個取代基,其中一個為硝基;
b)不能使酸性高錳酸鉀溶液褪色。
(6)根據上述信息,寫出以苯酚為原料合成水楊酸(鄰羥基苯甲酸)的路線。(可使用本題中出現的有機試劑,無機試劑任選)組卷:99引用:2難度:0.3


