2021-2022學年陜西省西安市長安一中高一(下)期末化學試卷(理科)
發布:2024/11/2 22:30:2
一、選擇題(本題共20小題,每小題2分,共40分。每小題只有1個正確選項。)
-
1.NA表示阿伏加德羅常數的值,下列說法正確的是( )
A.標準狀況下,2.24LN2和O2的混合氣體中分子數為0.2NA B.1mol重水比1mol水多NA個質子 C.48g正丁烷和10g異丁烷的混合物中共價鍵數目為13NA D.92.0g甘油(丙三醇)中含有羥基數為1.0NA 組卷:11引用:2難度:0.7 -
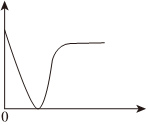 2.下列實驗過程中產生的現象與座標圖形相符合的是( )
2.下列實驗過程中產生的現象與座標圖形相符合的是( )A.稀硫酸滴加到Ba(OH)2溶液中(橫坐標是稀硫酸的體積,縱坐標為溶液的導電能力) B.鐵粉加到一定量CuSO4溶液中(橫坐標是鐵粉的質量,縱坐標為沉淀質量) C.CO2通入一定量NaOH溶液中(橫坐標是CO2的體積,縱坐標為溶液的導電能力) D.稀鹽酸滴加到一定量NaOH溶液中(橫坐標是稀鹽酸的體積,縱坐標為鈉離子物質的量) 組卷:81引用:18難度:0.7 -
3.在不同pH下含+5價V微粒的化學式不同,與pH關系如表所示。
不同價態V在溶液中顏色不同,如V2+(紫色)、V3+(綠色)、VO2+(藍色)、VO2+(黃色)、VO43-(無色)、V5O143-(紅棕色)等。下列說法正確的是( )含釩元素的不同微粒 VO2+ VO3- V2O74- VO43- pH 4~6 6~8 8~10 10~12 A.VO3-轉化為V2O74-的離子反應為2VO3-+H2O═V2O74-+2H+ B.含VO2+的溶液中滴加氨水有NH4VO3沉淀產生,該過程V元素被還原 C.酸性VO2+滴加燒堿溶液,溶液顯紅棕色的離子反應為5VO2++8OH-═V5O143-+4H2O D.紫色VSO4溶液中滴加酸性高錳酸鉀溶液,溶液顏色出現綠色→藍色→黃色,兩個過程均失去1mol電子 組卷:36引用:1難度:0.7 -
4.NaClO2是一種高效的漂白劑,實驗室中一種制備NaClO2的過程如圖所示,下列說法正確的是( )
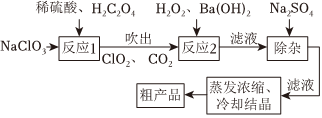
A.NaClO2的漂白原理與SO2相同 B.每生成1molClO2有1molH2C2O4被氧化 C.反應2過程中,H2O2作氧化劑 D.粗產品經重結晶可得到純度更高的NaClO2 組卷:6引用:3難度:0.7 -
5.據國外媒體報道,“火星快車”號和“金星快車”號探測器分別在火星和金星大氣層中發現了一種非常特殊的氣態化合物。這種化合物的存在不但會導致金星上的溫室效應被成倍的放大,而且可能會在火星上也誘發溫室效應的產生。它的結構式為16O=C=18O.下列說法正確的是( )
A.相同條件下16OC18O與16OC16O密度相同 B.16OC18O與16OC16O互為同位素 C.16OC18O與Na216O2反應生成的氧氣中沒有18O D.16OC18O與16OC16O的化學性質不同 組卷:57引用:7難度:0.8 -
6.下列實驗操作與實驗目的相符的是( )
序號 實驗操作 實驗目的 A 測定HF、HCl的熔點、沸點 比較F、Cl的非金屬性強弱 B MgSO4、Al2(SO4)3溶液中分別滴加足量氨水 比較鎂、鋁的金屬性強弱 C 將SO2氣體通入碳酸鈉溶液中 比較碳、硫的非金屬性強弱 D 向氯化銨、氯化鋁混合溶液中,滴加氫氧化鈉溶液至過量 比較NaOH、NH3?H2O、Al(OH)3的堿性強弱 A.A B.B C.C D.D 組卷:78引用:4難度:0.5 -
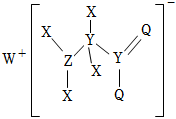 7.某種化合物的結構如圖所示,其中 X、Y、Z、Q、W 為原子序數依次增大的五種短周期元素,X的原子半徑是元素周期表所有元素中最小的,Q的核外最外層電子數與Y的核外電子總數相同。下列敘述不正確的是( )
7.某種化合物的結構如圖所示,其中 X、Y、Z、Q、W 為原子序數依次增大的五種短周期元素,X的原子半徑是元素周期表所有元素中最小的,Q的核外最外層電子數與Y的核外電子總數相同。下列敘述不正確的是( )A.W+的半徑小于Q的簡單離子半徑 B.元素非金屬性的順序為Y<Z<Q C.Z的氧化物對應的水化物是強酸 D.該化合物中Z滿足最外層8電子穩定結構 組卷:14引用:2難度:0.5 -
8.下列說法正確的是( )
A.凡是分子組成相差一個或幾個CH2原子團的物質,彼此一定是同系物 B.兩種化合物組成元素相同,各元素質量分數也相同,則兩者一定是同分異構體 C.相對分子質量相同的幾種化合物,互稱為同分異構體 D.組成元素的質量分數相同,且相對分子質量也相同的不同化合物,一定互為同分異構體 組卷:97引用:10難度:0.9
二、非選擇題(本題共5小題,共60分)
-
24.青蒿素是烴的含氧衍生物,為無色針狀晶體,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中幾乎不溶,熔點為156~157℃,熱穩定性差,青蒿素是高效的抗瘧藥。已知:乙醚沸點為35℃.從青蒿中提取青蒿素的方法之一是以萃取原理為基礎的,主要有乙醚浸取法和汽油浸取法。乙醚浸取法的主要工藝為:
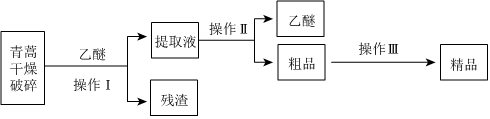
請回答下列問題:
(1)對青蒿進行干燥破碎的目的是。
(2)操作I需要的玻璃儀器主要有:燒杯、。
(3)在操作Ⅱ的蒸餾操作中,儀器選擇及安裝都正確的是(填標號)。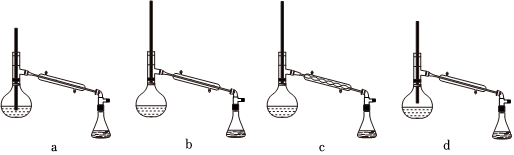
(4)操作Ⅲ的主要過程可能是(填字母)。
A.加水溶解,蒸發濃縮、冷卻結晶
B.加95%的乙醇,濃縮、結晶、過濾
C.加入乙醚進行萃取分液
(5)用下列實驗裝置測定青蒿素分子式的方法如下:
將28.2g青蒿素樣品放在硬質玻璃管C中,緩緩通入空氣數分鐘后,再充分燃燒,精確測定裝置E和F實驗前后的質量,根據所測數據計算。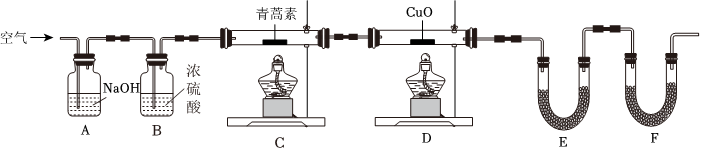
①裝置E中盛放的物質是,裝置F中盛放的物質是。
②該實驗裝置可能會產生誤差,造成測定含氧量偏低,改進方法是。
③用合理改進后的裝置進行試驗,稱得:
則測得青蒿素的最簡式是裝置 實驗前/g 實驗后/g E 22.6 42.4 F 80.2 146.2 。
(6)某學生對青蒿素的性質進行探究。將青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量較小,加熱并攪拌,青蒿素的溶解量增大,且溶液紅色變淺,說明青蒿素與(填字母)具有相同的性質。
A.乙醇 B.乙酸 C.乙酸乙酯 D.葡萄糖。組卷:18引用:3難度:0.4 -
25.有機物G(分子式為C16H22O4)是常用的皮革、化工、油漆等合成材料中的軟化劑,它的一種合成路線如圖所示:
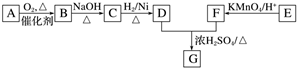
已知:①A是一種常見的烴的含氧衍生物,A的質譜圖中最大質荷比為46,其核磁共振氫譜圖中有三組峰,且峰面積之比為1:2:3;
②E是苯的同系物,相對分子質量在100~110之間,且E苯環上的一氯代物只有2種;
③1molF與足量的飽和NaHCO3溶液反應可產生氣體44.8L(標準狀況下);
④R1CHO+R2CH2CHONaOH△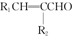 +H2O(R1、R2表示氫原子或烴基)。
+H2O(R1、R2表示氫原子或烴基)。
請根據以上信息回答下列問題:
(1)A的名稱為,請寫出A的一種同分異構體的結構簡式:。
(2)A轉化為B的化學方程式為。
(3)C中所含官能團的名稱為。
(4)E的結構簡式為。
(5)D和F反應生成G的化學方程式為。
(6)F有多種同分異構體,寫出同時滿足下列條件的F的同分異構體的結構簡式:(填寫兩種即可)。
①能和NaHCO3溶液反應;
②能發生銀鏡反應;
③遇FeCl3溶液顯紫色。組卷:6引用:2難度:0.5


