2019-2020學年安徽省六安一中高一(下)開學化學試卷(一)
發布:2024/12/7 9:0:2
一、選擇題共48分)本卷共16小題,每小題3分,每小題只有一個選項符合題意,答案填涂到答題卡上
-
1.設NA為阿伏加德羅常數的數值,下列說法中不正確的是( )
A.1 mol OH-含8NA個電子 B.1mol CH4和CO2混合氣體中含C原子數為NA C.常溫常壓下,48gO3含有的氧原子數為3NA D.標準狀況下,64gSO2中含有的原子數為3NA 組卷:22引用:2難度:0.8 -
2.下列敘述不正確的是( )
A.同溫同壓下,1molN2與1molCO可能具有不同的體積 B.同溫同壓下,二氧化碳與笑氣(化學式為N2O)的密度相同 C.質量相同的O2與O3一定具有相同的原子數 D.28gCO與1mol CO一定具有相同的碳原子數 組卷:43引用:2難度:0.6 -
3.下列指定反應的離子方程式正確的是( )
A.向Fe2(SO4)3溶液中加入過量鐵粉:Fe3++Fe═2Fe2+ B.用醋酸除水垢:CaCO3+2H+═Ca2++CO2↑+H2O C.向碳酸氫鈉溶液加入鹽酸溶液:H++CO32-+H+═CO2↑+H2O D.向Al2(SO4)3溶液中加入過量氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ 組卷:16引用:2難度:0.6 -
4.在無色透明溶液中,不能大量共存的離子組是( )
A.K+、Na+、SO42-、Cl- B.K+、Na+、HCO32-、NO3- C.Ca2+、Na+、OH-、HCO3- D.Ba2+、Na+、OH-、NO3- 組卷:20引用:2難度:0.6 -
5.對于白磷引起的中毒,硫酸銅溶液是一種解毒劑。有關反應如下:1lP+15CuSO4+24H2O═5Cu3P+6H3PO4+15H2SO4.下列關于該反應說法正確的是( )
A.Cu3P既是氧化產物也是還原產物 B.11molP參與反應時,該反應中有15mol電子發生轉移 C.P發生還原反應和氧化反應的物質的量之比為6:5 D.CuSO4僅作氧化劑。發生還原反應 組卷:41引用:4難度:0.5 -
6.將金屬鈉放入盛有下列溶液的小燒杯中,既有氣體產生。又有白色沉淀產生的是( )
A.NaHCO3溶液 B.MgSO4溶液 C.FeCl3溶液 D.HCl溶液 組卷:130引用:2難度:0.5
二、非選擇題共52分)
-
19.實驗室可用二氧化錳跟濃鹽酸反應制備并收集干燥純凈的氯氣。進行此實驗。所用儀器如圖:
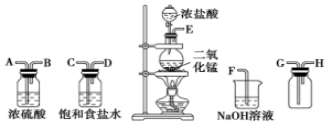
(l)連接上述儀器的正確順序 (填各接口處的字母):接;接;接;接。
(2)裝置中,飽和食鹽水的作用是;用濕潤的淀粉KI試紙可檢驗是否有Cl2產生。若有Cl2產生,可觀察到的現象是。
(3)寫出該實驗中氣體發生裝置中進行的反應的離子方程式。有興趣小組將實驗制得的氯氣通入熱的KOH溶液,得到了KClO3,寫出該反應的化學方程式。
(4)該興趣小組為比較Fe2+與I-還原性的強弱,向FeI2溶液中通入少量氯氣,再向其中加入(填試劑化學式),充分振蕩,下層溶液呈紫紅色。已知氧化性Cl2強于Fe3+,請寫出向FeI2溶液中通入過量氯氣反應的離子方程式。組卷:39引用:2難度:0.6 -
 20.純堿和小蘇打都是重要的化工原料,在生產和生活中有著廣泛的應用。
20.純堿和小蘇打都是重要的化工原料,在生產和生活中有著廣泛的應用。
(1)用潔凈的鉑絲蘸取Na2CO3溶液置于酒精燈火焰上灼燒,火焰呈色。
(2)實驗室中需0.2mol/L的Na2CO3溶液950mL,配制時應選用容量瓶的規格和稱取Na2CO3的質量分別是。
A.1000mL;21.2g B.950mL;20.14g C.500mL;21.2g D.500mL;10.6g
(3)若加熱10.00g的碳酸鈉和碳酸氫鈉的混合物,使碳酸氫鈉完全分解,混合物質量減少了2.48g。則原混合物中碳酸鈉的質量分數為。
(4)某同學為確定一包可能由碳酸鈉和碳酸氫鈉組成的白色混合物的成分,他取少量該白色物質溶于水,并向所得溶液中加入適量澄清石灰水,產生白色沉淀,據此該同學認為有碳酸鈉。你是否同意該同學的觀點,請你用適當的化學方程式闡述你的觀點。
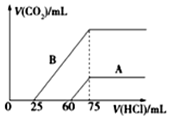
(5)取等物質的量濃度的NaOH溶液兩份A和B,每份10mL,分別向A、B中通入不等量的CO2,再繼續向兩溶液中逐滴加入0.1mol/L的鹽酸,標準狀況下產生的CO2的體積與所加鹽酸體積之間的關系如圖所示,試回答下列問題:
①曲線A表明,原NaOH溶液中通入CO2后,所得溶液加鹽酸后產生CO2氣體體積(標準狀況)的最大值為mL。
②曲線B表明,原NaOH溶液中通入CO2后,所得溶液中的溶質成分是,其物質的量之比為。組卷:115引用:2難度:0.7


