2022-2023學年福建省廈門市湖濱中學高二(上)期中化學試卷
發布:2024/12/26 8:0:14
一、選擇題(本題包括15小題,每小題3分共45分。每題只有一個選項符合題意)
-
1.化學與生產、生活、科技密切相關。下列有關說法不正確的是( )
A.2022北京冬奧會上用氫氣做交通車能源,理論上氫燃料電池汽車使用時不會產生污染物 B.植樹造林有利于實現“碳中和”,其捕獲和儲存大氣中的CO2過程涉及了氧化還原反應 C.將橋墩鋼鐵與外接電源負極相連的方法,稱為犧牲陽極的陰極保護法 D.“綠氫”燃料電池客車投入“冰絲帶”:光伏電解水制氫可作為“綠氫”的主要來源 組卷:8引用:1難度:0.6 -
2.化學用語是學習化學的重要工具,下列用來表示物質變化的化學用語中,正確的是( )
A.電解飽和食鹽水時,陽極的電極反應式為:2Cl--2e-═Cl2↑ B.氫氧燃料電池的負極反應式:O2+2H2O+4e-═4OH- C.粗銅精煉時,與電源正極相連的是純銅,電極反應式為:Cu-2e-═Cu2+ D.“Fe-稀硫酸-Cu原電池”中負極反應為:Fe-3e-═Fe3+ 組卷:29引用:3難度:0.7 -
3.下列操作或事實不能用勒夏特列原理解釋的是( )
A.CO中毒病人血液中存在化學平衡:CO(g)+Hb(O2)?O2(g)+Hb(CO),可用高壓氧艙治療CO中毒 B.H2(g)、I2(g)和HI(g)組成的平衡體系在壓縮體積后,氣體顏色最終比原來深 C.溴水中有下列平衡Br2+H2O?HBr+HBrO,當加入少量硝酸銀固體后,溶液顏色變淺 D.工業制取金屬鉀Na+KCl?NaCl+K,選取合適的溫度,使K變成蒸氣從體系中逸出 組卷:13引用:1難度:0.7 -
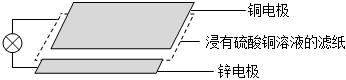 4.某興趣小組模擬紙電池進行實驗(如圖),有關說法正確的是( )
4.某興趣小組模擬紙電池進行實驗(如圖),有關說法正確的是( )A.該裝置把化學能轉化為電能 B.Zn為正極,發生氧化反應 C.工作時 由Zn電極向Cu電極遷移SO2-4D.工作一段時間后Cu電極質量不變 組卷:16引用:3難度:0.7 -
5.某反應過程中的能量變化如圖所示,下列熱化學方程式正確的是( )
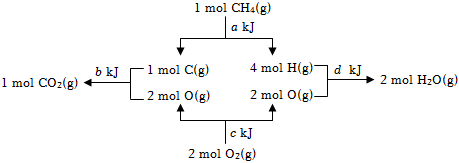
A.CH4(g)+2O2(g)═CO2(g)+2H2O(g) ΔH=-(a+c-b-d)kJ?mol-1 B.CH4(g)+2O2(g)═CO2(g)+2H2O(g) ΔH=-(b+2d-a-2c)kJ?mol-1 C.CH4(g)+2O2(g)═CO2(g)+2H2O(g) ΔH=-(a+2c-b-2d)kJ?mol-1 D.CH4(g)+2O2(g)═CO2(g)+2H2O(g) ΔH=-(b+d-a-c)kJ?mol-1 組卷:18引用:2難度:0.5 -
6.一定溫度下,某氣態平衡體系的平衡常數表達式為K=
,下列有關該平衡體系的說法正確的是( )c(C)?c2(D)c(A)?c2(B)A.升高溫度,平衡常數K一定增大 B.增大A的濃度,平衡向正反應方向移動 C.增大壓強,C的體積分數增大 D.升高溫度,若B的百分含量減少,則正反應是放熱反應 組卷:26引用:4難度:0.5
二、非選擇題(本題包括5小題,共55分。)
-
18.如圖是一個甲烷燃料電池工作時的示意圖,乙池中的兩個電極一個是石墨電極,一個是鐵電極,工作時M、N兩個電極的質量都不減少,請回答下列問題:
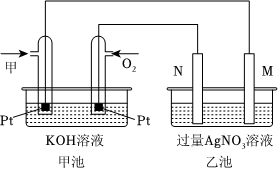
(1)通入甲烷的鉑電極上發生的電極反應式為。
(2)在此過程中,乙池中某一電極析出金屬銀4.32g時,甲池中理論上消耗氧氣為L(標準狀況下);若此時乙池溶液的體積為400mL,則乙池中溶液的H+的濃度為。
(3)若要用此裝置在鐵片上鍍銀,則①M電極的材料是,N電極的材料是,電解質溶液是。
②若M、N極質量相同,電鍍進行一段時間后,當兩極質量相差2.16g時,外電路共通過電子的物質的量是mol。組卷:75引用:3難度:0.6 -
19.某學習小組同學研究過氧化氫溶液與氫碘酸反應,查到一組室溫下的實驗數據,如下表所示:
(1)過氧化氫溶液與氫碘酸反應的化學方程式為實驗編號 ① ② ③ ④ ⑤ c0(H2O2)/mol?L-1 0.1 0.1 0.1 0.2 0.3 c0(HI)/mol?L-1 0.1 0.2 0.3 0.1 0.1 從混合至溶液出現棕黃色的時間/s 13 6.5 4.3 6.6 4.4 。
(2)本實驗的目的是。
(3)若該反應的速率方程可表示為v=kca(H2O2)cb(HI),對比表中數據可知a=,b=。
(4)資料顯示編號①的反應進行至20s時,測得氫碘酸的濃度為0.06mol?L-1,則20s內生成I2的平均速率v(I2)=。
(5)該實驗小組同學將氫碘酸用碘化鉀代替進行實驗,控制其他條件不變,未觀察到溶液變為棕黃色,卻觀察到有無色氣體生成。該小組同學認為KI可能對過氧化氫的分解起到催化作用。為驗證該猜想,該小組同學進行了如下實驗:取2支試管,分別加入2mL0.1mol?L-1H2O2溶液,然后向其中一支試管加入2mL0.1mol?L-1KI溶液,向另一支試管中加入,觀察現象。
(6)該小組同學將實驗編號④的溫度升高,發現到一定溫度下,溶液出現棕黃色所需時間變長,可能的原因是。組卷:12引用:2難度:0.4


