2021-2022學年湖北省武漢市青山區高二(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共15小題,每小題3分,共45分.在每小題給出的四個選項中,只有一項符合題目要求.
-
1.下列溶液呈中性的是( )
A.FeCl3溶液 B.Na2CO3溶液 C.NaCl溶液 D.CH3COOH溶液 組卷:12引用:2難度:0.7 -
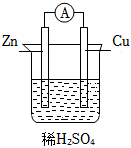 2.關于如圖所示原電池裝置,下列說法正確的是( )
2.關于如圖所示原電池裝置,下列說法正確的是( )A.電子從Zn電極流出,經導線流向Cu電極 B.Cu是正極反應物,得到電子 C.燒杯中換用蔗糖溶液,裝置仍可工作 D.稀H2SO4僅作離子導體 組卷:112引用:3難度:0.7 -
3.一定條件下,在2L密閉容器中發生反應:A(g)+3B(g)═2C(g)+4D(g),測得5min內,A的物質的量減小了10mol,則5min內該反應的化學反應速率是( )
A.υ(A)=1 mol/(L?min) B.υ(B)=1 mol/(L?min) C.υ(C)=1 mol/(L?min) D.υ(D)=1 mol/(L?min) 組卷:253引用:6難度:0.8 -
4.下列關于電化學腐蝕、防護與利用的說法中,正確的是( )
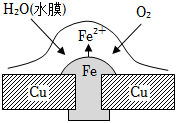

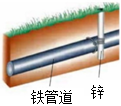
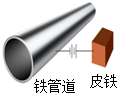
A.銅板打上鐵鉚釘后,銅板更易被腐蝕 B.暖氣片表面刷油漆可防止金屬腐蝕 C.連接鋅棒后,電子由鐵管道流向鋅 D.陰極的電極反應式為Fe-2e-═Fe2+ A.A B.B C.C D.D 組卷:207引用:9難度:0.4 -
5.下列關于化學反應方向的說法正確的是( )
A.凡是放熱反應都是自發反應 B.凡是熵增大的反應都是自發反應 C.凡是吸熱反應都不是自發反應 D.反應是否自發,需要綜合考慮反應焓變和熵變 組卷:194引用:4難度:0.7 -
6.根據給出資料,判斷以下說法中不正確的是( )
資料:
其中k為反應速率常數。化學反應 反應速率與參與反應物質的濃度的關系式 ①H2+I2=2HI(氣體反應) v=kc(H2)c(I2) ②CO+NO2═CO2+NO v=kc2(NO2) A.對于反應①,增大H2濃度(其他條件不變),反應速率增大 B.對于反應①,增大I2濃度(其他條件不變),反應速率增大 C.對于反應②,增大CO濃度(其他條件不變),反應速率增大 D.對于反應②,增大NO2濃度(其他條件不變),反應速率增大 組卷:125引用:3難度:0.8
二、非選擇題:本題共5小題,共55分.
-
19.t℃時,將3molA和2molB氣體通入體積為2L的密閉容器中(容積不變),發生如下反應:3A(氣)+B(氣)?xC(氣),2min時反應達到平衡狀態(溫度不變),剩余1.8molB,并測得C的濃度為O.4mol/L,請填寫下列空白:
(1)x=.
(2)比較達到平衡時,A、B兩反應物的轉化率:α(A)α(B)(填>、=或<)
(3)若繼續向原平衡混合物的容器中通入少量氦氣(氦氣和A、B、C都不反應)后,下列說法中正確的是(填寫字母序號)
A.化學平衡向正反應方向移動
B.化學平衡向逆反應方向移動
C.化學平衡不會發生移動
D.正、逆反應的化學反應速率將發生同等程度的改變
(4)若向原平衡混合物的容器中再充入3molA和2molB,在t℃時達到新的平衡,此時B的物質的量為n(B)3.6mol.(填“>”、“<”或“=”)
(5)如果將amolA、bmolB、cmolC在相同溫度和容器中進行反應,欲使反應達到平衡時C的物質的量分數與原平衡相等,起始加入的三種物質的物質的量n(A)、n(B)、n(C)之間應該滿足的等量關系式:(a,b及c的關系式)組卷:11引用:4難度:0.5 -
20.《我在故宮修文物》展示了專家精湛的技藝和對傳統文化的熱愛與堅守,也令人體會到化學方法在文物保護中的巨大作用。某博物館修復出土鐵器的過程如下。
(1)檢測銹蝕產物
鐵器在具有O2、主要成分的化學式 Fe3O4 Fe2O3?H2O FeO(OH) FeOCl 等環境中容易被腐蝕。
(2)分析腐蝕原理:一般認為,鐵經過了如下腐蝕循環。
Ⅰ.Fe轉化為Fe2+。
Ⅱ.Fe2+在自然環境中形成FeO(OH),該物質中鐵元素的化合價為。
Ⅲ.FeO(OH)和Fe2+反應形成致密的Fe3O4保護層,Fe2+的作用是。
a.氧化劑
b.還原劑
c.既不是氧化劑也不是還原劑
Ⅳ.Fe3O4保護層被氧化為FeO(OH),如此往復腐蝕。Fe3O4+O2+H2O═FeO(OH)(將反應補充完整)
(3)研究發現,Cl-對鐵的腐蝕會造成嚴重影響。化學修復:脫氯、還原,形成Fe3O4保護層,方法如下:
將鐵器浸沒在盛有0.5mol/L Na2SO3、0.5mol/L NaOH溶液的容器中,緩慢加熱至60~90℃.一段時間,取出器物,用NaOH溶液洗滌至無Cl-。
①檢測洗滌液中無Cl-的方法是。
②脫氯反應:FeOCl+OH-═FeO(OH)+Cl-.離子反應的本質是離子濃度的減小,FeOCl與FeO(OH)的溶解度更小的是。
③Na2SO3還原FeO(OH)形成Fe3O4的離子方程式是。組卷:115引用:2難度:0.6


