2021-2022學年河南省洛陽市高三(上)期中化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題共10小題,每小題只有一個選項符合題意,每小題2分,共20分)
-
1.反應8NH3+3Cl2═6NH4Cl+N2可用于氯氣管道的檢漏。下列表示相關微粒的描述錯誤的是( )
A.中子數為9的氮原子: N167B.N2分子的電子式: 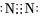
C.氨分子的比例模型為: 
D.Cl-的結構示意圖: 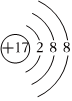 組卷:109引用:4難度:0.3
組卷:109引用:4難度:0.3 -
2.化學在人類社會發展中發揮著重要作用,下列事實不涉及化學反應的是( )
A.利用微生物降解水域中的有毒有害物質 B.小蘇打用作食品膨松劑 C.偏二甲肼用作發射“天宮二號”的火箭燃料 D.利用反滲透膜從海水中分離出淡水 組卷:8引用:2難度:0.8 -
3.設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.22.4L(標準狀況)HF所含的質子數為10NA B.16.25g FeCl3水解形成的Fe(OH)3膠體粒子數為0.1NA C.1LpH=4的0.1mol/LK2Cr2O7溶液中Cr2O72-離子數為0.1NA D.1L1mol/L氯化銨溶液中NH4+與H+離子數之和大于NA 組卷:19引用:2難度:0.8 -
4.室溫下,下列各組離子能大量共存的是( )
A.加入Mg能放出H2的溶液中:NH4+、Cl-、K+、SO42- B.NaHS溶液中:Cl-、K+、SO42-、Cu2+ C.通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3- D.無色溶液中:Na+、HCO3-、SO42-、Cl-、Al3+ 組卷:17引用:1難度:0.7 -
5.為除去括號內的雜質,下列各選項中所選用的試劑或方法正確的是( )
A.SO3(SO2),通過飽和亞硫酸氫鈉溶液 B.NaHCO3溶液(Na2CO3),通入過量的CO2氣體 C.MgCl2粉末(FeCl3),加入過量的NaOH溶液 D.CH4(C2H4),通過足量的酸性高錳酸鉀溶液 組卷:9引用:2難度:0.6 -
6.下列物質的轉化在給定條件下能實現的是( )
A.鋁土礦 AlO2-NaOH溶液Al(OH)3足量鹽酸Al2O3△B.鹽鹵(含MgCl2)溶液 Mg(OH)2石灰乳MgCl2鹽酸無水MgCl2蒸發結晶C.NaHCO3(s) Na2CO3(s)△NaOH(aq)飽和石灰水D.Fe2O3(s) Fe(s)AlFeCl3鹽酸組卷:26引用:1難度:0.5 -
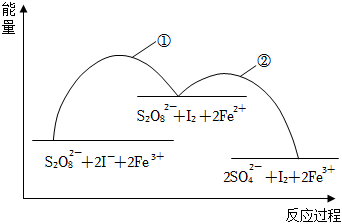 7.已知反應S2O82-(aq)+2I-(aq)?2SO42-(aq)+I2(aq),若向該溶液中加入含Fe3+的某溶液,反應機理如圖所示。下列有關該反應的說法正確的是( )
7.已知反應S2O82-(aq)+2I-(aq)?2SO42-(aq)+I2(aq),若向該溶液中加入含Fe3+的某溶液,反應機理如圖所示。下列有關該反應的說法正確的是( )
①2Fe3+(aq)+2I-(aq)?I2(aq)+2Fe2+(aq)
②2Fe2+(aq)+S2O82-(aq)?2Fe3+(aq)+2SO42-(aq)A.反應①和反應②相比,反應①更容易發生 B.Fe3+是該反應的催化劑 C.增大Fe3+的濃度,對反應速率無影響 D.若不加Fe3+,正反應的活化能比逆反應的活化能大 組卷:39引用:4難度:0.7 -
8.25℃時,下列說法正確的是( )
A.可溶性正鹽BA溶液呈中性,可以推測出BA為強酸強堿鹽 B.0.01mol/L、0.1mol/L的醋酸溶液的電離度分別為a1、a2,則a1<a2 C.pH=9的醋酸鈉溶液中,水電離出的c(H+)=10-5mol/L D.若測得NaR溶液pH=a,取該溶液10.0mL,升溫至50℃,測得pH=b,且a>b,可以說明HR是弱酸 組卷:23引用:3難度:0.7
三、填空題(本題共5小題,共50分)
-
24.NH4Al(SO4)2常作食品加工中的食品添加劑,用于焙烤食品;NH4HSO4在分析試劑、醫藥、電子工業中用途廣泛。請回答下列問題:

(1)NH4Al(SO4)2可作凈水劑,其原理是(用離子方程式說明)。
(2)相同條件下,0.1mol/L NH4Al(SO4)2溶液中的c()NH+4(填“等于”“大于”或“小于”)0.1mol/LNH4HSO4溶液中的c()。NH+4
(3)室溫時,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol?L-1 NaOH溶液,溶液pH與加入NaOH溶液體積的關系曲線如圖所示。
①試分析圖中a、b、c、d四個點,水的電離程度最大的是點。
②在b點,溶液中各離子濃度由大到小的排列順序是。
③由b到c發生反應的離子方程式為。組卷:21引用:1難度:0.7 -
25.固氮作用在中國科學院長春應用化學研究所張新波提出的一種獨特的鋰-氮氣電池(Li-N2)中實現了,該電池在放電過程中固定氮氣,充電過程中釋放氮氣,實現了氮氣的循環利用,并能對外提供電能。該電池在充電時發生的反應是:2Li3N═N2↑+6Li。現以該電池為電源進行如圖所示的實驗。
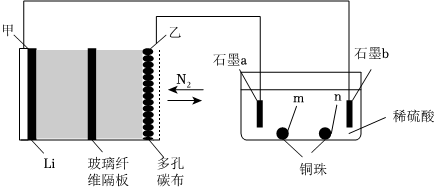
①多孔碳布起到的作用是。
②放電時,乙電極上的反應為。
③兩個石墨電極a、b上可能有銅析出的是石墨電極。組卷:2引用:2難度:0.6


