2022-2023學(xué)年天津外國語大學(xué)附屬外國語學(xué)校高二(上)期末化學(xué)試卷
發(fā)布:2024/10/22 0:0:2
一、單選題(每小題只有一個正確選項)
-
1.化學(xué)與生產(chǎn)生活密切相關(guān)。下列有關(guān)說法錯誤的是( )
A.家庭常用的鋅錳堿性電池放電時,將化學(xué)能轉(zhuǎn)化為電能 B.一次性保暖貼的主要原料是鐵粉、食鹽和活性炭,因發(fā)生電化學(xué)反應(yīng)放熱 C.明礬是一種良好的凈水劑,能夠殺菌消毒凈化水質(zhì) D.我國科學(xué)家突破的CO2人工合成淀粉技術(shù)有利于我國實現(xiàn)碳中和 組卷:14引用:2難度:0.6 -
2.下列表示正確的是( )
A.中子數(shù)為176的某核素: Ts176117B.基態(tài)鋅原子的價層電子排布式:3d104s2 C.26Fe3+的結(jié)構(gòu)示意圖: 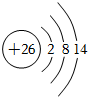
D.基態(tài)氮原子的軌道表示式: 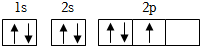 組卷:468引用:10難度:0.5
組卷:468引用:10難度:0.5 -
3.下列關(guān)于化學(xué)反應(yīng)與能量的說法中,不正確的是( )
A.化學(xué)反應(yīng)除了生成新物質(zhì)外,還伴隨著能量的變化 B.需要加熱的化學(xué)反應(yīng)都是吸熱反應(yīng) C.由H原子形成1molH-H鍵要釋放能量 D.反應(yīng)物的能量高于生成物的能量,反應(yīng)為放熱反應(yīng) 組卷:17引用:2難度:0.6 -
4.一定條件下,恒壓密閉容器中進行可逆反應(yīng):4NH3(g)+5O2(g)?4NO(g)+6H2O(g),則下列敘述中表示一定達到化學(xué)平衡狀態(tài)的是( )
A.單位時間生成nmolNO,同時生成nmolO2 B.混合氣體的壓強保持不變 C.v正(NH3)=v逆(NO) D.容器中NH3、O2、NO、H2O的物質(zhì)的量之比為4:5:4:6 組卷:57引用:1難度:0.5 -
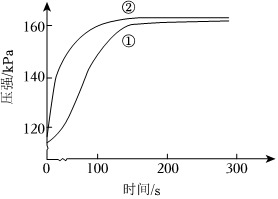 5.在兩個密閉的錐形瓶中,0.05g形狀相同的鎂條(過量)分別與2mL2mol?L-1的鹽酸和醋酸反應(yīng),測得容器內(nèi)壓強隨時間的變化曲線如圖。下列說法不正確的是( )
5.在兩個密閉的錐形瓶中,0.05g形狀相同的鎂條(過量)分別與2mL2mol?L-1的鹽酸和醋酸反應(yīng),測得容器內(nèi)壓強隨時間的變化曲線如圖。下列說法不正確的是( )A.曲線②代表醋酸與鎂條反應(yīng) B.反應(yīng)開始時,鹽酸與Mg反應(yīng)的更快 C.反應(yīng)結(jié)束時兩容器內(nèi)n(H2)基本相等 D.反應(yīng)過程中鹽酸c(H+)下降更快 組卷:22引用:6難度:0.6 -
6.已知某可逆反應(yīng):mA(g)+nB(g)?pC(g)ΔH在密閉容器中進行,如圖所示,反應(yīng)在不同時間t、溫度T和壓強p與反應(yīng)物B在混合氣體中的百分含量(B%)的關(guān)系曲線,由曲線分析下列判斷正確的是( )
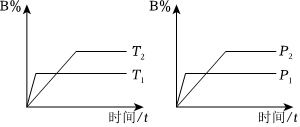
A.T1>T2,p1>p2,m+n<p,ΔH>0 B.T1>T2,p1>p2,m+n>p,ΔH>0 C.T1<T2,p1<p2,m+n<p,ΔH<0 D.T1<T2,p1<p2,m+n>p,ΔH<0 組卷:118引用:1難度:0.7 -
7.科學(xué)家通過觀察金星的酸性云層,分析出金星存在磷化氫氣體,從而推測金星可能存在生命的跡象。下列關(guān)于P元素的說法中,不正確的是( )
A.第一電離能:P<S B.原子半徑:S<P C.非金屬性:P<S D.電負性:P<S 組卷:81引用:4難度:0.6 -
8.反應(yīng)C(s)+H2O(g)?CO(g)+H2(g)在一容積可變的密閉容器中進行,若其它條件不變,只改變下列條件,對其反應(yīng)速率幾乎無影響的是( )
①增加C的量
②保持體積不變,充入N2使體系壓強增大
③升高溫度
④保持壓強不變,充入N2使容器體積變大A.只有① B.①② C.①④ D.②④ 組卷:265引用:5難度:0.5
二、填空題(每空2分)
-
25.能源、材料與生產(chǎn)生活和社會發(fā)展密切相關(guān)。
Ⅰ.光伏材料是指能將太陽能直接轉(zhuǎn)換成電能的材料。光伏材料又稱太陽能材料,只有半導(dǎo)體材料具有這種功能。可作太陽能電池材料的有單晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe等。
(1)寫出31號元素鎵(Ga)的原子結(jié)構(gòu)示意圖:。
(2)P、S、Ga電負性從大到小的順序為。
(3)As元素的第一電離能(填“大于”“小于”或“等于”)Se元素的第一電離能。
(4)寫出原子序數(shù)最小的第Ⅷ族元素基態(tài)原子的核外電子排布式:。
(5)寫出3p軌道上只有2個未成對電子的元素的符號:、。
Ⅱ.從化學(xué)鍵的角度分析,化學(xué)反應(yīng)的過程就是反應(yīng)物的化學(xué)鍵斷裂和生成物的化學(xué)鍵形成的過程。在化學(xué)反應(yīng)過程中,斷裂化學(xué)鍵需要消耗能量,形成化學(xué)鍵又會釋放能量。
已知:N2(g)+3H2(g)=2NH3(g)ΔH=akJ?mol-1,根據(jù)上表中所列鍵能數(shù)據(jù)可計算出a=化學(xué)鍵 H-H N-H N≡N 鍵能/(kJ/mol) 436 391 945 。組卷:102引用:1難度:0.7 -
26.工業(yè)生產(chǎn)和社會生活重要應(yīng)用。
Ⅰ.工業(yè)上用CO生產(chǎn)燃料甲醇,一定條件下發(fā)生反應(yīng):CO(g)+2H2(g)?CH3OH(g)。圖1表示反應(yīng)中能量變化;圖2表示一定溫度下,在容積為2L的密閉容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的濃度隨時間變化。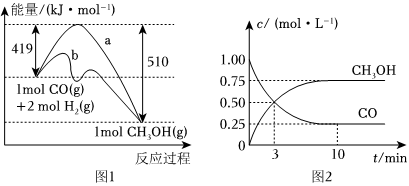
請回答下列問題:
(1)在圖1中,曲線(填“a”或“b”)表示使用了催化劑。
(2)該反應(yīng)屬于(填“吸熱”或“放熱”)反應(yīng)。
(3)增大反應(yīng)體系壓強,則該反應(yīng)化學(xué)平衡常數(shù)(填“增大”“減小”或“不變”)。
Ⅱ.CuSO4溶液是一種重要的銅鹽試劑,在電鍍、印染、顏料、農(nóng)藥等方面有廣泛應(yīng)用。某同學(xué)利用CuSO4溶液進行以下實驗探究:
(1)以CuSO4溶液為電解質(zhì)溶液進行粗銅(含Al、Zn、Ag、Pt、Au等雜質(zhì))的電解精煉,下列說法正確的是(填字母)。
a.溶液中Cu2+向陽極移動
b.粗銅接電源正極,發(fā)生還原反應(yīng)
c.電解后CuSO4溶液的濃度減小
d.利用陽極泥可回收Ag、Pt、Au等金屬
(2)圖中,Ⅰ是甲烷燃料電池(電解質(zhì)溶液為KOH溶液)的結(jié)構(gòu)示意圖,該同學(xué)想在Ⅱ中實現(xiàn)鐵上鍍銅: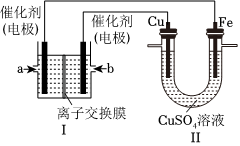
①b處通入的是(填“CH4”或“O2”),a處的電極反應(yīng)式為。
②當銅電極的質(zhì)量減輕3.2g,則消耗的CH4在標準狀況下的體積為。組卷:123引用:2難度:0.6


