2016-2017學年江蘇省常州市鐘樓實驗中學九年級(下)周末化學作業(4.1)
發布:2024/4/20 14:35:0
一、選擇題(共13小題,每小題3分,滿分39分)
-
1.塑化劑是塑料軟化劑,被禁止添加在食品里。塑化劑的下列性質屬于化學性質的是( )
A.無色粘稠液體 B.熔點-50℃ C.有慢性毒性 D.溶于多數有機溶劑 組卷:95引用:46難度:0.9 -
2.下列用品中,屬于合成材料的是( )
A.玻璃杯 B.金戒指 C.硬幣 D.橡皮筋 組卷:13引用:3難度:0.9 -
3.硫代硫酸鈉(Na2S2O3)俗稱海波,它屬于( )
A.酸 B.堿 C.鹽 D.氧化物 組卷:17引用:8難度:0.9 -
4.下列實驗操作正確的是( )
A. 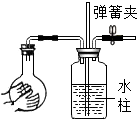 檢驗氣密性
檢驗氣密性B. 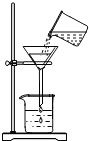
固液分離C. 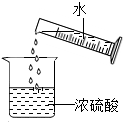
稀釋濃硫酸D. 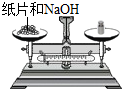
稱取氫氧化鈉組卷:13引用:10難度:0.9 -
5.下列實驗操作及現象合理的是( )
A.硫磺在空氣中燃燒發出黃色的火焰 B.紅磷在空氣中燃燒,產生大量白霧 C.選用10mL量筒量取5.5 mL 蒸餾水 D.鐵粉溶于足量稀硫酸中,形成黃色溶液 組卷:4引用:1難度:0.7 -
6.向AgNO3、Cu(NO3)2的混合溶液中加入一些鋅粉,完全反應后過濾。下列情況不可能存在的是( )
A.濾紙上有Ag,濾液中有Ag+,Cu2+,Zn2+ B.濾紙上有Ag,Cu,濾液中有Zn2+ C.濾紙上有Ag,Cu,Zn,濾液中有Zn2+ D.濾紙上有Ag,Cu,Zn,濾液中有Ag+,Cu2+ 組卷:7引用:1難度:0.7
二、非選擇題:
-
17.欲在室溫和1.01×105Pa條件下測定鎂的原子量.請利用下圖給定的儀器(盛放鎂條的隔板有小孔)組成一套實驗裝置(每種儀器只允許用一次).請回答下列問題:
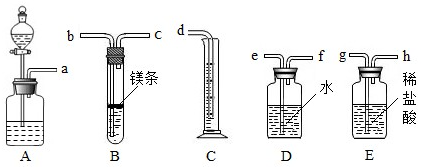
(1)假設氣流方向由左向右,則各儀器的接口連接的先后順序為a→→bc→fe→d(填寫字母).
(2)裝置A中的分液漏斗中盛放的液體作用是.
(3)連好儀器后,要進行的操作步驟有以下幾步:
①待儀器B中的物質恢復至室溫時,測量量筒C中水的體積(假設將測定的體積換算成標準狀況下為VmL);
②擦掉鎂條表面的氧化膜,將其置于天平上稱量(假設其質量為mg),并將其投入試管B 中;
③檢查各裝置的氣密性;
④旋開儀器A上分液漏斗的活塞,當鎂條完全溶解時再關閉活塞.
上述幾步操作的先后順序是.
(4)若未將試管B冷卻至室溫就測量量筒C中水的體積,這將會使所測鎂的相對原子質量的數據(填偏高、偏低或無影響).
(5)若未擦凈鎂條表面氧化膜就進行實驗,這將會使所測鎂的相對原子質量的數據(填偏高、偏低和無影響).
(6)甲、乙、丙三位同學用下圖裝置來測定一定質量的鎂完全反應后生成氫氣的體積: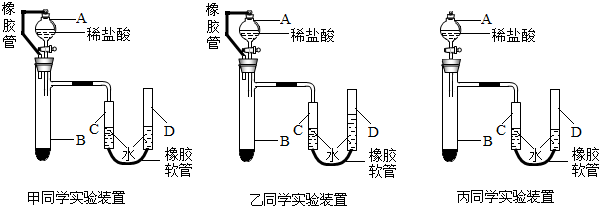
實驗步驟如下:
①檢查裝置的氣密性; ②向試管B中加入鎂條;
③準確操作,記錄C中液面刻度(C為帶有刻度的量氣管,D為可上下移動的水準管);
④由A向B中滴加稀鹽酸至過量;
⑤B中不再有氣體產生并恢復至室溫后,準確操作,記錄C中液面刻度,計算得到氣體的體積為Vml.
Ⅰ、甲同學檢查該裝置氣密性的方法是連接好裝置,從D管注水,C、D兩管液面形成高度差,做好標記,一段時間后,兩邊高度差(填“變大”、“變小”或“不變”),說明氣密性良好.為使測得的氣體體積更精確,記錄C中液面刻度時,除使視線與凹液面的最低處相平、冷至室溫外,還應;
Ⅱ、通常實驗前須估算藥品用量,如果實驗過程中,發現鹽酸的量不足,應中途加酸還是重新實驗?理由是.
Ⅲ、以上是乙、丙兩位同學所用實驗裝置,在步驟⑤讀數時所處的穩定狀態圖,則將會對實驗結果產生的影響是(假設其余步驟完善且操作準確無誤):乙,丙(填“偏大”、“偏小”或“無影響”).組卷:54引用:1難度:0.3 -
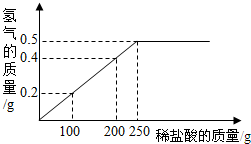 18.現有銅粉和鎂粉的混合物樣品,某興趣小組要測定樣品中鎂的質量分數.他們稱取該混合物樣品10g置于燒杯中,然后加入350g溶質質量分數為7.3%的稀鹽酸.所加稀鹽酸的質量與產生氫氣的質量關系如圖所示.
18.現有銅粉和鎂粉的混合物樣品,某興趣小組要測定樣品中鎂的質量分數.他們稱取該混合物樣品10g置于燒杯中,然后加入350g溶質質量分數為7.3%的稀鹽酸.所加稀鹽酸的質量與產生氫氣的質量關系如圖所示.
請計算:
(1)原混合物樣品中鎂的質量分數是.
(2)要將剩余的稀鹽酸完全反應掉,還需加入該樣品的質量是多少?(簡要寫出計算過程)組卷:36引用:4難度:0.3


