2021年北京市東城區(qū)高考化學二模試卷
發(fā)布:2024/4/20 14:35:0
一、本部分共14題,每題3分,共42分。在每題列出的4個選項中,選出最符合題目要求的一項。
-
1.下列三星堆出土的文物屬于合金制品的是( )
A. 
青銅人面具B. 
橢圓形玉器C. 
陶三足炊器D. 
帶孔海貝殼組卷:33引用:1難度:0.9 -
2.下列化學用語表達正確的是( )
A.乙烯的實驗式:C2H4 B.電鍍銅時,鐵制鍍件上的電極反應式:Fe-2e-═Fe2+ C.NH4Cl在水中的電離方程式:NH4Cl?NH4++Cl- D.用電子式表示NaCl的形成過程:  組卷:24引用:1難度:0.6
組卷:24引用:1難度:0.6 -
3.配制100mL 1.00mol?L-1NaOH溶液的操作如下所示。下列說法不正確的是( )
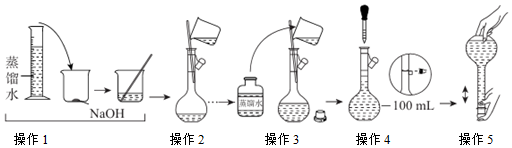
A.操作1前稱取NaOH的質(zhì)量為4.0g B.操作2前NaOH溶液需恢復至室溫 C.操作3和操作4分別為洗滌和定容 D.操作5后液面下降,需補充少量水至刻度線 組卷:54引用:2難度:0.7 -
4.化學與生活密切相關,下列說法正確的是( )
A.脂肪屬于天然高分子,可用于生產(chǎn)肥皂 B.聚丙烯酸鈉具有吸水保濕性,可用于干旱地區(qū)植樹造林 C.纖維素在人體內(nèi)水解最終產(chǎn)物為葡萄糖,可作為人類的營養(yǎng)食物 D.聚氯乙烯是一種熱穩(wěn)定性塑料,可用于制作食品包裝袋等薄膜制品 組卷:43引用:1難度:0.7 -
5.下列氣體的驗證方法沒有涉及氧化還原反應的是( )
A.氧氣--帶火星的小木條復燃 B.氯氣--濕潤的有色紙條褪色 C.乙烯--酸性高錳酸鉀溶液褪色 D.氨氣--濕潤的紅色石蕊試紙變藍 組卷:20引用:1難度:0.7 -
6.根據(jù)元素周期律,下列說法正確的是( )
A.原子半徑:K>Mg>Na B.堿性:NaOH>Mg(OH)2>Ca(OH)2 C.酸性:HCl>H2S,表明Cl的非金屬性強于S D.熱穩(wěn)定性:CH4>SiH4,表明C的非金屬性強于Si 組卷:42引用:2難度:0.6
二、本部分共5題,共58分。
-
18.碳酸鍶(SrCO3)為白色,難溶于水的固體,在電子工業(yè)中有泛應用。一種由天青石精礦(含SrSO4)制備高純SrCO3的方法如下:
天青石精礦粗SrCO3碳化劑過濾含Sr2+溶液精制高純SrCO3碳化劑過濾
已知:
ⅰ.BaSO4、SrCO3、BaCO3和SrSO4均難溶于水,在相同溫度下的溶解度(S)關系如下:S(BaSO4)≈S(SrCO3)<S(BaCO3)<S(SrSO4)
ⅱ.幾種氫氧化物在不同溫度下的溶解度:
(1)粗SrCO3的制取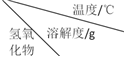
20 40 60 80 90 100 Sr(OH)2 1.77 3.95 8.42 20.2 44.5 91.2 Ba(OH)2 3.89 8.22 20.94 101.4 - - Ca(OH)2 0.173 0.141 0.121 0.094 0.086 0.076
①碳化劑一般選擇Na2CO3溶液或(NH4)2CO3溶液。寫出SrSO4轉化為SrCO3的離子方程式:。
②實驗發(fā)現(xiàn),當溫度和碳化劑的物質(zhì)的量濃度均相同時,SrSO4在Na2CO3溶液中的轉化速率大于在(NH4)2CO3溶液中的。從鹽類水解的角度解釋其原因是。
(2)含Sr2+溶液的精制
ⅰ.將粗SrCO3溶解于適量鹽酸中,過濾得到濾液(金屬陽離子有:Sr2+、Ba2+、Mg2+和Ca2+);
ⅱ.加NaOH溶液調(diào)節(jié)上述濾液pH至12~13.過濾得到濾液X和濾渣A;
ⅲ.將濾液X置于90~95℃的水浴中加熱,生成白色沉淀B,趁熱過濾棄去沉淀,得到濾液Y,并將ⅱ中的濾渣A重新投入濾液Y中浸泡(保持溫度為90~95℃);
ⅳ.重復ⅱ和ⅲ3~4次,最后得到熱的濾液Z;
ⅴ.趁熱向濾液Z中加入適量稀硫酸,過濾得到精制含Sr2+溶液。
①濾渣A中含有Sr(OH)2和。
②白色沉淀B的主要成分是。
③ⅳ的目的是。
④ⅴ中反應的離子方程式是。組卷:35引用:1難度:0.4 -
19.某化學興趣小組為探究高錳酸鉀與銅的反應,設計實驗如下:
資料:實驗一 現(xiàn)象 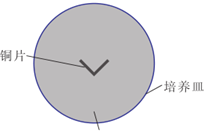
10mL 0.005mol?L-1KMnO4酸性溶液一段時間后,培養(yǎng)皿中由銅片向外側依次呈現(xiàn):
A區(qū)澄清且?guī)缀鯚o色;
B區(qū)底部覆蓋棕黑色固體;
C區(qū)澄清且紫色變淺
a.Cu+在酸性溶液中不能穩(wěn)定存在:2Cu+═Cu+Cu2+
b.MnS為粉紅色沉淀、溶于強酸;CuS為黑色沉淀、不溶于強酸
(1)Cu被氧化成,依據(jù)是。
(2)為探究MnO4-的還原產(chǎn)物,取A區(qū)中溶液(填操作和現(xiàn)象),證明有Mn2+生成。
(3)A區(qū)中KMnO4與Cu反應的離子方程式是。
(4)經(jīng)檢驗,B區(qū)的棕黑色固體是MnO2,從溶液中離子擴散的角度,結合離子方程式解釋B區(qū)和C區(qū)中的現(xiàn)象:。
(5)小組同學又進行了以下定量實驗:
通過計算,分析溶液紫色變淺而未完全褪色的原因:實驗一 現(xiàn)象 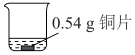
25mL 0.005mol?L-1KMnO4酸性溶液一段時間后,銅片質(zhì)量減少了0.02g,溶液中無固體析出、溶液紫色變淺 。組卷:75引用:1難度:0.5


